随着经济的发展和皮肤问题的日益普遍,皮肤医学美容越来越受到重视。伤口愈合不良、衰老和色素沉着等皮肤疾病不仅影响外观,还会给患者带来身体和心理问题,甚至给家庭和社会带来沉重的经济负担。
然而,由于其发病的复杂性,目前的治疗方案无法产生最佳效果,迫切需要新的有效治疗方法。间充质干细胞 (MSCs) 及其分泌组学治疗是一种新的再生医学疗法,可促进和调节内源性干细胞群和/或补充细胞库以实现组织稳态和再生。它在多项与皮肤相关的体内和体外研究中表现出显着的优势,有助于改善皮肤状况并促进皮肤美观。
间充质干细胞在皮肤医学美容中的作用:从基础到临床
近日,发表在“Stem Cell Research&Therapy”期刊杂志上一篇名为“Insights into the role of mesenchymal stem cells in cutaneous medical aesthetics: from basics to clinics(深入了解间充质干细胞在皮肤医学美容中的作用:从基础到临床)的文献综述,该综述表明了间充质干细胞疗法通过旁分泌作用、免疫调节、炎症管理和组织分化,在促进皮肤修复和再生方面表现出了巨大的潜力。

皮肤的作用丨皮肤的内部衰老丨皮肤的外部衰老丨
皮肤是人体最大的器官,除了具有美学价值外,还具有许多重要的生理和生物学功能,如保护身体免受有害物质的侵害、帮助感知各种感觉以及调节体温。皮肤问题不仅降低患者的生活质量和造成心理压力,还会给家庭和社会带来沉重的经济负担。许多皮肤病与成人抑郁症有关。人类皮肤伤口会造成显著的流行病学和经济成本。
随着人口老龄化和影响伤口愈合的已知合并症发病率的增加,其影响将持续增加。色素减退会引起美观和心理问题,降低患者的生活质量。疤痕是伤口愈合后的常见现象,严重影响伤口外观并带来美观、功能和/或心理问题。尤其是面部疤痕更容易导致功能缺陷和心理负担。预计到2027年疤痕治疗市场规模将增长至约320亿美元。

因此,随着经济的增长,近年来皮肤美学越来越流行。
- 内部衰老和众多外部刺激物的刺激最终会影响皮肤结构,导致皱纹、脱发等美容问题以及屏障维持障碍等功能问题。皮肤的内部衰老机制复杂,包括基因突变的积累、DNA损伤、细胞老化、炎症和氧化应激(OS)。
- 外部衰老是多种环境原因共同作用的结果,包括紫外线(UV)、PM2.5、二氧化氮、地面臭氧、香烟烟雾、食品添加剂和重金属离子,最终导致DNA损伤和细胞功能障碍。这对患者的生活产生了重大影响,导致各种生理和心理问题(图1)。
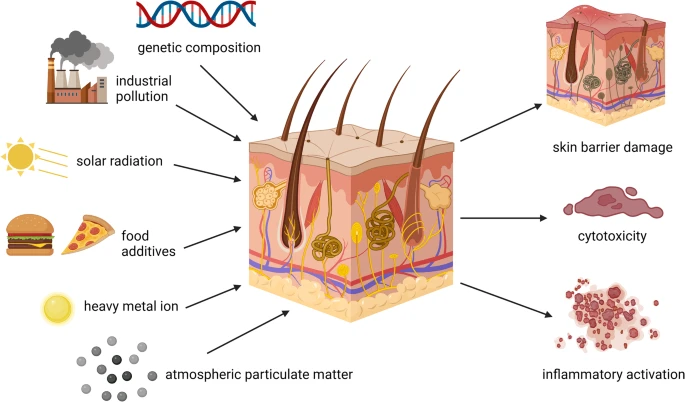
基因组成、环境污染、饮食添加剂、太阳辐射、重金属暴露和空气中的颗粒物都可能导致皮肤细胞毒性、皮肤屏障退化和炎症反应激活
因此,越来越多的人开始寻求有效、安全的医学美容治疗方法来解决皮肤问题。改善皮肤状况的方法有很多,例如通过皮肤护理、药物、激光和手术。然而,这些方法各有缺点,无法在皮肤修复和再生方面产生预期的效果。
作为当前的热门研究课题,干细胞治疗通过促进和控制内源性干细胞群和/或补充细胞库以实现组织稳定和再生,构成了再生医学的一个重要分支,并取得了卓越的治疗效果。最近的研究表明,间充质干细胞可以促进皮肤伤口愈合、色素沉着调节和抗衰老,作为皮肤医学美容的治疗选择。
我们系统地在PubMed和Web of Science中搜索了1975年至2024年2月期间与间充质干细胞、皮肤美容、伤口愈合、疤痕修复、皮肤年轻化和抗色素沉着相关的论文。
在这里,我们将描述间充质干细胞及其分泌组学在皮肤医学美容中的过程和用途的最新发现,例如伤口愈合、疤痕修复、皮肤年轻化和色素沉着修饰。更深入地了解它们各自的作用将阐明干细胞疗法在皮肤医学美容中的应用,为未来提供新的策略。
间充质干细胞及其分泌组在皮肤医学美容中的作用
间充质干细胞
间充质干细胞是多能干细胞,它们来自多种身体组织,包括骨髓、脐带、肌肉、脂肪组织和牙齿。来自不同组织的MSCs具有不同的生物学特性,这可以通过分化能力和分泌因子的差异来证明(图2)。
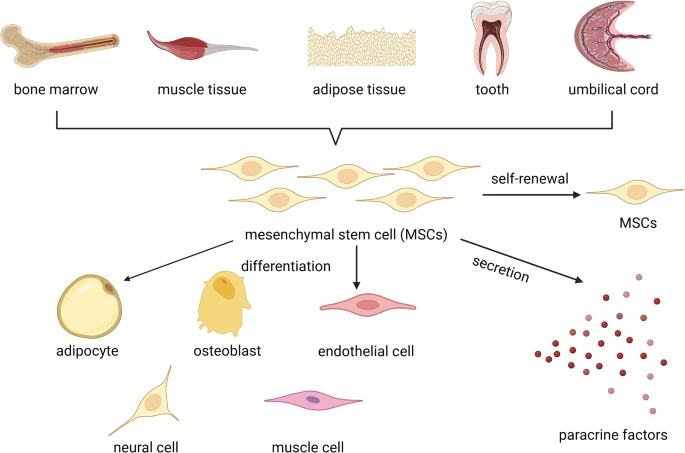
MSCs可来源于多种组织,如骨髓、肌肉组织、脂肪组织、牙齿和脐带等。MSCs可通过自我更新、分化和分泌发挥作用
MSCs可用于治疗软组织填充和再生、毛发再生、减少疤痕和抗皮肤衰老。一些研究发现,MSCs能够通过增加皮肤厚度、胶原蛋白形成和减少皱纹来改善皮肤健康。
- 从机制上讲,MSCs可能存在于损伤部位并释放伤口修复细胞因子,如血小板衍生的生长因子 (PDGF)、胰岛素样生长因子1 (IGF-1) 和白细胞介素8 (IL-8),控制炎症细胞并减少纤维化。此外,它还可以通过分泌生长因子、趋化因子、细胞因子和血管生成因子来调节免疫反应并刺激组织再生。
脂肪干细胞 (ADSC) 和骨髓间充质干细胞 (BMMSC) 已被研究并用于限制疤痕形成、刺激胶原蛋白生成、改善肤色和抗衰老。
间充质干细胞分泌组
MSCs可以分泌或释放大量生长和营养物质到细胞外环境中,形成所谓的分泌物组。这包括可溶性部分和细胞外囊泡 (EV) 部分。EV在运送不同遗传物质和蛋白质方面发挥着重要作用。
根据EVs的大小、内容和来源,EVs分为外泌体(Exo)、微泡(MV)和凋亡囊泡。其中,外泌体得到了广泛的研究,它是由多泡体(MVB)形成的微小颗粒(大小为40-120纳米)。外泌体包括多种生理活性大分子,包括在细胞生物调节中重要的核酸(如miRNA、IncRNA、CircRNA和DNA)、蛋白质和脂质。四跨膜蛋白(CD9、CD63、CD8和CD86)、膜连接蛋白和热休克蛋白(HSP60、HSP70和HSP90)在外泌体中含量丰富(图3)。
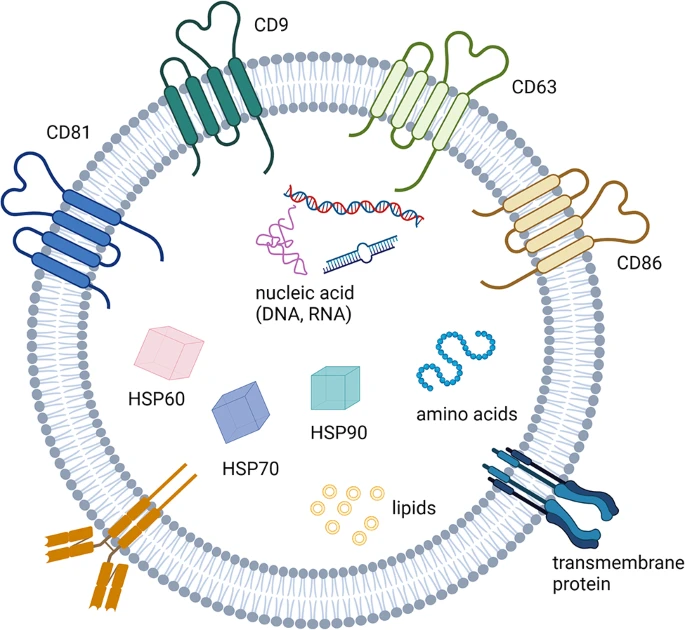
外膜含有四酯蛋白(CD9、CD63、CD81和CD86)和跨膜蛋白。外膜含有热休克蛋白(HSP60、HSP70和HSP90)、核酸、氨基酸和脂质
外泌体通过将其内容物直接注射到细胞中发挥作用,避免了需要专门的受体表达。因此,外泌体可以作为细胞间通讯载体,帮助克服生物界限。根据细胞的来源,外泌体拥有独特的蛋白质和核酸,它们通过细胞间通讯支持组织再生,并通过免疫调节功能、抗氧化应激和其他机制参与控制细胞凋亡(图4)。

分泌细胞受刺激,将早期内体转化为多泡体,多泡体通过与细胞膜融合分泌外泌体,外泌体再携带各种物质进入受体细胞
外泌体可以调节重要的生物学功能,如细胞分裂、迁移、分化和死亡。研究表明,内源性外泌体可以在多种皮肤细胞中穿梭,它们介导的信息和细胞间接触是维持细胞功能和组织稳态所必需的。来自干细胞的外泌体有望成为再生医学和美容医学的一种有用治疗方法,特别是在避免和减少疤痕、调节色素沉着和促进毛发生长方面。
间充质干细胞在皮肤医学美容中的作用:从基础到临床
间充质干细胞促进伤口愈合
MSCs通过多种机制达到促进伤口愈合的效果。首先,起作用的是MSCs的多向分化能力。MSCs可发育成多种细胞,例如ADSCs可发育成脂肪细胞、内皮细胞、骨骼肌细胞和平滑肌细胞,以增强皮肤伤口愈合。
因此,在整个再生和修复阶段,新循环系统的形成对整个愈合过程至关重要。受损的伤口血管重建会阻碍愈合并导致慢性伤口的发展。ADSC还可以分化为骨骼肌细胞,促进组织愈合。
MSC的旁分泌功能也至关重要。MSC可以在受伤部位定植并表达高水平的伤口愈合细胞因子,如IGF-1、PDGF和IL-8,从而调节炎症细胞并下调纤维化。特别是ADSC,可以产生健康伤口修复所需的几乎所有生长因子,如血管内皮生长因子 (VEGF)、肝细胞生长因子 (HGF)、碱性成纤维细胞生长因子 (bFGF) 和PDGF。它们还可以在缺氧环境下刺激慢性伤口中这些生长因子的排泄。MSC还能促进新血液形成、调节免疫反应并抑制过度炎症。
在伤口愈合的这个阶段,MSC可增强血管生成并促进功能性血管系统的生长。MSC可通过释放促血管生成因子(如VEGF、缺氧诱导因子1 (HIF-1)、上皮生长因子 (EGF) 和CXC基序趋化因子配体12 (CXCL12) )以及分泌各种可改善血管稳定性和保护性的分子来促进成人新血管形成。ADSC可释放血管生成细胞因子(如TGF-β、VEGF、HGF、bFGF、PDGF和血管生成素1 (Ang-1) ),这些因子可增加肉芽组织中的血管生成,增强局部血液循环,加速缺血部位的组织再生,并缩短愈合时间。
由于旁分泌功能是MSC的主要作用机制之一,人们对MSC的分泌组学进行了深入研究。下面将详细介绍。
- 例如,ADSC胞外囊泡通过增加衰老生物标志物VEGF、VEGF受体2 (VEGFR2) 和衰老标志蛋白30 (SMP30) 的磷酸化,同时抑制ROS和炎性细胞因子如白细胞介素-1 (IL-1)、TNF-α和白细胞介素-6 (IL-6) 的产生来促进伤口愈合。
- Li等人发现,当给糖尿病大鼠注射高表达NF-E2相关因子2 (Nrf2) 的ADSC外泌体时,其足部伤口溃疡面积大大减少。其主要机制是ADSC-exos通过调节III型/I型胶原蛋白、TGF-β3/TGF-β1和MMP-3/金属蛋白酶组织抑制剂1 (TIMP-1) 的比例并促进HDF分化,改善ECM重塑并减少疤痕形成。
为了防止切口治疗模型中的疤痕形成,ADSCs外泌体在恢复期早期增加I型和III型胶原蛋白的形成,同时抑制伤口愈合后期的胶原蛋白产生(图5)。
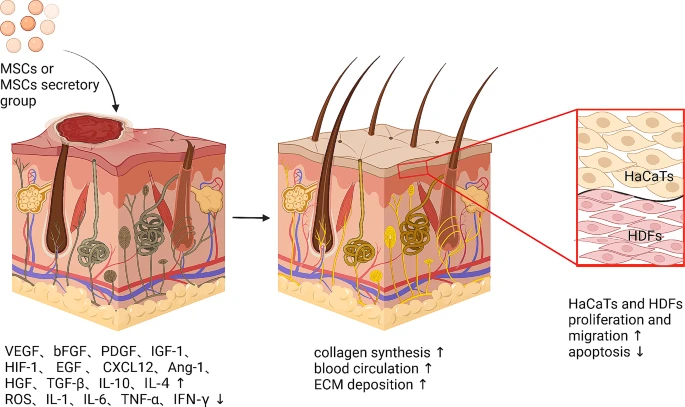
在损伤皮肤中,MSCs促进VEGF、bFGF、PDGF、IGF-1、HIF-1、EGF、CXCL12、Ang-1、HGF、TGF-β、IL-10、IL-4的分泌,抑制TNF-α、IFN-γ、IL-1、IL-6的分泌和ROS的水平,导致HaCaTs和HDFs分化迁移增强、凋亡减少,从而促进皮肤胶原合成、造血形成和ECM沉积,导致皮肤创面愈合的趋势
间充质干细胞促进疤痕修复
大量研究证明,MSC既能促进伤口愈合,又能减少疤痕形成。Fang等人发现,UMSC可减少小鼠皮肤缺损模型中的疤痕发展和肌成纤维细胞生成。
MSCs的旁分泌活性在这方面至关重要。MSCs产生多种抗纤维化介质和生长因子,包括HGF、IL-10和肾上腺髓质。迁移到损伤部位的MSCs会释放HGF和前列腺素E2,它们会抑制肌成纤维细胞分化并避免上皮-间质转化。MSCs还可能影响ECM和成纤维细胞的形成,从而更好地形成疤痕。
这些数据表明,MSC-exos,尤其是ADSC-exos,可以调节成纤维细胞活性以及胶原蛋白的沉积或排列,从而促进无瘢痕模式(图6)。
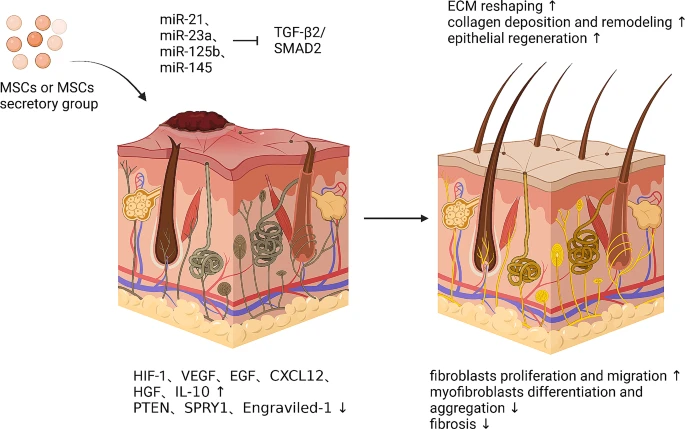
MSCs具有刺激疤痕皮肤释放HIF-1、VEGF、EGF、CXCL12、HGF和IL-10,同时抑制PTEN、SPRY1和Engraviled-1释放的能力。MSCs分泌的外泌体含有miR-21、miR-23a、miR-125b和miR-145,可抑制TGF-β2/SMAD2通路,促进成纤维细胞分化和迁移,抑制肌成纤维细胞分化和聚集。这可以减少纤维化,促进ECM重塑、胶原沉积重塑和上皮再生
在纳米材料的应用方面,Zheng等发现富含MSCs的水凝胶有助于皮肤伤口愈合,并形成具有毛囊的无疤痕组织。当与多功能多糖敷料支架结合使用时,ADSC-exos可通过增加细胞增殖、颗粒组织生长、胶原积累、上皮再生和重塑来加速恢复,同时减少疤痕组织发育和皮肤附着再生。
表1指出了使用间充质干细胞治疗不同类型伤口的最新临床研究。预计未来将开展更多MSCs移植临床研究。
| 来源 | 研究内容 | 发现 | 参考 |
|---|---|---|---|
| 脂肪干细胞 | 对七名患有复发性溃疡和缺血性肢体损伤的参与者进行的I期试验 | ADSC通过减轻腿部疼痛和溃疡大小来改善伤口愈合 | Bura等人2014年 |
| 脂肪干细胞 | 使用由ADSC和成体脱细胞胶原基质制成的生物绷带治疗慢性伤口 | 敷料大大增加皮肤血管再生和伤口重塑 | Lafosse等人2015年 |
| 脐血干细胞 | 一项治疗糖尿病足部溃疡的随机对照临床试验 | UMSCs植入后三个月,溃疡完全恢复或正在恢复 | 秦等人2016年 |
| 胎盘间充质干细胞 | 含胎盘MSCs的海藻酸钠凝胶局部应用于溃疡性糖尿病足 | 三周后溃疡基本愈合 | 曾等人2017年 |
| 脂肪干细胞 | 基于水凝胶的同种异体脂肪干细胞片治疗糖尿病足 | ADSC组的伤口完全愈合率更高 | Moon等人2019年 |
| 脐血干细胞 | 含血清的人类UMSC培养基对激光治疗恢复的影响 | 减少红斑治疗和激光消融治疗后的恢复时间 | Jihee Kim 等人2020年 |
| 脂肪干细胞 | ADSC加速皮肤伤口愈合的能力 | ADSC促进伤口愈合 | 周等人2022年 |
| 间充质干细胞 | 利用纤维蛋白聚合物喷雾将培养的自体MSCs应用于伤口 | 促进慢性、不愈合下肢伤口的愈合 | Falanga等人,2007年 |
| 间充质干细胞 | 将MSCs与基质或水凝胶一起注入伤口 | 加速愈合并显著改善临床结果 | Dash 等人2009年 |
间充质干细胞促进皮肤年轻化的作用及可能机制
通过增加成纤维细胞生长和生物活性、降低炎症和ROS、促进胶原蛋白生成和降低MMP表达,MSC也在老化皮肤治疗中表现出良好的效果。ADSC可以单独使用或与基质血管部分结合使用,以修复皮肤缺损,如面部疤痕、抗氧化剂、皱纹和黑色素合成,从而使皮肤美白。
根据Hu等人的研究,核受体相互作用蛋白1 (Nrip1) 在衰老中起着重要作用。用ADSC治疗后,皮肤老化减缓,炎症相关基因(IL-6、p65和IL-1α)、衰老相关基因(p21和p53)和生长因子相关基因(Igf1、mTOR)的表达降低(Nrip1敲低后)。ADSC与CO2激光表面修复和培养成纤维细胞等其他方法相结合时,表现出抗衰老和皮肤再生的特性。
Liang等人使用ADSC-exo处理发表的PCR数据表明I型胶原蛋白mRNA表达增强,MMP-1、MMP-3和III型胶原蛋白表达降低。同时,TGF-β1和TIMP-1表达上调,导致光损伤的真皮成纤维细胞修复(图7)。
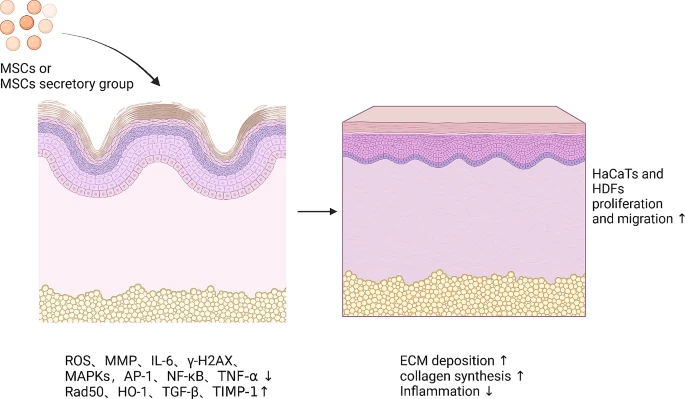
在老化皮肤中,MSCs刺激Rad50、HO-1、TGF-β和TIMP-1的释放,降低ROS水平,抑制炎症反应,抑制MMP、IL-6、γ-H2AX、MAPKs、AP-1、NF-κB和TNF-α的表达,促进HaCaTs和HDFs的分化和迁移,进而刺激胶原蛋白和ECM的合成,从而导致皮肤年轻化
脂质体、囊泡、固体脂质纳米颗粒和金属纳米颗粒是化妆品中最常用的纳米载体。活性成分通常包装在纳米载体中以促进皮肤吸收并达到更好的美容和治疗效果。纳米材料因其出色的封装能力、封装的生物活性成分更稳定以及可控释放而被用于防晒霜。
未来的研究可以考虑多种纳米材料和MSCs的联合疗法,以实现更高的抗衰老效果。
表2列出了最近使用MSCs疗法促进皮肤恢复活力的临床研究。预计未来将开展更多相关研究。
| 来源 | 研究内容 | 发现 | 参考 |
|---|---|---|---|
| 羊膜间充质干细胞 | 羊膜MSC-CM对光老化的影响 | 治疗后光老化明显改善 | Prakoeswa 等人,2019 年 |
| 羊水中的间充质干细胞 | 使用干细胞培养基与针灸相结合进行面部年轻化 | 改善皮肤纹理,促进胶原蛋白和弹性蛋白的产生,并帮助调节面部衰老 | El-Domyati,M.等人2020年] |
| 脂肪干细胞 | 使用ADSC进行日光性弹性变性患者的ECM再生 | 获得日光性弹性变性的完全恢复 | LuizCharles-de-Sá 等人2020年 |
| 脂肪干细胞 | 研究通过微针将ADSC培养基中的蛋白分离物应用于亚洲皮肤的效果 | 呈现嫩肤美白功效 | 王等人,2018年 |
| 马鹿脐带膜 MSCs | 比较红鹿MSCs提取物与面部嫩肤载体的功效 | 对老化面部有有效的修复作用 | Marwan Alhaddad 等人,2019 年 |
| 脂肪干细胞 | 分析烟酰胺与ADSC-CM 联合用于激光局部治疗后的效果 | 有效的抗衰老作用 | Lee等人,2020年 |
| 脂肪干细胞 | 纳米方法植入含有干细胞的脂肪组织用于患者皮肤治疗 | 皮肤质量更好,斑点和色素沉着减少 | Omeed Memar 等人2014年 |
| 间充质干细胞 | 由 MSC-CM 制成的生物活性物质可消除黑眼圈 | 减少黑眼圈,改善眼部整体外观 | Samatha Bhat 等人2022年 |
结论
皮肤医学美容最近受到越来越多的关注,特别是在皮肤更新和无疤痕皮肤伤口愈合方面。间充质干细胞疗法通过旁分泌作用、免疫调节、炎症管理和组织分化,在促进皮肤修复和再生方面表现出了巨大的潜力。
间充质干细胞的旁分泌影响是最重要的,它通过VEGF、bFGF和PDGF等细胞因子和外泌体等细胞外囊泡控制细胞间接触,其中外泌体的研究最为广泛。新提出的干细胞裂解物也显示出良好的治疗效果,有助于对抗皮肤光老化和改善皮肤状况。
综上所述,间充质干细胞疗法在皮肤科和美容医学领域有着非常广泛的应用前景,未来需要更多的机制研究和大规模的临床研究来制定间充质干细胞疗法的生产或应用指南。为了提高间充质干细胞的治愈能力,剂量、持续时间、频率和治疗方式都应仔细考虑,而这些尚未标准化。
因此,在间充质干细胞治疗进入临床使用之前,应该制定标准化的临床指南,以确保安全性和有效性,以便间充质干细胞在美容皮肤科中发挥最大作用,同时对人体无害。
参考资料:Li, J., Liu, Y., Zhang, R. et al. Insights into the role of mesenchymal stem cells in cutaneous medical aesthetics: from basics to clinics. Stem Cell Res Ther 15, 169 (2024). https://doi.org/10.1186/s13287-024-03774-5
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请及时跟本公众号联系,我们将在第一时间处理。




 官方微信公众号
官方微信公众号