细胞疗法对中风后脑修复大有裨益。虽然越来越多的证据证实了细胞疗法的临床前和临床益处,但它们促进脑修复的潜在机制仍不清楚。
近日,牛津学术子刊《Brain》发表了一篇“干细胞治疗中风后的脑修复机制”的文章,在这里,简要回顾了缺血性中风后脑修复的内源性机制,然后重点介绍不同的干细胞和祖细胞来源如何促进脑修复。

中风简介:中风仍然是导致残疾和死亡的主要原因,25岁以上的人群中每4人中就有1人患有中风。大约87%的中风是缺血性中风,即供应大脑的血管被阻塞。超过一半的中风幸存者会出现不同程度的损伤,影响他们的躯体感觉功能、运动、言语和/或认知功能,因此存在未得到满足的医疗需求。因此,开发超越传统治疗范围的新型再生疗法至关重要。
确认干细胞治疗中风后的大脑修复机制,以推动干细胞治疗中风进入临床至关重要!
01临床批准的中风治疗的现状
美国食品药品管理局 (FDA) 批准的唯一中风治疗方法是重新建立闭塞血管的灌注,以恢复正常的脑血流水平。要实现再通,有两种不同的策略:
(i) 通过血管内血栓切除术进行机械血凝块取回;
(ii) 使用组织型纤溶酶原激活剂 (t-PA) 进行药物血栓溶解。尽管这些方法在临床试验中取得了巨大成功,但由于中风发作后4.5小时的治疗窗口很窄,只有一小部分中风患者从中受益。这使得相当一部分未经治疗的中风患者无法接受促进修复和康复的药物治疗。
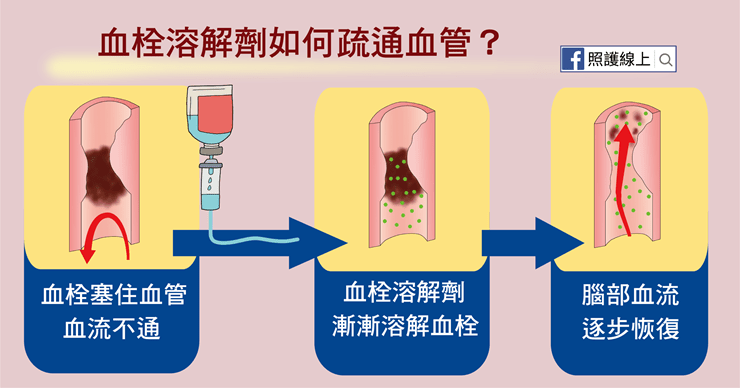
在慢性期,中风治疗涉及长期神经康复,以防止进一步出现并发症,例如肢体逐渐僵硬,并刺激神经可塑性。尽管中风患者护理取得了进展,但康复仍不足以诱导完全的功能恢复。迄今为止,尚无临床试验成功缓解中风幸存者的神经损伤。
如今,开发促进中风后脑修复和功能恢复的新疗法至关重要。在目前正在开发的所有治疗策略中,细胞疗法在临床前模型中显示出增强脑修复的前景。移植细胞的关键优势在于它们能够激活中风后的多种内源性修复过程。干细胞疗法对治疗中枢神经系统多种疾病(包括中风)有着巨大的前景。
本文总结了干细胞疗法在缺血性中风后长期治疗方面的最新进展,以及我们目前对脑修复机制的理解,通过这些机制,细胞移植可以增强中风后的脑再生和功能恢复。本综述的总体重点是评估基于细胞的疗法在中风康复方面的治疗潜力,并为未来的研究方向提供建议。
02中风后的病理生理学和大脑修复
缺血性脑卒中是指脑动脉血流中断。发生大血管闭塞的患者平均失去1.2亿个神经元、8300亿个突触和714千米的髓鞘纤维,大脑每小时衰老3.6年。除神经损伤外,中风还会引起局部和全身的大规模炎症反应以及BBB成分的严重损坏。随后是神经可塑性阶段,该阶段会激活内源性修复和组织重塑机制,试图使受损组织再生并恢复丧失的功能。
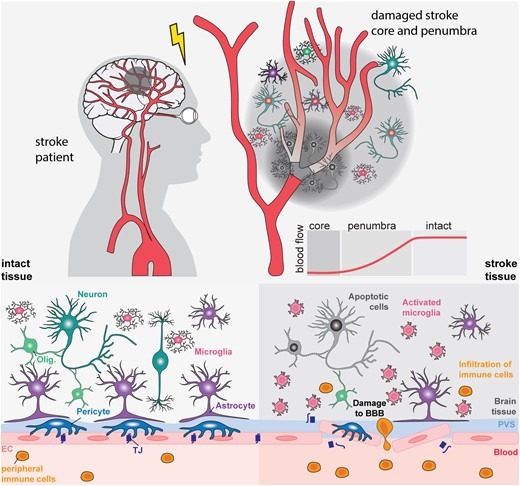
中风的病理生理学:缺血性中风通常发生在脑动脉阻塞时,导致受影响脑区的氧气和营养物质减少。这些区域可分为:中风核心区,脑血流量严重减少且细胞坏死不可逆(<10ml/100g/min);半暗影区,损伤可逆(17-10ml/100g/min);正常完整组织(>17ml/100g/min)。中风组织损伤包括细胞坏死和凋亡、血脑屏障损伤、驻留小胶质细胞激活和外周免疫细胞浸润。
中风后的内源性恢复
中风后的神经可塑性也称为神经可塑性,可定义为大脑在受伤后重新连接和重组其神经回路的能力,以试图适应与组织和功能丧失相关的结构、代谢和细胞变化。可塑性包括现有神经元、轴突、突触和神经元连接的新生和改变,在中风后持续数月,主要发生在梗死周围区域。
在这一阶段,转录特征表明,在中风的实验性啮齿动物模型中,涉及轴突生长、血管发育、树突萌发、突触形成、粘附分子和细胞骨架重排的基因和信号通路上调。
中风后的神经可塑性
研究表明,新神经元的形成,即神经发生,也可能有助于中风后的神经可塑性和修复。早期的实验数据表明,脑室下区的NPCs可以增殖、向病变部位迁移并分化为成熟的神经元。
此外,实验性中风可激活缺血区内和周围的NPCs,其范围超出室下区和齿状回等传统神经源区。大量证据表明,实验性神经发生的增强与康复的改善有关,而抑制神经发生则与康复受损有关。
其他各种细胞类型,包括免疫细胞和血管细胞,在损伤后刺激神经发生和可塑性方面发挥着重要作用。实验研究表明,血管内皮细胞能够释放生长因子,刺激梗死周围区域的血管生长和重塑,这反过来又促进了NSC的增殖和向病变部位的迁移,同时引导它们浸润梗死周围区域以刺激神经元的可塑性。反过来,NPC通过分泌血管内皮生长因子增加血管生成,表明血管和神经元重塑之间存在双向关系。
其他对可塑性重要的细胞类型是周细胞和神经胶质细胞。例如,作为神经血管单元的一部分,周细胞已被证明可调节中风后的血管生成、CBF和BBB修复,而它们的缺失会导致神经血管解偶联。
星形胶质细胞不仅具有消除神经递质和其他与兴奋性毒性相关的分子的能力,而且在神经血管耦合和通过促进新的功能性突触的形成来增强突触形成方面也发挥着重要作用。少突胶质细胞祖细胞分化为成熟的少突胶质细胞,促进轴突髓鞘再生并改善白质完整性,而小胶质细胞已被证明可以减少炎症并释放营养因子(如BDNF),从而促进突触形成。
血管形成和血脑屏障的修复
在中风后的亚急性阶段,血管系统和BBB的相关成分以及血管周围ECM在肢体周围发生广泛的重塑。在这一被称为中风后血管生成的现象中,新血管形成,周细胞被招募到血管壁,紧密连接重新建立,从而部分恢复了BBB的完整性。越来越多的证据表明,脑卒中后血管生成的效率与年龄有关,因为患者和啮齿动物随着年龄的增长,脑血管的EC增殖和重塑会减弱。
动物研究表明,卒中后所有主要血管生成相关信号因子转录上调,如Vegfa、Vegfr2、Tie2、Angpt2、Pdgf、Cxcl1和Pecam1。VEGF的分泌及其受体VEGFR2的激活是中风后血管生成所必需的。研究表明,病变周围血管生长增加与实验和人类中风的功能恢复有关。
脑动脉和毛细血管由平滑肌细胞和周细胞支撑,它们通过与EC的细胞串扰在BBB通透性和完整性中发挥重要作用。在卒中后血管生成过程中,EC分泌的PDGFB与周细胞表面的受体PDGFRB结合,而周细胞分泌的Angpt1与EC表面的受体Tie2结合。研究表明,病变周围血管壁的周细胞覆盖率增强可改善BBB完整性,有助于组织修复和功能恢复。
03从临床试验中发现:中风临床细胞疗法的疗效与挑战
细胞疗法已成为一种有前途的中风治疗策略,并在二十年前进入临床试验。最初,永生化神经细胞系、胎儿细胞来源和成人MSCs被用作细胞来源(图2)。
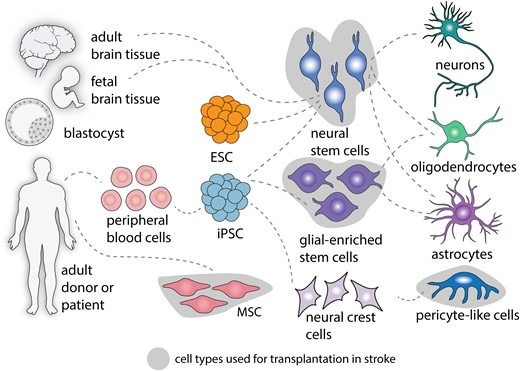
细胞移植可来自胚胎/胎儿阶段或成年人。成体干细胞包括间充质干细胞 (MSC) 或来自外周血的分化细胞,这些细胞被重新编程以产生诱导性多能干细胞 (iPSC)。胚胎干细胞 (ESC) 和iPSC均可分化为神经或富含神经胶质细胞的干细胞,以产生神经元、少突胶质细胞或星形胶质细胞。周细胞样细胞可通过神经嵴细胞中间体从iPSC产生。
中风的细胞疗法通常被认为是安全的,大量来自临床前和更大规模的2期和3期临床试验的证据报告称,只有零星的不良事件,而且通常具有良好的安全性(表1)。关于中风细胞疗法的临床疗效和安全性的综合评论和荟萃分析已在其他地方讨论过。
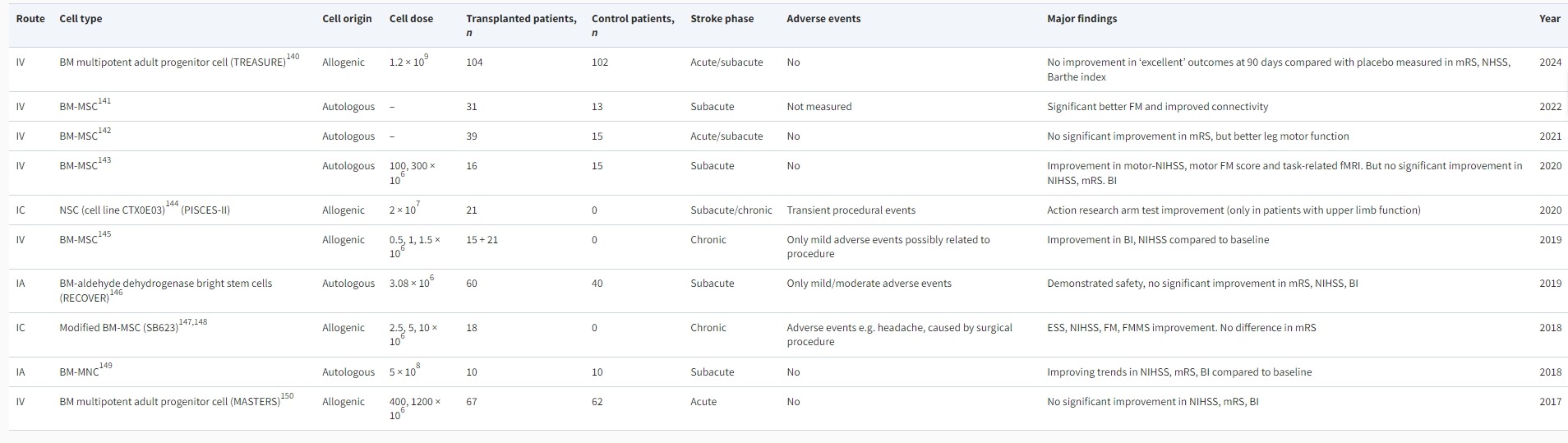
在过去5年中,有限数量的小型研究表明,与中风后急性/亚急性和慢性期的对照组中风患者相比,通过静脉或动脉内施用MSCs可显著改善国立卫生研究院中风量表 (NHSS)、改良Rankin量表 (mRS) 和/或Barthel指数 (BI)。
一项更广泛的3期随机对照试验STARTING-2仅部分证实了MSCs的疗效,该试验招募了60名中风患者。通过神经影像学评估,静脉内应用MSCs可减少皮质脊髓束变性并增强神经网络连接,同时根据Fugl-Meyer评估改善下肢运动功能。然而,STARTING-2的主要结果(以90天后的mRS测量)显示,两组之间没有显著差异。
除了MSCs,基因改造的神经干细胞系CTX0E03也已通过PISCES系列试验在慢性卒中患者身上进行了测试。PISCES-I和PISCES-II均涉及通过立体定向注射向慢性卒中患者施用CTX0E03细胞。
规模更大的PISCES-II试验是一项2a期多中心试验,向23名患者施用了2000万个细胞,结果患者上肢功能在3、6和12个月的间隔内得到改善。

到目前为止,临床试验的结果好坏参半。这表明,更全面地了解潜在机制可以改进细胞疗法的各个方面。
中风细胞疗法有两种普遍有益的机制。
- 第一种机制是直接细胞置换,使移植细胞分化为成熟的神经元或神经胶质细胞,并在功能上整合到受损宿主的脑回路中。根据细胞来源,移植物归巢可以直接有助于恢复受损区域的脑功能、BBB完整性或CBF。
- 其次,移植细胞可能通过间接方式做出贡献,例如通过支持性释放促再生因子来增强或延长内源性再生程序,最终导致康复改善。
04干细胞治疗中风的机制见解
中风后细胞替代:替代受损的神经细胞干细胞具有自我更新和多向分化的潜能,可以分化为神经元、星形胶质细胞和少突胶质细胞等神经细胞,从而替代受损或死亡的神经细胞,重建神经回路,恢复神经功能。
细胞疗法的间接有益作用:尽管细胞整合到宿主组织中是可能的,但大多数针对中风的细胞移植研究发现,对修复和恢复的有益作用是通过间接机制刺激的,包括免疫调节、刺激血管和神经生长的促再生因子的释放以及梗塞周围组织的ECM重塑,所有这些都激活了大脑的内源性修复机制,促进中风后的修复和恢复(图3)。
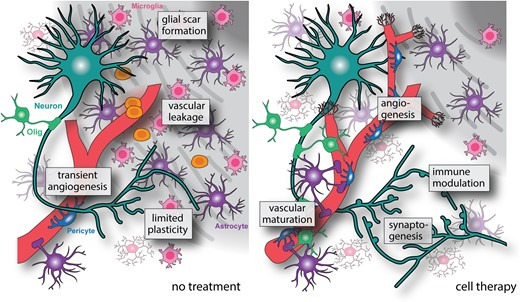
细胞疗法的间接作用包括通过在梗塞周围区域释放促血管生成因子来改善血管修复和成熟。免疫调节和增强的抗炎特征可减少继发性损伤并减少神经胶质疤痕形成。细胞移植释放的神经营养因子也会增加受损区域的轴突形成和突触形成。
免疫调节:中风后,脑部会发生炎症反应,导致神经细胞的进一步损伤。干细胞具有免疫调节作用,可以抑制炎症细胞的活化和浸润,减轻炎症反应,保护神经细胞。
血管修复和重塑:近年来,来自临床前和人体研究的大量证据表明,中风后血管生成在激活内源性修复机制和损伤后功能恢复中起着重要作用,而血管生成抑制与修复和恢复的延迟或恶化有系统性联系。
一旦被输送到受伤的大脑中,移植的干细胞(包括MSCs和NSCs )就会产生促血管生成因子,如VEGF、ANG1、FGF2、PDGFA和HIF-1a,导致梗死周围组织的血管密度增加和血管生成受体的表达。
神经胶质细胞和神经胶质疤痕形成:胶质瘢痕形成损伤部位轴突浸润的主要物理屏障,并限制再生过程。胶质瘢痕形成减少与卒中恢复改善和卒中后细胞治疗的有益效果相关。
神经胶质细胞可进一步促进少突胶质细胞祖细胞 (OPC) 增殖和分化为髓鞘少突胶质细胞。一种潜在机制是通过星形胶质细胞释放TIMP-1并调节周围的ECM。在皮层下白质卒中模型中,移植的神经胶质祖细胞促进了内源性OPC增殖和轴突发芽,从而改善了运动和认知恢复。
神经修复:细胞治疗后,神经回路可通过多种机制间接修复。移植的MSC和NSC已被证实可诱导内源性神经发生和神经胶质生成。
移植干细胞与中风脑组织之间的分子串扰:转录组学技术的进步现在使我们能够识别移植细胞与中风损伤宿主组织之间的分子相互作用。最近的一项研究表明,移植iPSC衍生的NSC 可促进脑缺血后的长期功能恢复。
05结论
细胞疗法仍然是一种很有前途的中风再生策略。细胞移植的多模态效应具有改善中风患者长期康复的巨大潜力。尽管具有这种潜力,但现有临床试验的不同结果凸显了更全面的机制理解的重要性。
其他临床前研究表明,细胞移植的基因工程可以改善当前的临床挑战,例如免疫相容性、移植物输送和细胞疗法的安全性。对潜在治疗机制的不断了解也将有助于确定理想的细胞来源并为中风患者量身定制治疗方案。
未来的临床试验可能会实施这些最近的临床前进展,并研究它们是否产生更一致的有益效果,为未来将基于细胞的疗法整合到标准中风治疗中铺平道路。
参考文献:Ruslan Rust, Lina R Nih, Luca Liberale, Hao Yin, Mohamad El Amki, Lin Kooi Ong, Berislav V Zlokovic, Brain repair mechanisms after cell therapy for stroke, Brain, Volume 147, Issue 10, October 2024, Pages 3286–3305, https://doi.org/10.1093/brain/awae204
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号