1型糖尿病 (T1DM) 是一种高度流行的自身免疫性疾病,会导致胰岛β细胞遭到破坏。由此产生的胰岛素产生不足导致终生需要胰岛素替代疗法、全身并发症以及生活质量和预期下降。细胞疗法已被广泛尝试恢复胰岛素非依赖性 (IID),自体造血干细胞移植 (AHST) 似乎给出了最有希望的结果,但在整个研究中实现IID的患者数量差异很大。
近期,意大利米兰大学在《Cells》期刊中发表了一篇《造血干细胞/祖细胞治疗1型糖尿病:是否有理想的候选者》的论文,在这份论文中,意大利米兰大学将回顾迄今为止在使用造血干/祖细胞 (HSPC) 疗法治疗T1DM方面所做的尝试。根据过去二十年设计的试验收集的经验,我们还将讨论量身定制治疗的最佳患者候选人。

意大利米兰大学研究人员对涉及干细胞的试验进行了全面审查,尤其是造血干细胞移植用于治疗T1DM。然后,意大利米兰大学汇集了参加不同试验的患者,并寻找可能与实现IID相关的患者特征。意大利米兰大学发现老年患者实现IID的概率明显更高(OR1.17,95%CI 1.06–1.33,p=0.002),并且在有酮症酸中毒病史的患者中概率显着降低(OR 0.23,95%CI 0.06–0.78,p=0.023)。这表明1型糖尿病患者更有可能从造血干细胞移植中受益,但需要进一步的数据来描述理想候选人的概况。
用于细胞治疗的造血干/祖细胞
HSPC是自我更新的多能细胞,位于骨髓内的特殊壁龛中。由CD34表面抗原鉴定,其功能尚不清楚,它们能够在所有类型的血细胞中分化,包括骨髓和淋巴谱系,并在骨髓消融后重建整个造血系统。
目前,迄今为止报道的大多数临床前和临床研究都是鉴于HSPC的假定心血管保护和促血管生成作用而进行的,而忽略了这些细胞是免疫系统细胞的前体并具有免疫调节功能。一致地,同种异体骨髓HSPC移植非肥胖糖尿病 (NOD) 小鼠已被证明可以预防糖尿病发作并恢复1型糖尿病小鼠的胰岛素非依赖性 (IID),尽管不能再生丢失的胰岛。这些证据,加上来自同一同种异体供体的移植胰岛可以被先前移植了骨髓并暂时恢复IID的糖尿病患者所接受,提示HSPC的主要作用机制在于其免疫调节特性,而不仅仅是再生作用。
除了HSPCs,其他细胞类型已经在治疗T1DM的试验中进行了测试。其中包括未经选择的骨髓来源的单核细胞 (BM-MNC) 部分和间充质干细胞 (MSC)。前者由不同种类的细胞组成,通常通过从髂嵴抽取骨髓获得,其中CD34+细胞占约0.5-6%的比例,最有可能对治疗效果负责。另一方面,MSC是多能细胞,可以分化成多种细胞类型,例如成骨细胞、成软骨细胞、肌细胞、脂肪细胞和β细胞样细胞;可以从各种组织中采集,包括骨髓、脂肪和脐带血;并具有免疫调节特性和保护胰岛并促进其再生的潜力。
最后一种细胞类型,即胚胎干细胞 (ESC),正在一些临床试验中进行评估(NCT02239354、NCT04678557、NCT03163511、NCT05210530、NCT04786262)。与其他细胞类型不同,这些细胞经过操作以获得胰腺内胚层细胞,这些细胞可以直接施用于患者以恢复胰岛素的产生。此外,对免疫缺陷小鼠的研究表明,它们能够正确分化为干细胞衍生的β样细胞,并在移植后变得对胰岛素敏感。
迄今为止,在所有细胞类型中,HSPC在治疗T1DM方面取得了最大的有希望的结果。因此,涉及这些细胞的试验(总结在表1中)将是我们的重点。
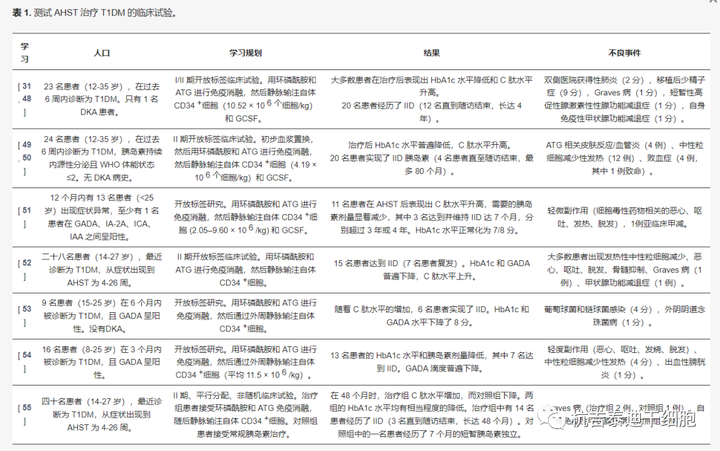
各国造血干/祖细胞在移植治疗1型糖尿病的临床试验
HSPCs治疗T1DM的有效性已在多项采用造血干细胞移植方法的临床试验中得到评估。由于T1DM是一种自身免疫性疾病,其特征是对胰岛β细胞产生自身反应,从而导致胰岛素生成受损,因此研究人员旨在验证造血干细胞移植是否可以在特定环境下中断或至少减缓免疫系统对β细胞的破坏新发/早期T1DM,在独立于胰岛素给药或减少剂量方面具有益处。这种方法有可能被证明是一种比胰岛移植更有效、风险更低、成本更低且终生无免疫抑制的治疗替代方法。
巴西研究
第一项研究由Voltarelli等人进行。在巴西 (NCT00315133)。他们招募了15名患者,包括在2003年11月至2006年7月的前6周内诊断出患有T1DM的黑人、白人和混血儿,并进行了7至36个月的随访。
该研究给出了非常有希望的结果:13名患者持续发生IID,1名患者在ASHT后1年恢复胰岛素治疗。此外,移植前C肽水平的平均曲线下面积 (AUC)在6个月、12和24个月时显示出统计学上显着的增加;抗谷氨酸脱羧酶抗体 (GADA) 水平在6个月后显着降低;在研究开始时,14名患者中有11名糖化血红蛋白 (HbA1c) 值超过7%,但在3个月内观察到持续下降,除了一名最终复发的患者。
该研究首次提供了T1DM患者在接受AHST治疗后IID(胰岛素非依赖性)持续恢复的临床证据。两年后,同一组发表了延长随访的结果,增加了8名新患者,总计23。随访7-58个月后,12例为持续性IID,8例为短暂性IID,其中4例在上呼吸道感染后恢复胰岛素。
总之,Voltarelli等人证实造血干细胞移植能够逆转人类的1型糖尿病,至少长达4年,并且具有可接受的不良反应负担。
中国研究
两项不同的中国临床试验已正式注册(NCT01341899和NCT00807651),涉及在上海和南京招募的患者;然而,作者发表了多篇论文,介绍了有时基线特征非常相似的不同患者群体的结果。因此,很难对他们的总体发现进行清晰的评估。
2014 年,D’Addio等人。对Snarsky等人、Li等人进行的试验结果进行了汇总分析。(共65名患者)。总体而言,59%的患者在治疗后的前6个月内完成了IID,而只有32%的患者在随访结束时仍处于IID。HbA1c和C肽水平与CD34+细胞数量无显着相关性;多变量分析对性别、年龄和基线HbA1c和C肽水平呈阴性。然而,作者发现较早治疗的患者(在T1DM发病后6周内)实现IID的可能性是后者的两倍(82%对40%)。
2017年,顾等人发表了一项II期非随机试验的结果,该试验涉及20名接受造血干细胞移植治疗的患者(4名患者撤回同意,1名失访)和20名定期接受胰岛素注射治疗的患者(4名失访) ,病程少于6个月。AHST分支中的14名患者成为IID,其中3名一直到随访结束(48个月),而胰岛素治疗分支中只有一名患者成为短暂的IID,然后复发。不良事件发生率与其他研究一致。
此外,2020年,郑州市第一人民医院分析在1型糖尿病患者治疗过程中采用自体造血干细胞进行移植治疗所取得的临床效果。
方法:在2019年1月至2020年2月期间于郑州市第一人民医院进行治疗的1型糖尿病患者中选取110例作为研究对象,将其分为两组进行治疗(各55例),其中,对照组采用胰岛素进行常规治疗,观察组采用自体造血干细胞进行移植治疗,对两组患者的治疗效果进行比较。
结果:在血糖控制问题上,观察组血糖波动平均幅度(MAGE)、最大血糖波动幅度(LAGE)、平均血糖值(MBG)以及血糖标准差(SDBG)的数值均低于对照组;在胰岛素用量方面,经过治疗后,观察组药物用量低于对照组,组间比较,差异具有统计学意义(P<0.05)。
结论:在1型糖尿病患者治疗过程中,通过自体造血干细胞移植治疗的开展,有利于实现患者治疗效果的提升与优化,对于患者治疗质量的进一步提升具有一定作用。
波兰研究
随后的研究由Snarsky等人进行。在波兰,最初是在一个由8名患者组成的小队列中进行的。所有患者在造血干细胞移植治疗后均成为IID,只有1例患者后来恢复了胰岛素治疗;六名患者额外服用阿卡波糖以改善血糖控制。AHST后,HbA1c平均水平显着下降,而C肽水平上升。没有重大并发症和一些轻微的不良反应。
墨西哥研究
由于众所周知的与免疫消融相关的潜在不良反应,Cantú-Rodríguez 等人设计了一个简化的AHST协议,考虑使用氟达拉滨代替抗胸腺细胞球蛋白和较低剂量的环磷酰胺进行调理。值得注意的是,纳入的受试者(16名患者诊断为T1DM不到3个月)在门诊进行:目的是降低毒性、限制手术成本并降低院内感染的风险。
没有记录到严重的不良事件,但52%的患者出现了副作用:最常见的包括恶心、呕吐、发烧和脱发;4名患者出现中性粒细胞减少性发热,但无需住院治疗,均接受口服阿莫西林治疗;一名患者经历了出血性膀胱炎,在不到36小时的时间内通过强烈补液得到解决。结果与其他研究相当,7名患者 (44%) 实现并维持完全IID,6名 (37%) 患者仅实现部分IID。
接受治疗者患者概况
我们的最终人群为90名患者;由于样本数量少,我们只选择了适用于所有人群的变量(性别、年龄、体重指数、DKA病史和从诊断到治疗的时间)。由于某些研究中缺乏准确信息,从诊断到治疗的时间转换为二项式变量(≤/>12周)。患者的特征见表2。
表2:参加选择进行统计分析的临床试验的患者特征。
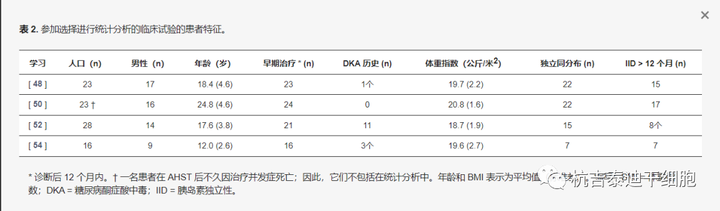
我们进行了单变量分析,然后构建了一个多变量模型,其中包含我们在分析过程中发现的重要特征(图1)。
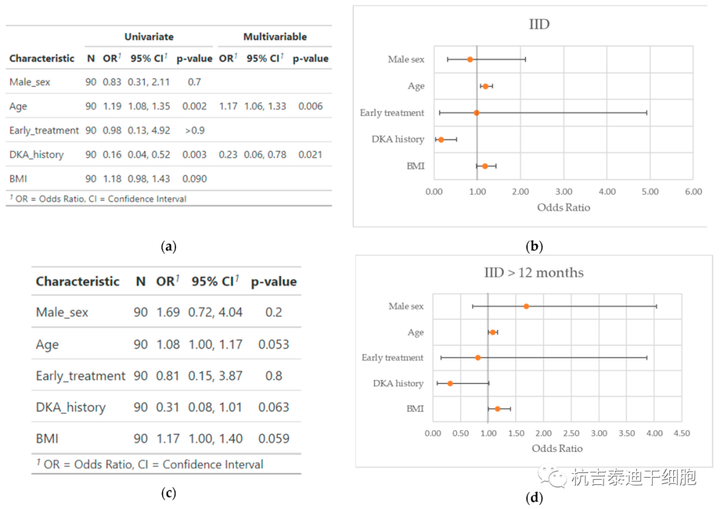
图1:优势比、95%置信区间和患者特征对实现胰岛素独立性 (a) 和维持超过12个月 (c) 的统计显着性;各自的森林地块(b,d)。森林图代表单变量分析的结果。
因此,我们发现老年患者实现IID的概率显着更高(OR 1.17,95%CI 1.06–1.33,p=0.006),而有DKA病史的患者实现IID的概率显着降低(OR 0.23,95%CI 0.06–0.78,p=0.021)。
结论
综上所述,1型糖尿病的细胞疗法在近年来取得了诸多突破性进展和鼓舞人心的成果,为未来T1DM个体化阶段化精准治疗提供了新思路。
胰岛移植目前仅针对少数T1DM患者有绝对适应证,而造血干细胞移植治疗技术仍处于临床研究阶段,细胞疗法尚不能作为常规临床实践广泛开展。
随着造血干细胞移植相关技术不断优化,治疗安全性与疗效逐步提高,临床循证依据不断累积,干细胞将有望更广泛地应用于T1DM的临床治疗,为广大患者带来福音。
参考资料:
[1]:Carulli, E.; Pompilio, G.; Vinci, M.C. Human Hematopoietic Stem/Progenitor Cells in Type One Diabetes Mellitus Treatment: Is There an Ideal Candidate? Cells 2023, 12, 1054. https://doi.org/10.3390/cells12071054
[2]:刘爽,宋丹.自体造血干细胞移植治疗1型糖尿病的临床研究[J].深圳中西医结合杂志,2020,30(14):7-8.DOI:10.16458/j.cnki.1007-0893.2020.14.003.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞不保证信息的准确性和完整性。所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号