简介:糖尿病 (DM) 是导致高血糖水平的一组代谢性疾病,在当今世界很普遍。糖尿病的全球成本及其后果正在上升,预计到2030年将大幅增加,尤其是在中等收入和低收入国家。以证据为基础的疗法,特别是针对降低高血糖水平和最大限度地减少糖尿病并发症,是目前的治疗选择。干细胞疗法为治疗糖尿病提供了一个有前途的愿景。尽管这种疗法仍然面临挑战,但研究已经产生了与胰岛素分泌细胞非常相似的再生 β细胞。自细胞治疗概念验证确定以来,已经探索了许多干细胞来源。

介绍
DM有两种类型1型和2型。
1型糖尿病,也称为胰岛素依赖型糖尿病和青少年糖尿病,涉及免疫系统,这是由细胞介导的自身免疫性胰腺BETA细胞破坏引起的. 它可以发生在任何年龄,但最常见于儿童和年轻人。1型DM的病因尚未完全揭示,但在大多数情况下,身体的免疫系统会攻击并破坏产生胰岛素的β细胞。已知家族史在约10%至15%的1型DM患者中发挥作用。
2型糖尿病,也称为成人发病型DM,通常在40岁以后发病,但在肥胖患者中可能更早出现。对于2型 DM,胰腺会产生胰岛素,但身体无法有效利用它。胰岛素治疗并不总是必要的,在这些患者中,与1型DM一样。糖尿病与严重的长期微血管和大血管并发症有关,并且具有很高的发病率和死亡率。1型和2型DM都是一个重大的公共卫生问题,具有许多使人衰弱的并发症。糖尿病的全球成本及其后果正在上升,预计到2030年将大幅增加,尤其是在中低收入国家。以证据为基础的疗法,特别是针对降低高血糖水平和最大限度地减少糖尿病并发症,是目前的治疗选择。
DM(无论是1型还是2型)的发病机制都可以追溯到胰腺β细胞的功能障碍。尽管存在增强β细胞功能的批准疗法,但没有一种疗法可以导致丢失或功能失调的β细胞再生。研究表明,β细胞可以用某些分子重新编程,例如GABA和激素。然而,这些研究也揭示了许多需要探索的不确定性。用于治疗DM的干细胞来自多种生物来源,如胚胎、胎盘和骨髓。祖细胞是另一个令人兴奋的研究途径。像干细胞一样,这些细胞可以呈现出许多不同类型的成熟人类细胞的形式,但是,与干细胞不同的是,它们不能无限分裂。
祖干细胞已被用于在实验室条件下从肠细胞和未发育的胰腺细胞中培养产生胰岛素的细胞。本文概述了用于糖尿病患者胰腺再生的各种方法、包括我们的贡献在内的最新进展以及未来可能探索的新方法。
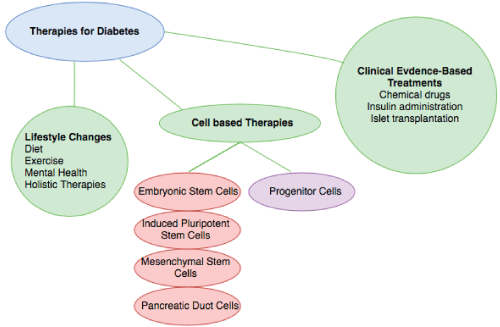
祖细胞与干细胞非常相似。它们是生物细胞,并且像干细胞一样,它们也具有分化成特定类型细胞的能力。然而,它们已经比干细胞更具特异性,只能被推动分化成它的“目标”细胞。然而,干细胞具有分化成许多不同类型细胞的能力,如图1所示。表 1 详细突出显示了干细胞和祖细胞之间的比较。

| 比较中 | 干细胞 | 祖细胞 |
| 描述 | 干细胞是储备细胞,能够变成许多不同类型的细胞并无限生长。它们有可能创造出许多新的不同细胞,这些细胞可以帮助替换垂死和/或受损的细胞。干细胞也有可能从几个干细胞中产生新的组织甚至整个器官。 | 祖细胞与干细胞非常相似。它们是生物细胞,并且像干细胞一样,它们也具有分化成特定类型细胞的能力。然而,它们已经比干细胞更具特异性,只能被推动分化成它的“目标”细胞。 |
| 类型 | 干细胞的四种主要类型: 1) 成体或成体干细胞 2) 胎儿干细胞 3) 胚胎干细胞 4) 诱导干细胞 | 许多,因为每个“目标”细胞都有自己的祖细胞。其中一些类型包括: 1) 肌肉中发现的卫星细胞。 2) 在脑室下区形成的中间祖细胞。 3) 骨髓基质细胞 4) 骨膜含有发育成成骨细胞和成软骨细胞的祖细胞。 5) 胰腺祖细胞 6) 成血管细胞或内皮祖细胞 (EPC) 7) 原始细胞 |
| 特征 | 1) 通过细胞分裂倍增以补充垂死的细胞并再生受损的组织。2) 生成它们起源的器官的所有细胞类型。3) 有可能从几个细胞中再生出整个器官。 | 1) 倾向于分化成特定类型的细胞,但已经比干细胞更特异,并被推动分化成其“目标”细胞。 2) 只能划分有限的次数。 |
| 好处 | 它们有可能促进愈合,并有可能从几个细胞中再生出整个器官。他们被调查在未来在一下疾病具有临床应用价值: 1) 糖尿病 2) 类风湿性关节炎 3)帕金森病 4)老年痴呆症 5) 骨关节炎 6)中风及脑外伤修复 7)身体缺陷 8) 脊髓损伤修复 9) 心脏梗塞 10) 抗癌 11) 秃头 12) 更换缺失的牙齿 13)修复听力 14) 恢复视力 15) 肌萎缩侧索硬化症 16) 克罗恩病 17) 伤口愈合 | 它们充当身体的修复系统。它们补充特殊细胞,还维持血液、皮肤和肠道组织。在组织损伤、损坏或死亡细胞的情况下,可以激活祖细胞。它导致组织的恢复。 |
| 争议 | 在研究和治疗中使用人类成体干细胞不被认为是有争议的。在研究和治疗中使用人类胚胎干细胞是有争议的,因为它们来源于指定用于科学研究的IVF(体外受精)诊所产生的5天大的人类胚胎。 | 祖细胞没有争议。 |
造血细胞和骨髓细胞移植治疗2型糖尿病
自体骨髓含有造血干细胞、单核细胞、少量间充质细胞和其他细胞的混合物。外周血干细胞主要通过其CD34抗原阳性来选择。据称,不同的造血细胞制剂可有效纠正高血糖、改善内源性胰岛素的产生,以及减少或消除对胰岛素和其他糖尿病控制治疗的需求。
王等人使用自体骨髓治疗31名患者,将干细胞输注到为胰腺供血的主要动脉中。HbA1c在30天内下降了 > 1.5%,C 肽在3个月的随访标记时增加。据报道,所有患者的抗糖尿病药物用量都显着减少。

Bhansali等人[19]在一项旨在治疗11名患者的前瞻性随机安慰剂对照试验中使用了骨髓单核细胞 (BM-MNC) 。在干预组中,11名患者中有9名 (82%) 的胰岛素需求减少了50%,10名 (91%) 的HbA1c<7%。

这两项最近对已发表试验的荟萃分析得出结论,BM-MNC和外周血单核细胞输注可能会导致大多数接受治疗的患者在12个月时改善HbA1C、空腹血糖、C肽水平和内源性胰岛素产生患者。
人类胚胎干细胞
胚胎干细胞可以在体外和体内分化,形成广泛的特化细胞类型。胚胎干细胞取自胚泡阶段的胚胎,具有多能性。它们的多功能性是成体干细胞的优点,但也是一个挑战。虽然ES细胞在培养中可以变成胰岛素分泌细胞,例如,细胞不如成体干细胞稳定。体外和体内研究的ES细胞可以分化成肿瘤细胞。同样,ES 细胞的快速增殖率也高于成体细胞,在体内形成肿瘤的风险更大。
1998年分离和培养人类胚胎干细胞 (ESC) 的方法的发现重新燃起了研究人员、临床医生和糖尿病患者及其家人的希望,即治愈1型DM和非DM1型的方法可能在打击距离。理论上,可以培养ESC并诱导其发育成产生胰岛素的胰腺胰岛细胞。有了现成的培养干细胞供应,理论上可以根据需要为任何需要移植的人培育出一系列胚胎干细胞。
干细胞研究——优点和缺点
表2列举了干细胞来源的优缺点
| 干细胞类型 | 来源 | 优点 | 缺点 |
| 胚胎的 | 来自人类囊胚的细胞 | 多能 | 需要破坏胚胎 |
| 胎儿干细胞 | 来自流产胎儿性腺的细胞 | 多能 | 需要破坏数周大的胎儿 |
| 脐带干细胞 | 来自新生儿脐带血的细胞 | 多能/多能? | 干细胞频率低 |
| 胎盘干细胞 | 来自新生儿胎盘的细胞 | 多能/多能? | 低频率(但高于脐带血) |
| 成体干细胞 | 来自成人组织的细胞 | 多能 | 非常低的频率 |
| 诱导多能干细胞 (iPS) | 来自成人组织的细胞重新编程为多能性 | 多能 | 不可申请专利 |

优点
1)在治疗性克隆和再生医学领域提供医疗效益。
2) 它为发现治疗和治愈多种疾病提供了巨大的潜力,包括帕金森病、精神分裂症、阿尔茨海默病、癌症、脊髓损伤、糖尿病等等。
3) 可以在实验室中用干细胞培养四肢和器官,然后用于移植或帮助治疗疾病。
4) 它将帮助科学家了解人类生长和细胞发育。
5) 科学家和医生将能够在不使用动物或人类测试者的情况下测试数百万种潜在的药物和药物。这需要一个模拟药物对特定细胞群影响的过程。这将告诉您该药物是否有用或有任何问题。
6) 干细胞研究也有利于对人类胚胎无法直接研究的发育阶段的研究,这些阶段有时与出生缺陷、流产和不孕等重大临床后果有关。对正常发育的更全面了解最终将有助于预防或治疗人类发育异常。
7) 干细胞研究也有利于对人类胚胎无法直接研究的发育阶段的研究,这些阶段有时与出生缺陷、流产和不孕等重大临床后果有关。对正常发育的更全面了解最终将有助于预防或治疗人类发育异常。
8) 使用成体干细胞治疗疾病的一个优势是患者自身的细胞可用于治疗患者。风险会大大降低,因为患者的身体不会排斥自己的细胞。
9) 胚胎干细胞可以发育成身体的任何细胞类型,然后可能比成体干细胞更通用。
缺点
1) 将胚胎干细胞用于研究涉及破坏由实验室受精的人类卵子形成的囊胚。对于那些相信生命始于受孕的人来说,囊胚是人类的生命,摧毁它是不道德和不可接受的。
2) 与任何其他新技术一样,这种对自然的干扰会产生什么样的长期影响也是完全未知的。
3) 胚胎干细胞可能不是所有疾病的解决方案。
4) 根据一项新的研究,干细胞疗法被用于心脏病患者。结果发现它可以使他们的冠状动脉变窄。
5) 大多数成体干细胞的缺点是它们是预特化的,例如,造血干细胞只制造血液,而脑干细胞只制造脑细胞。
6) 这些来自非患者自己的胚胎,患者的身体可能会排斥它们。
多能干细胞
多能干细胞(PSCs)具有自我更新和分化为外胚层、内胚层和中胚层三个胚层的能力,因此可以在再生医学和细胞治疗中发挥重要作用。PSC是从囊胚的内细胞团(胚胎干细胞,ES)或胎儿生殖嵴(胚胎生殖细胞,EG)中获得的。Thomson教授及其团队于1998年首先报道了人ES细胞系,而Shamblott教授于同年报道了人EG细胞系。
还存在通过使用多种因子(诱导多能干细胞,iPS)将它们重新编程为胚胎状态或通过允许卵母细胞细胞质中存在的因子重新编程体细胞(治疗性克隆)来从成体体细胞中提取PSC的技术。
Yamanaka教授因iPS技术分享了2012年的诺贝尔医学奖,而Mitalipov教授的团队在2013年率先通过体细胞核移植 (SCNT) 获得了人类ES细胞系。Jiang等人观察到30%的移植小鼠在移植通过分化ES细胞获得的胰岛素阳性细胞后,在超过六个月的时间内表现出高血糖降低。因此,建立了使用人类胚胎干细胞治疗糖尿病的概念证明;然而,这个过程仍然非常低效。
能干细胞的治疗最严重的问题无疑是畸胎瘤的形成。在最初的临床前研究中,由于受到多能干细胞污染,畸胎瘤的形成是常见的事。随着分化方案的完善和耐用封装设备的使用,这个问题似乎已经得到解决。在用于临床试验的胰腺祖细胞的分化细胞制剂中,没有发现残留的多能干/祖细胞。
▉ VC-01的临床试验
2015年,第一例1型糖尿病患者在埃德蒙顿接受了hESC来源的胰腺前体细胞移植,由美国再生医学公司ViaCyte主导。临床试验(NCT02239354,2014年提交)的目的是测试hESC来源的胰腺前体细胞(PEC-01),这些细胞有望在移植后成熟为有功能的胰岛素生成细胞。第一次移植4000万个细胞,分两个胶囊封装设备(PEC-Encap),和六个较小的胶囊封装植入手臂皮下。
VC-01(PEC-01细胞和PEC-Encap设备的组合)在一项开放的、剂量递增的1/2期研究中进行评估,研究对象是产生胰岛素的β细胞功能最低的1型糖尿病患者。初步临床试验的报告表明,在移植的“前哨”设备中,显示存活细胞很少,甚至没有活细胞(不知道是否是早期缺氧的问题,因为移植的细胞显示附近有血管生成,供氧不足)。其次,会引起强烈的细胞异物反应,极大影响植入胰腺祖细胞的存活,堵塞了半透膜,阻止了血管形成。2018年6月,ViaCyte发布了PEC-Encap针对 1 型糖尿病1/2期临床试验的两年数据,结果显示该产品安全且耐受性良好,可分化为胰岛素生成细胞。
▉ VC-02的临床试验
2017年,ViaCyte启动了一项新的为期1年的临床试验(NCT03162926),引入了另一种胶囊封装设备(PEC-Direct,VC-02),改良后的膜允许血管形成,但不提供免疫保护,需要使用免疫抑制剂。正在进行的为期2年的临床试验(NCT03163511),旨在测试VC-02皮下植入1型糖尿病患者时的安全性和耐受性。PEC-01细胞可以移植存活,并产生可测量的C肽水平。一小部分患者(6/18)的初步结果显示,移植后9个月后,大量移植的装置中含有胰岛素阳性细胞。而全部的患者都能在术后12个月内维持产生C肽(有些患者已经达到15、18或21个月都有C肽表达)。
2022年初,ViaCyte宣布了I/II 期临床试验结果:将具有血管形成能力的微囊化的 PEC-01 细胞植入1型糖尿病患者皮下后,它们能够在体内成功存活下来并成熟为功能性的β细胞。
间充质干细胞
间充质干细胞 (MSC) 是自我更新的多能细胞,能够分泌多种生物因子,恢复和修复受损组织。临床前和临床证据证实了 MSCs 在各种医疗条件下的治疗益处。目前,MSCs 是临床试验中最常用的基于细胞的疗法,因为它们具有再生作用、易于分离和低免疫原性。实验和临床研究已经提供了使用 MSCs 治疗糖尿病的有希望的结果。
2015年,来自瑞典的研究人员率先评估了自体间充质干细胞治疗新诊断1型糖尿病的安全性和有效性。从髂嵴骨髓中采集干细胞,中位全身单剂量为2.75×106个细胞/kg。他们得出结论,MSCs的施用并未导致10 名患者中的任何一名发生不良事件,并且在1年的随访中提供了有希望的C肽浓度。该I期试验未显示对照组和MSC组在血红蛋白A1c (HbA1c) 或胰岛素剂量方面存在任何功能差异。
Hu及其同事进行了一项单中心、双盲研究,以检验脐带沃顿氏胶质来源的MSCs对新发I型糖尿病患者的安全性、可行性和初步结果。MSC治疗组接受了两次静脉输注(平均细胞计数为 2.6 × 10 7) 相隔4周。在 MSC输注后9至24个月,实验组的餐后血糖和HbA1c测量值较低。此外,MSC组的胰岛素使用和空腹C肽显着改善。研究作者得出结论,在他们的小型研究中,脐带间充质干细胞移植是可行且安全的,无法检测功能差异。
在中国进行的一项涉及将胎盘来源的MSCs输送给患有长期2型糖尿病的患者的初步研究表明,移植是安全、简单且可能有效的。该调查包括10名病程≥3年、胰岛素依赖(≥0.7U/kg/天)至少1年且血糖控制不佳的2型糖尿病患者。受试者平均收到1.35×106/kg胎盘干细胞在三个不同的场合,静脉输注之间间隔1个月。治疗六个月后,所有患者的胰岛素剂量和HbA1c测量值均有所改善。此外,MSC治疗后C肽和胰岛素释放也更高。此外,这项研究包括一组更接近实际临床情况的个体,因为他们还患有其他合并症,包括心脏病、肾脏疾病和血管并发症。
2018年进行的一项荟萃分析,包括9项随机对照试验和14项自身对照试验,结论是,造血干细胞和间充质干细胞单独或联合移植的混合效应导致C肽水平高于常规胰岛素治疗,而脐带血间充质干细胞则没有达到显著性水平。另一项对2019年发表的6项1型糖尿病随机对照试验的荟萃分析显示,在葡萄糖刺激情况下,C肽水平和空腹C肽水平没有差异。糖化血红蛋白(HbA1c)的降低是治疗患者和对照组之间观察到的唯一不同之处。
间充质干细胞治疗1型糖尿病争议颇多,而治疗2型糖尿病临床试验则显示出一定的疗效。
结论
1型和2型糖尿病都是最适合治疗的疾病。现有β细胞的功能恢复、干细胞或干细胞衍生的 β 样细胞的移植可能会提供新的治疗机会(图 3)。
然而,使用干细胞产生用于糖尿病治疗的可再生β细胞来源仍然具有挑战性,这主要是出于安全方面的考虑。已经有大量已发表的小型研究确实不能构成对正在尝试的不同干细胞功效的可靠科学证据。不同制药公司引入预制备或冷冻细胞,如脐带或骨髓来源的 MSC,在这一点上已被证明是极其昂贵的,而且绝对是绝大多数人无法承受的。需要更大规模的研究来推进该领域并了解实现其潜力的最佳方式。
我们认为干细胞疗法目前只能用于临床试验,直到获得足够的可评估数据。实验室方法,如培养条件和细胞计数方法,必须得到更好的考虑和更统一的标准化,并且对结果的解释应该批判性地进行。
总之,再生医学仍然是一个令人兴奋的新研究领域,它对治疗所有年龄段的内分泌疾病患者具有很大的希望。基于证据的糖尿病症状临床治疗只会增加疾病负担。随着干细胞疗法的出现,根除糖尿病的潜力似乎即将出现。
参考资料:
- Mathers CD, Loncar D (2006) Projections of global mortality and burden of disease from 2002 to 2030. PLoS Med 3: e442.
- William L Isley, Mark E Molitch (2005) Type 1 Diabetes. The Journal of Clinical Endocrinology & Metabolism 90: E2.
- Makam AN, Nguyen OK (2017) An evidence-based medicine approach to antihyperglycemic therapy in diabetes mellitus to overcome overtreatment. Circulation 135: 180-195.
- Mirmira RG (2017) Reprogramming Beta cells in Diabetes: Step closer to cure. MedScape: Diabetes and Endocrinology.
- Li J, Casteels T, Frogne T, Ingvorsen C, Honoré C, et al. (2017) Artemisinins target GABAA receptor signaling and impair α cell identity. Cell 168: 86.e15-100.e15.
- Wang P, Alvarez-Perez JC, Felsenfeld DP, Liu H, Sivendran S, et al. (2015) A high-throughput chemical screen reveals that harmine-mediated inhibition of DYRK1A increases human pancreatic beta cell replication. Nat Med 21: 383-388.
- Fadini GP, Sartore S, Agostini C, Avogaro A (2007) Significance of endothelial progenitor cells in subjects with diabetes. Diabetes Care 30: 1305-1313.
- Zeng YC, Ricordi C, Lendoire J, Carroll PB, Alejandro R, et al. (1993) The effect of prednisone on pancreatic islet autografts in dogs. Surgery 113: 98-102.
- Lakey JR, Warnock GL, Rajotte RV, Suarez-Alamazor ME, Ao Z, et al. (1996) Variables in organ donors that affect the recovery of human islets of Langerhans. Transplantation 61: 1047-1053.
- Woodfield J (2017) Success for new method of islet cell transplantation in type 1 diabetes. Diabetes News.
- Ryan EA, Lakey JR, Rajotte RV, Korbutt GS, Kin T, et al. (2001) Clinical outcomes and insulin secretion after islet transplantation with the Edmonton protocol. Diabetes 50: 710-719.
- Shapiro AM, Lakey JR, Ryan EA, Korbutt GS, Toth E, et al. (2000) Islet transplantation in seven patients with type 1 diabetes mellitus using a glucocorticoid-free immunosuppressive regimen. N Engl J Med 343: 230-238.
- Shapiro AM, Ricordi C, Hering BJ, Auchincloss H, Lindblad R, et al. (2006) International trial of the Edmonton Protocol for islet transplantation. N Engl J Med 355: 1318-1330.
- Westenfelder C, Gooch A, Hu Z, Ahlstrom J, Zhang P (2017) Durable control of autoimmune diabetes in mice achieved by intraperitoneal transplantation of “Neo-Islets,” three-dimensional aggregates of allogeneic islet and “mesenchymal stem cells”. Stem Cells Transl Med 6: 1631-1643.
- Barton FB, Rickels MR, Alejandro R, Hering BJ, Wease S, et al. (2012) Improvement in outcomes of clinical islet transplantation: 1999-2010. Diabetes Care 35: 1436-1445.
- Carlow DA, Gold MR, Ziltener HJ (2009) Lymphocytes in the peritoneum home to the omentum and are activated by resident dendritic cells. J Immunol 183: 1155-1165.
- Litbarg NO, Gudehithlu KP, Sethupathi P, Arruda JA, Dunea G, et al. (2007) Activated omentum becomes rich in factors that promote healing and tissue regeneration. Cell Tissue Res 328: 487-497.
- Wehbe T, Chahine NA, Sissi S, Isabelle Abou-Joaude, Louis Chalhoub (2016) Bone marrow derived stem cell therapy for type 2 diabetes mellitus. Stem Cell Investig 3: 87.
- Bhansali A, Asokumar P, Walia R, Bhansali S, Gupta V, et al. (2014) Efficacy and safety of autologous bone marrow-derived stem cell transplantation in patients with type 2 diabetes mellitus: A randomized placebo-controlled study. Cell Transplant 23: 1075-1085.
- Wu Z, Cai J, Chen J, Huang L, Wu W, et al. (2014) Autologous bone marrow mononuclear cell infusion and hyperbaric oxygen therapy in type 2 diabetes mellitus: An open-label, randomized controlled clinical trial. Cytotherapy 16: 258-265.
- Subrammaniyan R, Amalorpavanathan J, Shankar R, Rajkumar M, Baskar S, et al. (2011) Application of autologous bone marrow mononuclear cells in six patients with advanced chronic critical limb ischemia as a result of diabetes: Our experience. Cytotherapy 13: 993-999.
- Wang L, Zhao S, Mao H, Zhou L, Wang ZJ, et al. (2011) Autologous bone marrow stem cell transplantation for the treatment of type 2 diabetes mellitus. Chin Med J (Engl) 124: 3622-3628.
- Kodama S, Faustman DL (2004) Routes to regenerating islet cells: Stem cells and other biological therapies for type 1 diabetes. Pediatr Diabetes 5: 38-44.
- Odorico JS, Kaufman DS, Thomson JA (2001) Multilineage differentiation from human embryonic stem cell lines. Stem Cells 19: 193-204.
- Calafiore R, Montanucci P, Basta G (2014) Stem cells for pancreatic β-cell replacement in diabetes mellitus: Actual perspectives. Curr Opin Organ Transplant 19: 162-168.
- Grompe M (2002) Adult versus embryonic stem cells: It’s still a tie. Mol Ther 6: 303-305.
- Thomson JA, Itskovitz-Eldor J, Shapiro SS, Waknitz MA, Swiergiel JJ, et al. (1998) Embryonic stem cell lines derived from human blastocysts. Science 282: 1145-1147.
- Shamblott MJ, Axelman J, Wang S, Bugg EM, Littlefield JW, et al. (1998) Derivation of pluripotent stem cells from cultured human primordial germ cells. Proc Natl Acad Sci U S A 95: 13726-13731.
- Takahashi K, Yamanaka S (2006) Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors. Cell 126: 663-676.
- Tachibana M, Amato P, Sparman M, Nuria Marti Gutierrez, Rebecca Tippner-Hedges, et al. (2013) Human embryonic stem cells derived by somatic cell nuclear transfer. Cell 153: 1228-1238.
- Jiang J, Au M, Lu K, Eshpeter A, Korbutt G, et al. (2007) Generation of insulin-producing islet-like clusters from human embryonic stem cells. Stem Cells 25: 1940-1953.
- Schulz TC, Young HY, Agulnick AD, Babin MJ, Baetge EE, et al. (2012) A scalable system for production of functional pancreatic progenitors from human embryonic stem cells. PLoS One 7: e37004.
- Bruin JE, Erener S, Vela J, Hu X, Johnson JD, et al. (2014) Characterization of polyhormonal insulin-producing cells derived in vitro from human embryonic stem cells. Stem Cell Res 12: 194-208.
- Kirk K, Hao E, Lahmy R, Itkin-Ansari P (2014) Human embryonic stem cell derived islet progenitors mature inside an encapsulation device without evidence of increased biomass or cell escape. Stem Cell Res 12: 807-814.
- Hu J, Yu X, Wang Z, Wang F, Wang L, et al. (2013) Long term effects of the implantation of Wharton’s jelly-derived mesenchymal stem cells from the umbilical cord for newly-onset type 1 diabetes mellitus. Endocr J 60: 347-357.
- Jiang R, Han Z, Zhuo G, Qu X, Li X, et al. (2011) Transplantation of placenta-derived mesenchymal stem cells in type 2 diabetes: A pilot study. Front Med 5: 94-100.
- Vanikar AV, Dave SD, Thakkar UG, Trivedi HL (2010) Cotransplantation of adipose tissue-derived insulin-secreting mesenchymal stem cells and hematopoietic stem cells: A novel therapy for insulin-dependent diabetes mellitus. Stem Cells Int 2010: 1-5.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞不保证信息的准确性和完整性。所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 官方微信公众号
官方微信公众号