系统性红斑狼疮 (SLE) 是一种慢性自身免疫性疾病,可影响多个器官系统,其表现和对治疗的反应各不相同。与成人SLE相比,儿童期确诊的SLE发病率和死亡率更高,通常需要大量免疫抑制,且有严重副作用的风险。
对于重症或难治性疾病患者,仍存在大量未满足的新疗法需求,这些疗法可以改善疾病控制并减少糖皮质激素和其他毒性药物的暴露。SLE的发病机制涉及B细胞失调和自身抗体产生,这是该疾病的标志。目前批准的B细胞定向疗法通常会导致B细胞耗竭不完全,并且可能不会针对导致SLE自身抗体的长寿浆细胞。
据推测,通过持续消除B细胞和浆母细胞,CAR-T疗法可以阻止自身免疫并防止对当前B细胞耗竭治疗有抵抗力的患者的器官受损。
近期,期刊杂志Pediatric Rheumatology(小儿风湿病学)发表了一篇“CAR-T细胞治疗难治性儿童系统性红斑狼疮:新时代的希望”的文献综述。

综述表明CAR-T细胞疗法在治疗年轻成人难治性SLE方面已证明是安全有效的,据报道,单次输注后疗效可持续2年。最近有新疗法被批准用于治疗狼疮性肾炎,包括治疗的诱导期;然而,这些药物中的大多数都是作为附加疗法。
在此,我们总结了目前利用CAR-T细胞治疗系统性红斑狼疮的临床前和临床数据,并讨论了这种治疗方式治疗狼疮的未来。
什么是系统性红斑狼疮
系统性红斑狼疮(SLE)是一种严重的自身免疫性疾病,在普通人群中的发病率为0.1%,主要影响年轻女性。在这种终身性疾病中,包括双链DNA(dsDNA)和核蛋白在内的核抗原的免疫耐受性被破坏,导致患者T淋巴细胞减少、抑制性T细胞功能降低、B细胞过度增生,从而产生大量针对dsDNA和其他核抗原的自身抗体,随后在一系列不同器官引发免疫复合物诱导的炎症反应,主要影响关节和皮肤,还可能导致对器官的严重损害。
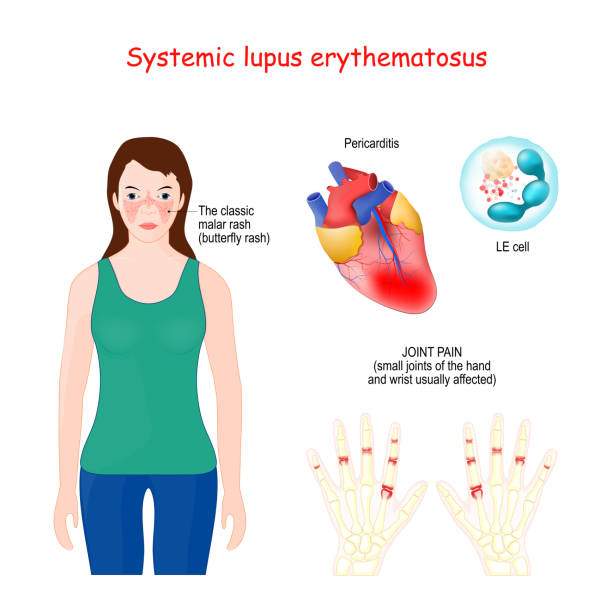
近年来,系统性红斑狼疮的治疗取得了重大进展,然而,仍有一些患者对当前的疗法没有反应,从而处于器官衰竭甚至死亡的高风险中。此外,目前也没有可靠的策略可以无药物缓解甚至治愈该疾病,因此,患者通常需要终身治疗。
系统性红斑狼疮的疾病发病机制和针对性治疗
先天性和适应性免疫反应都与SLE的发病机制有关。先天免疫系统包括补体蛋白、巨噬细胞、中性粒细胞、抗原呈递细胞以及各种抗菌分子和支持细胞。在SLE中,凋亡物质清除能力较差,从而允许细胞内物质呈递,然后引发炎症级联。补体途径和Fas配体途径的异常和缺陷也与其发病机制有关。中性粒细胞凋亡缺陷会导致抗原产生增加并引发炎症。适应性免疫系统包括T细胞、B细胞和自然杀伤细胞。
在SLE中,B细胞失调并产生自身抗体,这是SLE的标志。自身抗体被认为通过多种方式促成SLE的发病机制,包括沉积以及直接损伤组织、刺激干扰素的产生和信号传导、结合中性粒细胞胞外陷阱并增加其免疫原性。
尽管针对SLE发病机制中涉及的免疫系统不同方面采取了多模式治疗,但许多患者的病情仍然难以治愈,难治性定义为“3-4个月内无改善或5-12个月后无法达到部分缓解或2年治疗后无法完全缓解”。大多数研究表明,当患者对除皮质类固醇外的1-3种免疫抑制药物无反应时,SLE也被认为是难治性的。鉴于这些患者已经用尽了许多治疗选择,他们通常依赖糖皮质激素来控制病情。
广泛实施诸如CYC之类的治疗方法已经改善了难治性疾病患者的预后,但对于患有严重肾脏疾病的患者来说,疗效较为有限。
CAR-T细胞在人类系统性红斑狼疮中的应用
鉴于这些有希望的临床前数据和CD19 CAR-T细胞用于治疗血液系统恶性肿瘤的大量临床经验,人们对利用CD19 CAR-T细胞治疗自身免疫性疾病有着浓厚的兴趣。
在患有SLE、抗合成酶综合征和重症肌无力的患者中已证实了早期临床成功。
2021年,德国的一个研究小组发表了第一份关于CAR-T治疗人类SLE的报告。MougiakakosD等人报道了一例20岁重度难治性SLE女性患者,其表现为活动性狼疮性肾炎(IIIA类)、肾病综合征、心包炎、胸膜炎、皮疹、关节炎,并有利布曼-萨克斯心内膜炎病史,尽管使用羟氯喹、大剂量糖皮质激素、CYC、霉酚酸酯 (MMF)、他克莫司、贝利木单抗和利妥昔单抗治疗,但狼疮仍未得到充分控制。

CD19靶向CAR-T细胞治疗难治性系统性红斑狼疮
在使用氟达拉滨和CYC进行淋巴细胞清除后,单剂量给予1.1×106CD19CAR-T细胞/kg(CD4+与CD8+T细胞比例为3:1)。CAR-T疗法的常见副作用包括细胞因子释放综合征 (CRS)、免疫效应细胞相关神经毒性综合征 (ICANS) 和长期血细胞减少症,但该患者未出现。她的循环B细胞完全耗竭,并且这种情况持续了44天以上。
她的双链DNA (dsDNA) 自身抗体和补体水平恢复正常。临床上,她的蛋白尿有所改善,治疗后SLEDAI评分从18提高到0。
2022年,国际期刊杂志《自然》子刊《自然医学》发表了一篇“抗CD19 CAR-T细胞疗法治疗难治性系统性红斑狼疮”的文章,文章概述了五名患有难治性狼疮的年轻成年患者参加了自体CD19CAR-T细胞疗法的用药试验,这些患者先前使用常规免疫抑制剂治疗失败。
患者年龄为18至24岁,患病时间为1至9年,根据SLEDAI测量,基线狼疮疾病活动性较高(评分为8至16)。所有患者均患有狼疮性肾炎(III、IV或III/V期)。

治疗难治性系统性红斑狼疮的抗CD19 CAR-T细胞疗法
五名SLE患者(四名女性和一名男性)的中位年龄(范围)为22 (6) 岁,中位病程(范围)为4 (8) 年,疾病处于活动期(中位SLE疾病活动指数系统性红斑狼疮疾病活动指数:16 (8)),对几种免疫抑制药物治疗有抵抗力,他们参加了一项同情使用嵌合抗原受体 (CAR) T细胞计划。SLE患者的自体T细胞被慢病毒抗CD19CAR载体转导,扩增并在用氟达拉滨和环磷酰胺进行淋巴细胞清除后以1×106CAR-T细胞/公斤体重的剂量回输给患者。
CAR-T细胞在体内扩增,导致B细胞深度耗竭、临床症状改善和实验室参数正常化,包括抗双链DNA抗体血清转化。根据DORIS标准,所有五名患者在3个月后均达到 SLE缓解,3个月后系统性红斑狼疮疾病活动指数评分中位数(范围)为0(2)。
在较长的随访期间(CAR-T细胞给药后中位数(范围)为8(12)个月)仍保持无药缓解,甚至在B细胞重新出现后仍保持无药缓解,在CAR-T细胞治疗后平均(±sd)110±32天后观察到。重新出现的B细胞是幼稚的,并显示非类别转换的B细胞受体。CAR-T细胞治疗耐受性良好,仅出现轻度细胞因子释放综合征。
这些数据表明CD19 CAR-T细胞在治疗系统性红斑狼疮中是可行、可耐受且高效的。
2023年,一名32岁的SLE女性患者成功接受了CD19靶向CAR-T细胞治疗。她在怀孕期间被诊断出患有狼疮。临床表现包括浆膜炎、肾炎、血细胞减少、免疫学发现(ANA、dsDNA、低补体血症)以及对中枢神经系统受累的担忧。她对多种药物(包括他克莫司、贝利木单抗、CYC和利妥昔单抗)仍无反应。
在接受细胞回收预处理治疗之前,她在白细胞分离术前三周停用免疫抑制剂,只使用糖皮质激素,糖皮质激素逐渐减少至每日5毫克。她耐受CAR-T细胞治疗,未报告任何不良反应,三个月后,她根据低狼疮疾病活动状态 (LLDAS) 标准达到狼疮低疾病活动状态,蛋白尿恢复正常,治疗三个月后,她体内不再检测到循环抗dsDNA抗体。值得注意的是,B细胞在2个月内返回外周血,且未发生相关疾病复发。
2024年,3月27日,浙江大学医学院附属儿童医院运用CAR-T治疗的系统性红斑狼疮患儿顺利出院。

回输当日,浙江大学医学院附属儿童医院毛建华教授(右二)团队在观察受试患儿。受访者供图
12岁女孩灿灿(化名)三年多前不幸确诊为系统性红斑狼疮,这些年一直在浙大儿院风湿免疫科接受治疗。尽管同龄患者大多病情可控,但灿灿却对药物反应欠佳,面部蝴蝶斑、身上也经常有皮疹反复,加之口腔溃疡、关节疼痛等症状加剧,正处于青春期的她深受困扰。由于长期依赖激素治疗,灿灿已有典型的“满月脸”特征。
就在今年2月份,灿灿在随诊时发现新出现了尿蛋白,检查结果显示24小时尿蛋白定量高达2000毫克,如果继续升高,很有可能会发展成为肾病综合征和慢性肾功能不全。”
常规手段差不多都用过了,病情依然难以控制,还能怎么帮助这位孩子?
综合考量下,毛建华教授提议灿灿可入组,团队正在推进的靶向CD19嵌合抗原受体T淋巴细胞(CAR-T)治疗难治性儿童系统性红斑狼疮(cSLE)的临床研究,这对灿灿来说,这无疑是新的希望。在家人的鼓励下,灿灿停用了除CAR-T治疗的一切药物,参加了这项临床治疗研究。
2024年2月8日,灿灿入组到红斑狼疮CAR-T治疗临床研究项目,2月22日,研究团队对她实现单采,3月12日把经过CAR-T处理后的细胞回输到孩子体内。
“整个治疗过程,孩子的感受就跟一次时长仅十多分钟的输液差不多,不用承受那么多痛苦。可以说她是在放松、快乐的心情中接受了CAR-T治疗,副作用反应也很快过去,现在看着就跟普通孩子差不多。”何雪开心分享。
因为一切都十分顺利,3月27日,在回输半个月后,灿灿顺利出院。
血液肿瘤科主任徐晓军表示,CAR-T细胞疗法的应用不局限于白血病,从国际研究来看,在系统性红斑狼疮、皮肌炎等风湿免疫疾病的治疗效果也很显著。此次毛建华教授团队把这技术用于红斑狼疮治疗,是临床的重要探索,具有重要意义。
“截至目前,治疗效果还是不错的,尿蛋白明显减少,皮疹和口腔溃疡都没有新发,孩子状态明显好了很多,灿灿还告诉我她回家后要看演唱会。目前我们会进一步关注孩子的病情,后期需要患者定期随访复查。医院团队也在探索,希望未来CAR-T细胞疗法除了应用于系统性红斑狼疮外,还能用于其他严重疾病的治疗,给更多患者带去希望。”毛建华教授说。
表1:针对人类SLE患者的CAR-T疗法综述:
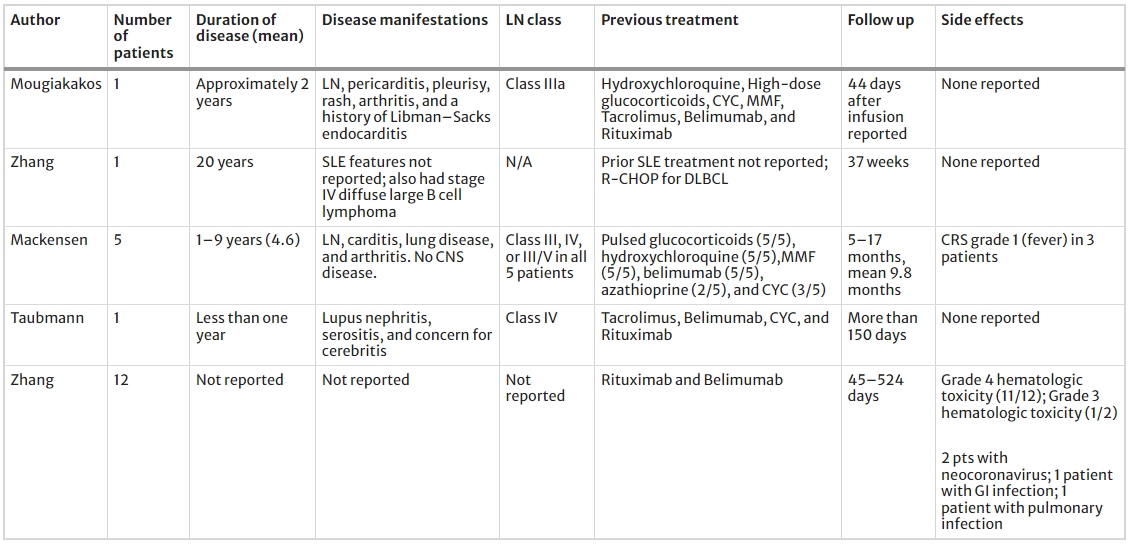
讨论和结论
总之,尽管最近可用的SLE治疗方法有所扩展,但缓解率仍然低得令人无法接受,发病率和死亡率仍然高得令人无法接受。对于儿童期发病的SLE患者来说尤其如此,与成人发病的SLE相比,他们的疾病严重程度和预后更差。B细胞定向CAR-T细胞疗法为改善难治性儿科疾病的预后提供了巨大的希望。
如上所述,CAR-T细胞疗法在治疗年轻成人难治性SLE方面已证明是安全有效的,据报道,单次输注后疗效可持续2年。最近有新疗法被批准用于治疗狼疮性肾炎,包括治疗的诱导期;然而,这些药物中的大多数都是作为附加疗法。
因此,CAR-T细胞疗法在减少SLE儿童和青少年对其他潜在毒性药物(包括糖皮质激素)需求方面的潜力尤其令人鼓舞。由于目标T细胞群较小,因此SLE患者的安全性迄今为止比肿瘤患者更佳,从而导致CRS的潜在风险较低。
CAR-T细胞能够消除组织驻留B细胞,这些细胞在使用目前可用的其他B细胞耗竭药物(例如利妥昔单抗和贝利木单抗)治疗后仍可能导致疾病发病。然而,外周B细胞区室大多数情况下都会恢复,迄今为止尚未在该患者群体中报告任何显著的副作用。值得注意的是,最近报道的CAR-T治疗T细胞淋巴瘤的安全性信号很少见,在无潜在原发性恶性肿瘤的患者中尚未报道过。
由于接受CAR-T细胞疗法治疗自身免疫性疾病的患者数量有限,因此需要进一步的数据来评估其长期安全性。在成人和儿童狼疮中开展的 CAR-T治疗对照临床试验将进一步深入了解该疗法的有效性、安全性和持久性(表2)。
| 临床试验: | 地点: | 资格标准: | 年龄 | 输注剂量: | 疾病活动度要求: | 主要结果: |
|---|---|---|---|---|---|---|
| 双靶点CAR-T细胞治疗难治性SLE患者 | 上海交通大学医学院仁济医院南院风湿免疫科上海, 上海, 中国 | 血清或尿液妊娠检测阴性筛查和基线妊娠试验阴性受试者同意在试验期间直至CAR-T细胞输注后至少1年采取有效的避孕措施。白细胞≥2.5×10^9/L NEUT≥1×10^9/L BPC≥50×10^9/L | 18–70 | DL-1:0.5±20%×10^5/kg,DL1:1±20%×10^5/kg,DL2:2±20%×10^5/kg DL3:3±20%×10^5/kg | 塞莱娜-斯莱达 I ≥ 8 | 剂量限制毒性 |
| 抗CD19 CAR-T细胞治疗儿童难治性SLE的疗效研究 | 浙江大学医学院附属儿童医院 | 心脏、肾脏和肾功能正常 | 5–18 | 三个剂量组(1×105/kg、3×105/kg、5×105/kg) | 尽管已使用≥ 3 M 高剂量糖皮质激素(泼尼松≥ 1 mg/kg/d 或同等量的其他类固醇)、羟氯喹和至少 2 种以下治疗(CYC、MMF、硫唑嘌呤、甲氨蝶呤、环孢菌素、他克莫司、雷帕霉素、来氟米特、替他西普、贝利尤单抗、和利妥昔单抗);或对标准治疗不耐受SLEDAI 2K评分≥8分 | 安全3个月 |
| CD19 重定向自体 T 细胞治疗 CD19 阳性系统性红斑狼疮 (SLE) 的研究 | 上海交通大学医学院附属仁济医院中国上海 | 肌酐<1.5毫克/分升心脏射血分数 > 55%血红蛋白 > 9 克/分升胆红素 < 2.0 毫克/分升 | 18–69 | 1E6 ~ 1E7 CD19-CAR阳性T细胞 | 未指定 | CAR-T 细胞 6 周安全性 |
| BRL-301(靶向CD19基因的同种异体嵌合抗原受体T细胞注射液)治疗难治性SLE的安全性和有效性临床研究 | 浙江大学医学院附属第一医院中国浙江省杭州市 | 充足的骨髓、肝脏凝血和心脏功能输注后至少 6 个月内采取避孕措施或禁欲 | 18–65 | 未指定 | 至少获得一个 BILAG2004 A 类成绩或两个 B 类成绩,或两者兼有;SELENA-SLEDAI评分≥8分; | BRL-301 治疗 SLE 12 个月的安全性 |
| CD19/BCMA 嵌合抗原受体 T 细胞治疗难治性 SLE 患者的安全性和有效性临床试验 | 浙江大学医学院附属第一医院中国浙江省杭州市 | CD19/BCMA 表达阳性的 SLE,且常规治疗无效和(或)无有效治疗预计生存时间>12周;给药开始前尿妊娠试验阴性并同意在整个研究期间采取有效的避孕措施 | 儿童、成人、老年人 | 未指定 | 未指定 | 安全性和剂量限制毒性 |
| GC012F注射液治疗难治性SLE的I期临床研究 | 浙江大学医学院附属第一医院中国浙江省杭州市 | 血红蛋白≥85g/L;WBC≥2.5×10^9/L;NEUT≥1×10^9/L;PLT≥50×10^9/LAST/ALT低于正常上限2倍;肌酐清除率≥30mL/min;血胆红素≤2.0mg/dl;超声心动图提示射血分数≥50%; | 18–70 | 未指定 | 塞莱娜-雪莱迪亚≥8 | 具有药物限制性毒性的受试者比例 |
| 一项开放标签、多中心、1/2 期研究,旨在评估 YTB323 对重度难治性 SLE 患者的安全性、有效性和细胞动力学 | 诺华研究基地 | 肾脏、肝脏、心脏、血液和肺功能充足 | 18–65 | 未指定 | 对两种或两种以上标准免疫抑制疗法无反应SLEDAI-2 K ≥ 8(不包括 SLEDAI-2 K 的狼疮性头痛、脑血管意外、器质性脑综合征等范畴)且至少存在以下一项显著的 SLE 相关器官受累:(肾脏、中度或重度心肌炎、中度或重度胸膜炎或其他肺部受累、血管炎) | 发生 AE 和 SAE 的参与者人数以及长期安全性随访 1-2 年 |
| Descartes-08 适用于 SLE 患者 | 深厚研究有限责任公司美国加利福尼亚州欧申赛德 | 筛查时 SLE | 18 岁以上 | 未指定 | 尽管最近或正在接受糖皮质激素免疫抑制治疗,并且在筛查后的 24 个月内尝试了至少 12 周的其他 2 种免疫抑制药物,但仍有活动性症状。经 CLIA 认证实验室评估,筛选时可检测到以下至少一种抗体:抗 dsDNA、抗组蛋白、抗染色质和/或抗 Sm 抗体。 | 评估 Descartes-08 对 SLE 患者的安全性和耐受性 |
| PiggyBac 转座子介导的嵌合抗原受体 T 细胞靶向 CD-19 治疗泰国难治性 SLE 患者的安全性/I 期研究 | 朱拉隆功国王纪念医院曼谷, 请选择, 泰国 | 有生育能力或有生育潜力的参与者必须同意从入组到接受 CAR-T 细胞输注后四个月内实施避孕 | 18–60 | 未指定 | 1 持续活动性 SLE 需要持续维持治疗(若无禁忌症):抗疟药。MMF(每日最低剂量 1500 毫克)或硫唑嘌呤(每日最低剂量 1.5 毫克/千克)。患者还必须需要每天至少服用 7.5 毫克泼尼松龙来维持较低的疾病活动度或使 SLEDAI 评分达到 8 分或更高。 | 安全 |
| 一项 1/2 期开放标签研究,旨在评估 IMPT-514 对活动性、难治性狼疮性肾炎和系统性红斑狼疮患者的安全性、耐受性、药代动力学、药效学和疗效 | 加州大学洛杉矶分校(UCLA)医学中心加州大学旧金山分校爱荷华大学亨利福特医疗系统辛辛那提大学 (UC) | 入组时体重>45公斤;血压得到充分控制 | > 18 | 未指定 | 未指定 | 第一阶段:剂量限制性毒性 (DLT)、严重不良事件 (SAE) 和其他治疗中出现的不良事件的发生率( |
| 抗B细胞成熟抗原(BCMA)/分化抗原簇20(CD20)嵌合抗原受体自体T细胞产品(C-CAR168)治疗标准疗法无效的自身免疫性疾病的探索性临床研究 | 上海交通大学医学院仁济医院风湿免疫科上海, 上海, 中国 | 足够的骨髓、凝血、心肺、肝脏和肾功能。 | 18–70 | 未指定 | 接受标准治疗至少 8 周且剂量稳定超过 2 周后,病情仍活跃或复发;患者应接受至少两种免疫抑制剂治疗 | 不良事件发生率(安全性和耐受性 |
| 一项 1/2 期开放标签研究,旨在评估自体 CD19 特异性嵌合抗原受体 T 细胞 (CABA-201) 对活动性 SLE 患者的安全性和有效性 | 加州大学戴维斯分校健康麻省总医院布莱根妇女医院明尼苏达大学哥伦比亚大学欧文医学中心罗切斯特大学北卡罗来纳大学教堂山分校费城儿童医院德克萨斯大学 MD 安德森癌症中心 | 筛选时 ANA 滴度或抗 dsDNA 抗体呈阳性。 | 18–65 | 仅适用于狼疮性肾炎患者,根据 2018 年修订的国际肾脏病学会/肾脏病理学会 (ISN/RPS) 标准,活动性、活检证实的狼疮性肾炎 III 类或 IV 类,无论是否存在 V 类仅适用于非肾脏 SLE 患者:活动性、中度至重度 SLE | 评估不良事件的发生率[时间范围:CABA-201 输注后最多 28 天 | |
| BCMA-CD19 cCAR T 细胞治疗复发/难治性 SLE | 中山市人民医院中国广东省中山市 | 预期生存期≥3个月;血清肌酐<221.0µmol/L(2.5mg/dl);AST/ALT低于正常上限3倍,血胆红素<34.2µmol/L(2.0mg/dl);心肺功能基本正常,超声心动图检查提示射血分数>50%,静息状态下不吸氧血氧饱和度在94%以上;无明显活动性感染;体能素质评分0~2分(ECOG标准);无怀孕 | 18–65 | 未指定 | 未指定 | BCMA-CD19 cCAR T 细胞输注后不良事件的数量和发生率 [ 时间范围:CAR 输注后 3 个月 |
| 通用CAR-T细胞(BRL-301)治疗复发或难治性自身免疫性疾病的安全性和有效性临床研究 | 上海长征医院上海, 上海, 中国 | 流式细胞术测定外周血B细胞CD19阳性表达。骨髓造血功能需满足:(a)白细胞计数≥3×10^9/L;(b)中性粒细胞计数≥1×10^9/L(检查前2周内未接受集落刺激因子治疗);(c)血红蛋白≥60g/L。肝功能:ALT≤3×ULN、AST≤3×ULN、TBIL≤1.5×ULN(不包括Gilbert综合征,总胆红素≤3.0×ULN)(对疾病本身引起的病症无要求)。肾功能:肌酐清除率(CrCl)≥60ml/分钟(Cockcroft/Fault公式)。凝血功能:国际标准化比率(INR)<1.5×ULN,凝血酶原时间(PT)<1.5×ULN。心脏功能:血流动力学稳定性良好。具有生育能力的女性受试者以及伴侣为育龄女性的男性受试者需在研究治疗期间以及研究治疗期结束后至少6个月内使用医学上认可的避孕方法或禁欲;育龄女性受试者在入组研究前7天内血清HCG检测结果为阴性,且未处于哺乳期。 | 18–65 | 未指定 | 未指定 | 安全成果时间范围:12个月 |
参考资料:Stojkic, I., Harper, L., Coss, S. et al. CAR T cell therapy for refractory pediatric systemic lupus erythematosus: a new era of hope?. Pediatr Rheumatol 22, 72 (2024). https://doi.org/10.1186/s12969-024-00990-4
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号