干细胞治疗1型糖尿病是现在再生医学研究领域重要研究的方向。事实上,β细胞替代疗法源于胰岛移植的经验,胰岛移植始于40年前,目前是一个快速发展的领域,正在进行多项使用源自干细胞的β细胞的临床试验。
1型糖尿病特别适合干细胞疗法,因为它是一种由于仅一种细胞类型(产生胰岛素的β细胞)缺乏而引起的疾病,而这种内分泌细胞不需要位于胰腺内部即可发挥其功能。另一方面,双重免疫屏障(同种异体屏障和自身免疫屏障)的存在使得保护β细胞免受排斥成为一项重大挑战。
直到今天,胰岛移植教会了我们很多,开创性的免疫抑制疗法、移植物封装、组织工程和不同植入部位的测试,并激发了对β细胞功能的大量研究。这篇综述从胰岛移植开始,介绍其目前的适应症和最新发表的试验,到干细胞治疗的前景,介绍该领域的最新创新。
今天的胰岛移植
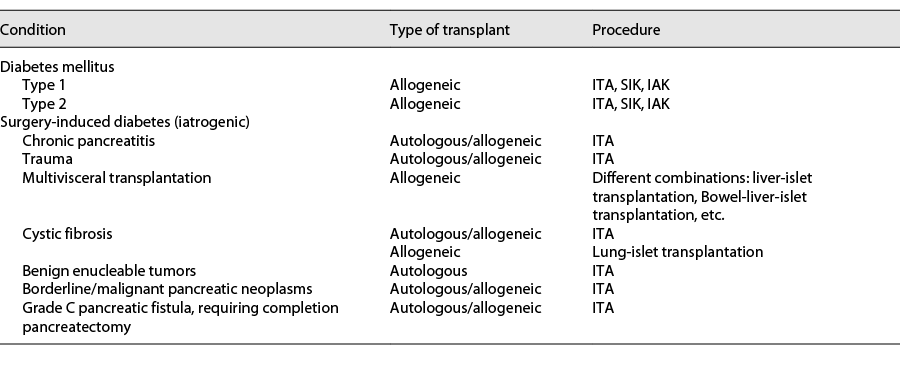
如今,胰岛移植可被视为与β细胞功能丧失相关的多种病症的一种治疗选择(表1)。该程序可以作为单独胰岛移植 (ITA) 在非尿毒症受试者中进行,这是一种通常用于治疗医源性(手术引起的)糖尿病和1型糖尿病的非尿毒症患者的选择。
什么是胰岛移植
- 什么是胰岛?
- 什么是胰岛移植?它如何治疗1型糖尿病?
- 谁适合胰岛移植?
- 医生如何进行胰岛移植?
- 胰岛移植有什么好处?
- 胰岛移植有多成功?
- 胰岛移植有哪些风险?
- 胰岛移植有多普遍?
- 为什么胰岛移植没有更多地用于治疗1型糖尿病?
- 胰岛移植是否用于治疗任何其他病症?
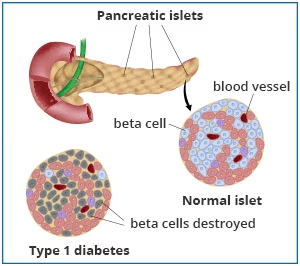
什么是胰岛?
胰岛,也称为朗格汉斯岛,是胰腺中的细胞群。胰腺是一种产生激素的器官,可以帮助您的身体分解和利用食物。胰岛包含多种类型的细胞,包括制造激素胰岛素的β细胞。胰岛素帮助您的身体利用葡萄糖获取能量,并帮助控制您的血糖水平,也称为血糖。
什么是胰岛移植?它如何治疗1型糖尿病?
在1型糖尿病患者中,身体的免疫系统会攻击并破坏β细胞。1型糖尿病患者必须服用胰岛素,因为他们的身体不再产生这种激素。
胰岛移植是1型糖尿病的实验性治疗方法。因为这是一个实验性程序,胰岛移植只能作为美国食品和药物管理局 (FDA) 允许的临床试验的一部分进行。
在用于治疗1型糖尿病的胰岛移植类型中,也称为胰岛同种异体移植,医生从已故器官捐献者的胰腺中取出带有健康β细胞的胰岛。然后,医生将取自捐赠者的健康胰岛细胞注入静脉,该静脉将血液输送至1型糖尿病患者的肝脏。接受移植的人称为接受者。这些胰岛开始在接受者体内制造和释放胰岛素。通常需要多次注射移植的胰岛细胞才能停止使用胰岛素。
研究人员希望胰岛移植能帮助1型糖尿病患者
- 改善他们的血糖水平;
- 降低或消除注射胰岛素的需要;
- 更好地识别低血糖症状,也称为低血糖症;
- 预防严重的低血糖症,即当一个人的血糖水平变得如此低以至于他或她需要另一个人的帮助来治疗低血糖症时。
全胰腺移植是另一种可以为1型糖尿病患者提供健康β细胞的手术。然而,胰腺移植是一项大手术,与胰岛移植相比,并发症的风险更大。
谁适合胰岛移植?
并非所有1型糖尿病患者都适合进行胰岛移植。某些1型糖尿病患者的血糖水平难以控制,经历过严重的低血糖症,并且没有意识到低血糖症(一种人无法感觉到或识别低血糖症状的危险状况),可能是候选者。
如果可能的益处(例如能够更好地达到血糖目标而不会出现低血糖等问题)大于风险(例如免疫抑制剂可能产生的副作用),医生会考虑进行胰岛移植。免疫抑制剂是接受者必须服用的药物,以防止其免疫系统攻击和破坏移植的胰岛。
患有1型糖尿病并且已经或计划进行肾移植以治疗肾衰竭的人可能是胰岛移植的候选者。胰岛移植可以在肾移植的同时或之后进行。肾移植受试者已经在服用免疫抑制剂以防止移植肾排斥反应。因此,胰岛移植并没有增加多少风险。
医生如何进行胰岛移植?
特殊酶用于从已故捐赠者的胰腺中去除胰岛。胰岛在实验室中被纯化和计数。平均而言,每个程序移植约400,000个胰岛。
移植接受者通常会在手术过程中接受局麻和镇静剂(帮助您放松的药物)。在某些情况下,接受者可能会接受全身麻醉。
胰岛移植输液过程包括通过接受者上腹部的一个小切口插入一根称为导管的细而柔韧的管子。放射科医师使用X射线和超声波引导导管进入肝脏的门静脉。胰岛通过导管缓慢注入并靠重力进入肝脏。或者,可以使用微创开放手术直接观察肝脏附近的静脉以插入导管。
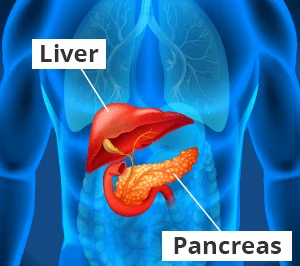
在接下来的2周内,新血管形成并将胰岛与接受者的血管连接起来。胰岛中的β细胞在移植后立即开始制造胰岛素并将其释放到血液中。
胰岛移植有什么好处?
收件人可能会看到以下好处
- 改善血糖水平;
- 减少或不需要注射胰岛素来控制糖尿病;
- 很少或没有严重低血糖发作;
- 提高对低血糖症的认识,这有助于预防严重低血糖症的发作。
研究还表明,胰岛移植可以预防或减缓糖尿病并发症的发展,例如心脏病、肾病以及神经或眼睛损伤。
胰岛移植有多成功?
由美国国立卫生研究院 (NIH) 赞助的临床胰岛移植联盟外部链接进行的3期临床试验研究了与胰岛移植相关的结果。3期试验在大量人群中测试新疗法,以确认疗法有效并监测副作用。这项由 NIH赞助的研究的参与者包括1型糖尿病患者,他们的血糖水平管理存在问题,例如严重的低血糖和低血糖无意识。
研究发现,胰岛移植1年后,每10名移植受试者中就有近9人的A1C水平低于7%,并且没有发生严重的低血糖症。许多糖尿病患者的A1C目标低于7%。大约一半的接受者不需要服用任何胰岛素。胰岛移植两年后,每10名接受者中约有7人的A1C水平低于7%,并且没有发生严重低血糖症,并且每10人中约有4人不需要胰岛素。
这项研究正在进行的研究还发现,胰岛移植受者在与糖尿病相关的生活质量方面有了显着改善,并且在移植后报告了更好的整体健康状况。即使是仍然需要服用胰岛素来控制糖尿病的移植接受者也经历了这些改善。
胰岛移植有哪些风险?
胰岛移植的风险包括
- 手术后出血、血块和疼痛;
- 移植的胰岛可能无法正常工作或停止工作的可能性;
- 抗排斥药物(也称为免疫抑制剂)的副作用如下所述;
- 针对供体细胞的抗体的发展,如果将来需要进行另一次移植,可能会更难找到合适的器官供体。
胰岛移植有多普遍?
胰岛移植不是1型糖尿病的常见治疗方法。在美国,胰岛移植被认为是一种实验性治疗。胰岛移植只能在获得FDA许可就此程序进行临床研究(涉及人的医学研究)的医院进行。随着更多的研究,胰岛移植可能成为未来更普遍的治疗方法。
协作胰岛移植登记处 (CITR) 报告称,1999年至2015年间,全球有1,086人因1型糖尿病接受了胰岛移植。CITR收集有关在北美、欧洲、澳大利亚和亚洲的研究中心进行的胰岛移植的信息。国家糖尿病、消化和肾脏疾病研究所建立并支持CITR。JDRF,前身为青少年糖尿病研究基金会,也帮助建立了CITR。
为什么胰岛移植没有更多地用于治疗1型糖尿病?
出于以下几个原因,胰岛移植不常用于治疗1型糖尿病:
胰岛移植被认为是一种实验性程序
在美国,胰岛移植被认为是一种实验性程序。在胰岛移植被批准用于治疗1型糖尿病之前,该程序只能通过临床试验用于研究目的。健康保险计划通常不包括实验程序的费用。
来自NIH支持的3期临床试验的信息正在与FDA共享,以提供证据来考虑胰岛移植是否可以被批准用于治疗某些1型糖尿病患者。
您可以在www.ClinicalTrials.gov上查看联邦政府资助、开放和招募的胰岛移植临床研究的筛选列表。您可以扩大或缩小列表以包括来自行业、大学和个人的临床研究;但是,NIH不会审查这些研究,也不能确保它们是安全的。在您参加临床研究之前,请始终与您的医疗保健提供者交谈。
胰岛移植受试者必须服用免疫抑制剂
胰岛移植受试者必须长期服用免疫抑制剂,而这些药物可能会引起严重的副作用。研究人员正在寻找无需长期免疫抑制剂即可预防胰岛排斥的方法。在一种称为封装的方法中,胰岛被一种材料包裹,可以保护它们免受受体免疫系统的攻击。
供体胰岛供不应求
每年只有少量供体胰腺可用于胰岛移植。根据器官采购和移植网络,2017年从已故捐献者身上回收了1,315个胰腺。许多捐赠的胰腺不适合胰岛分离。此外,一些供体胰岛可能在移植过程中受损或被破坏。
研究人员正在研究克服供体胰岛供应短缺的不同方法。例如,科学家正在研究从猪身上移植胰岛或从干细胞创建新的人类胰岛的方法。
胰岛移植是否用于治疗任何其他病症?
医生可能会对切除整个胰腺以治疗严重和慢性胰腺炎的患者进行不同类型的胰岛移植,称为胰岛自体移植。1型糖尿病患者不能接受胰岛自体移植。
在胰岛自体移植中,医生会切除患者的胰腺,从胰腺中取出胰岛,然后将胰岛移植到患者的肝脏中。目标是为身体提供足够的健康胰岛来制造胰岛素。患者在胰岛自体移植后不需要服用免疫抑制剂,因为他们接受的是来自自己身体的胰岛。
胰岛自体移植不被认为是实验性的。
最后,主要挑战之一是手术费用和一些监管问题,最近美国正在进行的讨论就证明了这一点。事实上,2022年4月15日,美国食品和药物管理局的细胞、组织和基因治疗咨询委员会投票赞成批准生物制品许可证申请,寻求将异体朗格汉斯胰岛推向市场,用于治疗成人 “脆性 “I型糖尿病,尽管强化胰岛素治疗,其症状仍未得到很好的控制。
美国食品和药物管理局对胰岛移植的认可增加了欧洲国家机构的名单,如瑞士联邦公共卫生局、英国国家卫生局、瑞典地方当局和地区、波兰和比利时卫生部以及最近法国国家卫生局(HAS)都批准将胰岛移植作为报销的标准护理程序。不幸的是,美国食品和药物管理局选择将胰岛作为一种生物制品,需要获得许可,这使得该程序在临床上的普遍实施非常具有挑战性。
细胞疗法治疗糖尿病的新视野
用于治疗糖尿病的细胞疗法领域正在迅速发展,一个激动人心的新时代已经开始(如图1所示)。在各种新的治疗方法中,干细胞疗法是一种能恢复正常胰岛功能并取代外源性胰岛素治疗的新疗法。干细胞疗法治疗1型糖尿病历经数十年的发展,在实验室水平和临床研究中均取得了一定的进展并有患者从中获益。
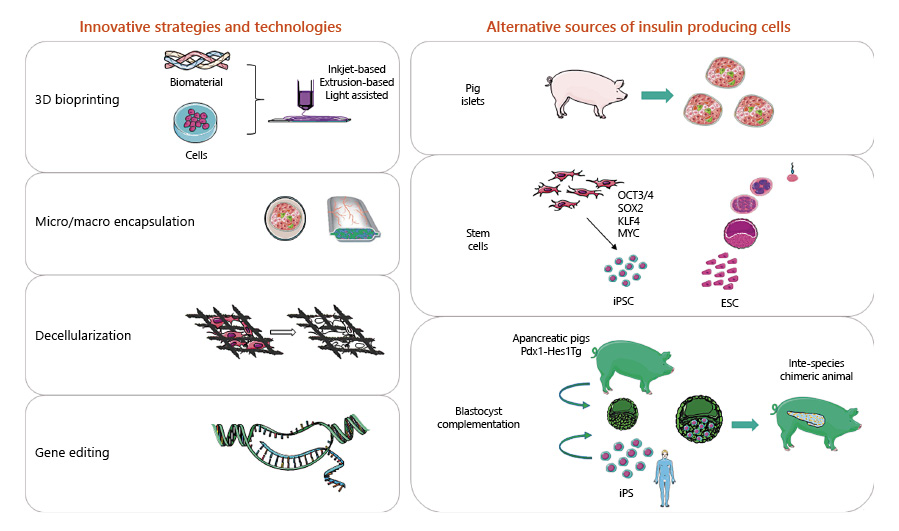
目前治疗用于研究1型糖尿病的干细胞主要有间充质干细胞、人类多能干细胞(包括胚胎干细胞和诱导多能干细胞),其中胚胎干细胞和诱导多能干细胞)是制造β细胞的最佳候选者,因为它们具有无限的分裂和分化潜力。多个实验室已经开发出将多能细胞分化为β细胞的有效方案,去年的巨大努力集中在开发具有一致效力和安全性的细胞产品,以供临床应用。
目前在ClinicalTrial.gov上注册了6项使用人类多能干细胞治疗1型糖尿病的临床试验:
3项正在招募中(NCT03163511;NCT04678557;NCT04786262),1项已完成(NCT03162926),1项应邀入组(NCT02939118) , 和一个活跃但未招募 (NCT02239354)。除NCT04786262外,所有这些试验均使用PEC-01细胞作为细胞产品。PEC-01细胞是一个混合细胞群,包含胰腺内胚层和多激素内分泌细胞,由称为CyT49的多能干细胞系分化。这些胰腺前体细胞在植入后完全致力于进一步分化为成熟的内分泌胰腺细胞,并首先在被假设可以防止免疫抑制需要的封装封闭装置 (PEC-Encap) 中对人体进行测试。
临床经验始于美国和加拿大2014年,将带有胰腺前体细胞的装置植入没有免疫抑制的1型糖尿病患者的皮下。首次临床经验证明了多能干细胞衍生产品的安全性(没有供体细胞的脱靶生长、与手术相关的轻微不良事件)和该策略的免疫保护功效(没有同种异体或自身免疫排斥的证据或致敏),但未能始终如一地维持长期的细胞存活,因为存在对设备组件的异物反应。出于这个原因,试验被暂停,目前从2021年2月开始使用新修改的封装系统重新启动。
从2017年开始,PEC-01细胞也在封装开放装置 (PEC-Direct) 中结合免疫抑制进行了测试。这第二次在北美和欧洲进行的临床经验首次证明,胰腺祖细胞在皮下植入后可以存活、植入、分化并成熟为人类胰岛样细胞,并且可以产生临床相关的内源性胰岛素通过葡萄糖反应性C肽水平的显着增加、范围内的时间增加和HbA1C的减少可见。
目前,欧洲Beta细胞疗法联盟(由VUB[比利时布鲁塞尔]、ViaCyte [美国加利福尼亚州圣地亚哥]、圣拉斐尔医院糖尿病研究所的临床、工业和研究团队组成)取得了有希望的临床结果Institute [意大利米兰]、雀巢健康科学研究所 [瑞士洛桑]、大学医学中心 [荷兰莱顿] 和Institut du Cerveau et de la Moelle Epiniere [法国巴黎]),它们在美国糖尿病协会的第81次虚拟科学会议,针对1名患者进行了为期9个月的植入PEC-Direct的研究。
数据显示刺激的C肽Cmax浓度从0.1ng/mL(基线)增加到0.8ng/mL(第39周),曲线下面积0–4 h从0.225(基线)增加到2.55ng×h/mL (第39周),表明细胞正在产生和分泌胰岛素。用于监测治疗性植入物的哨兵装置的组织学评估进一步表明植入成功。重要的是,患者在第42周时时间也从54%增加到88%,HbA1C从7.4%(基线)减少 0.8%到6.6%(第39周),这两个结果都表明血糖控制得到改善与治疗。在同一时间段内,该患者没有报告严重的AE。
此外,2021年12月,PEC-Direct临床试验的中期结果出现在两篇文章中:Cell Reports Medicine的一篇论文报道了17名在美国和加拿大植入PEC-Direct装置的患者。在植入后3至12个月的时间点,在从试验对象中移出的VC-02单元中,有63%观察到植入和胰岛素表达。在6/17名T1D受试者 (35.3%) 中观察到通过从头产生C肽捕获的葡萄糖反应性胰岛素分泌。
Cell Stem Cell论文报告了来自该试验最大参与地点、不列颠哥伦比亚大学和加拿大温哥华海岸卫生局的15名患者的研究结果。植入六个月后,患者的空腹和葡萄糖反应性C肽水平有所提高,并出现混合膳食刺激C肽的产生。此外,患者在范围内花费的时间增加了13%,其中一些能够减少他们的胰岛素需求。
在这两篇论文中,(i) 诱导和维持免疫抑制似乎可有效防止移植细胞的同种异体和自身免疫破坏,以及 (ii) VC-02产品似乎安全且耐受性良好,因为未观察到畸胎瘤形成,并且绝大多数轻度至中度的不良反应是由于外科手术风险和免疫抑制的副作用。这些初步数据强化了分化为胰腺内分泌细胞的多能干细胞可能成为T1D患者β细胞可再生来源的希望。
在公布这些初步结果的几周前,Viacyte已经向前迈出了一大步,宣布加拿大卫生部已批准该公司的新产品临床试验申请,该产品名为VCTX210,这是一种同种异体、基因编辑、免疫逃避、T1D的干细胞衍生细胞疗法。这项计划于2021年底开始招募患者的试验将面临在没有免疫抑制的情况下控制对移植物的免疫排斥的巨大挑战。
VX-880是2021年批准的第二种细胞产品,作为治疗1型糖尿病的研究性细胞疗法,允许进行第二代临床试验。VX-880由从多能干细胞中获得的完全分化的产生胰岛素的胰岛细胞组成。最近批准了一项1/2期、单臂、开放标签临床试验,用于患有低血糖意识受损和严重低血糖的T1D患者。这是一项连续的、多部分的临床试验,用于评估不同剂量VX-880的安全性和有效性。VX-880被注入门静脉,需要长期伴随免疫抑制治疗,以保护胰岛细胞免受免疫排斥。
延伸阅读:突破!治疗1型糖尿病!Vertex干细胞疗法获FDA批准临床
除了正在进行的临床经验外,其他商业或学术组织也宣布他们打算对功能性干细胞来源的胰岛进行临床试验。此时,保护移植的干细胞来源的β细胞免受免疫排斥的需求变得越来越重要。
结论
总之,目前的胰岛移植不能成为1型糖尿病的万能疗法。它代表了少数经过精心挑选的患者的临床选择,但它证明了可以通过细胞疗法有效替换糖尿病患者体内β细胞的原理。由此看来,胰岛移植将进一步促进糖尿病根治性研究,为糖尿病的下一代细胞治疗领域提供实施临床策略的知识和工具平台(如图2所示)。
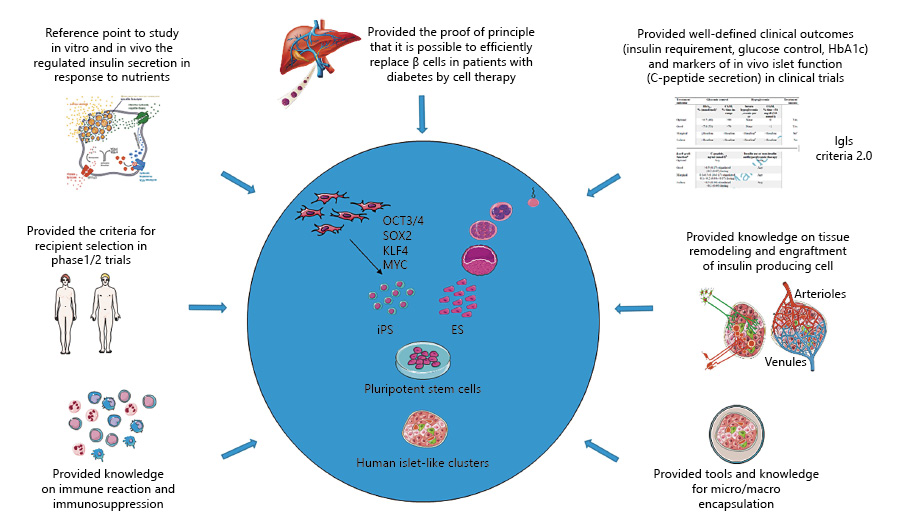
由于胰岛移植的经验,我们知道1型糖尿病是一种临床模型,用于测试基于干细胞的替代疗法。例如,与其他情况(即中枢神经系统疾病)不同,我们通过胰岛移植知道细胞不需要移植回原位即可发挥其功能。此外,明确的临床结果(胰岛素需求、葡萄糖控制、HbA1c)和体内功能标志物(C肽分泌)已经可用。彻底治愈糖尿病仍需要时间,但许多激动人心的新奇事物为我们指明了一条清晰的前进道路。
参考文献:
[1] Collaborative Islet Transplant Registry (CITR). CITR Tenth Annual Report. Collaborative Islet Transplant Registry website. https://citregistry.org/system/files/10th_AR.pdf External link (PDF, 7.9 MB) . Datafile Closure: January 6, 2017. Accessed September 18, 2018.
[2] Nyqvist D, Speier S, Rodriguez-Diaz R, et al. Donor islet endothelial cells in pancreatic islet revascularization. Diabetes. 2011:2571–2577.
[3] Shapiro AM, Pokrywczynska M, Ricordi C. Clinical pancreatic islet transplantation. Nature Reviews. Endocrinology. 2017;13(5):268–277.
[4] Hering BJ, Clarke WR, Bridges ND, et al. Phase 3 trial of transplantation of human islets in type 1 diabetes complicated by severe hypoglycemia. Diabetes Care. 2016;39(7):1230–1240.
[5] Foster ED, Bridges ND, Feurer ID, Eggerman TL, Hunsicker LG, Alejandro R; Clinical Islet Transplantation Consortium. Improved health-related quality of life in a phase 3 islet transplantation trial in type 1 diabetes complicated by severe hypoglycemia [published online March 21, 2018]. Diabetes Care. 2018. pii:dc171779. doi:10.2337/dc17-1779.
[6] U.S. Department of Health and Human Services. National data. Organ Procurement and Transplantation Network website. https://optn.transplant.hrsa.gov/data/ External link. Accessed October 12, 2018.
[7]:Valeria Sordi, Laura Monaco, Lorenzo Piemonti; Cell Therapy for Type 1 Diabetes: From Islet Transplantation to Stem Cells. Horm Res Paediatr 2022;
https://doi.org/10.1159/000526618
免责说明:本文 仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号