概述:干细胞疗法作为肝移植的替代方案,为晚期肝病病例提供了一条有前途的途径。临床研究正在进行中,以探索不同来源的干细胞治疗不同肝脏疾病的潜力。然而,由于当前研究的差异性,需要进一步验证以确保干细胞治疗的安全性和有效性。
为了为最佳干细胞治疗应用奠定坚实的基础,选择合适的干细胞来源、移植方案标准化和患者标准至关重要。这篇综述全面审查了有关干细胞来源、移植方法和患者选择的现有文献。此外,我们还讨论了新的策略,包括干细胞预处理、无细胞疗法、干细胞基因修饰以及肝脏类器官的使用,以解决当前干细胞疗法的局限性。然而,这些创新方法需要进一步验证。
一、背景
虽然肝脏可以再生,但各种原因造成的损伤可能导致肝硬化、肝衰竭或肝细胞癌 (HCC) 等疾病,占全球死亡率的3.5%。肝移植是治疗急性肝衰竭或终末期肝病的一种挽救生命的选择。然而,捐赠者和接受者之间日益扩大的差距需要替代疗法。由于肝细胞移植的局限性,例如增殖和可用性有限,基于干细胞的治疗成为一种有前途的方法。
干细胞具有自我更新和分化能力。胚胎干细胞(ESC)、间充质干细胞(MSC)和诱导多能干细胞(iPSC)是肝再生的潜在来源。过去20年来,大量临床研究探索了干细胞治疗肝病的方法,超越了终末期肝病的治疗。然而,研究异质性挑战了广泛的临床应用。我们的目的是讨论现有研究中的患者纳入标准、移植干细胞类型、移植方法和治疗效果评估。
迄今为止干细胞治疗肝病的临床移植手术
治疗肝病的干细胞来源
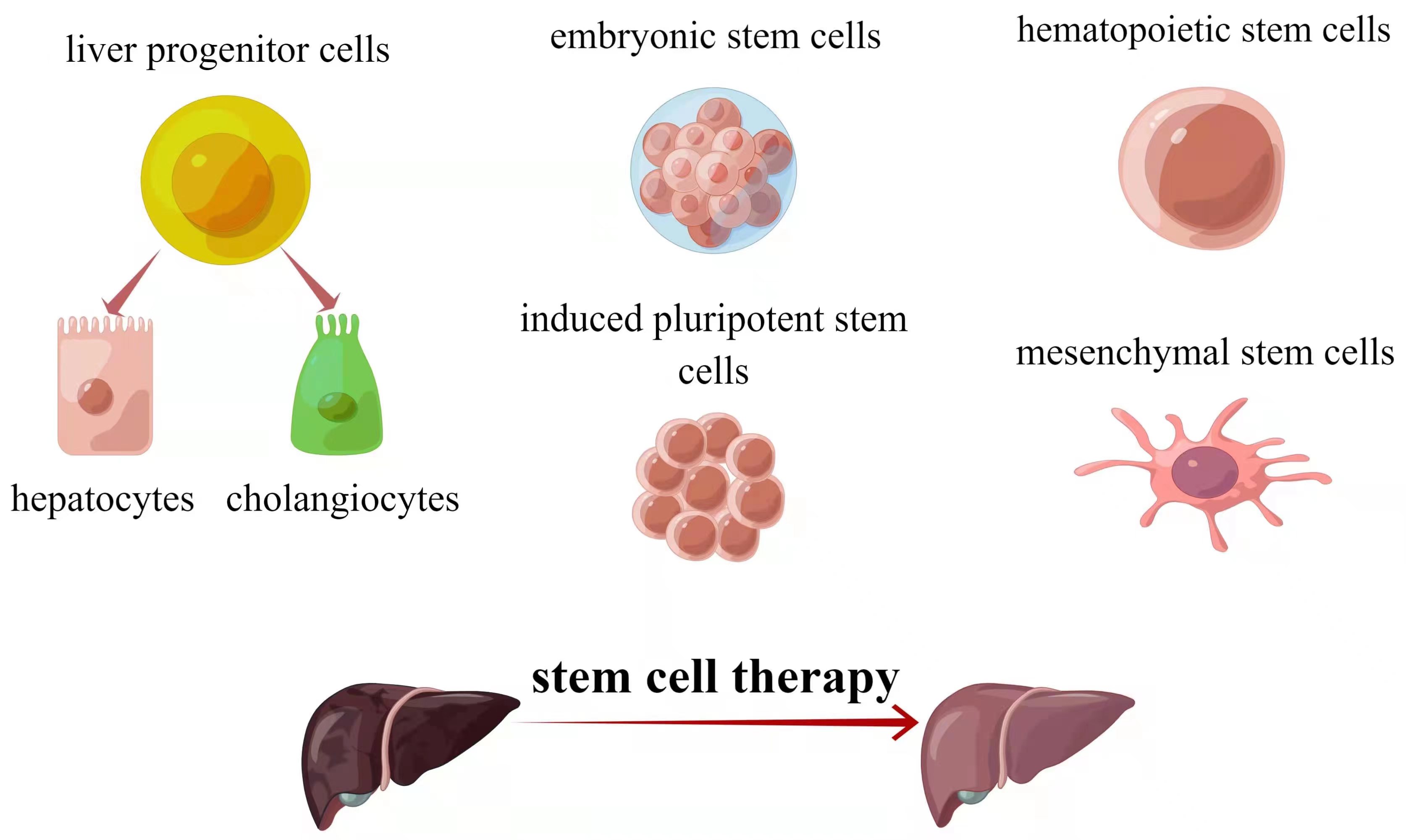
以细胞为基础的治疗方法有望成为移植或人工肝支持的替代方法。目前已发现三种干细胞类型–肝细胞、肝内干细胞和肝外干细胞–可用于肝脏再生(图1)。肝细胞移植始于1992年,对代谢性肝病有效。面临的挑战包括功能细胞有限和肝细胞易受冷冻损伤。
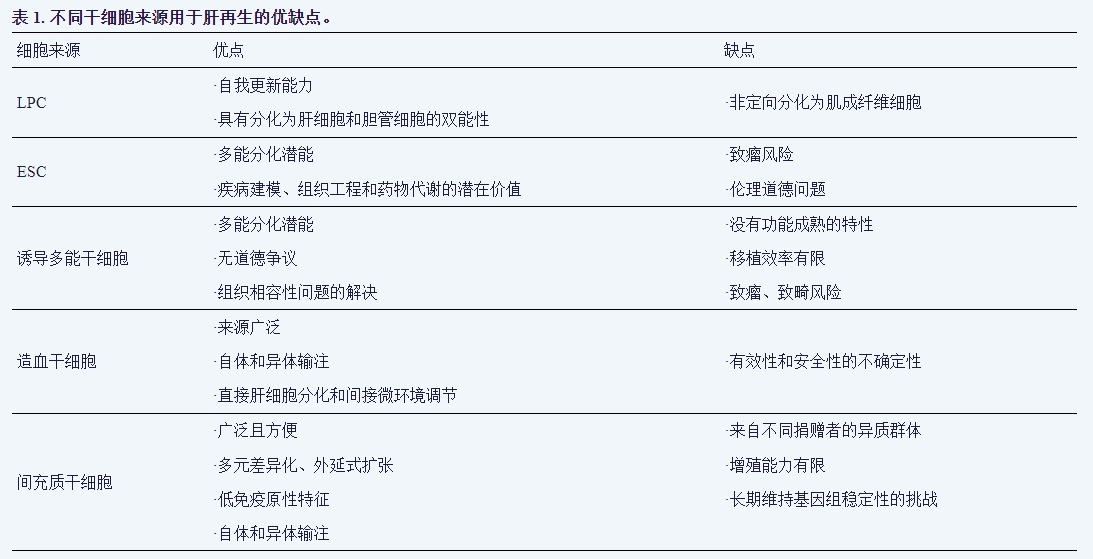
干细胞具有分化和增殖能力,可提供潜在的解决方案。肝内干细胞被称为肝祖细胞(LPCs),既可成为胆管细胞,也可成为肝细胞。肝外干细胞如胚胎干细胞(ESCs)、诱导多能干细胞(iPSCs)和成体干细胞(ASCs)也在探索之列。每种类型都有其优点和局限性。表1总结了用于肝脏再生的干细胞类型。
干细胞治疗肝病的类型
截至2024年3月5日,ClinicalTrials.gov列出了120项使用干细胞治疗肝病的临床研究,主要关注慢性肝衰竭急性期 (ACLF) 和失代偿性肝硬化。干细胞还在其他肝脏疾病中发挥治疗作用,包括代谢紊乱、自身免疫性疾病和遗传相关疾病(图2)。
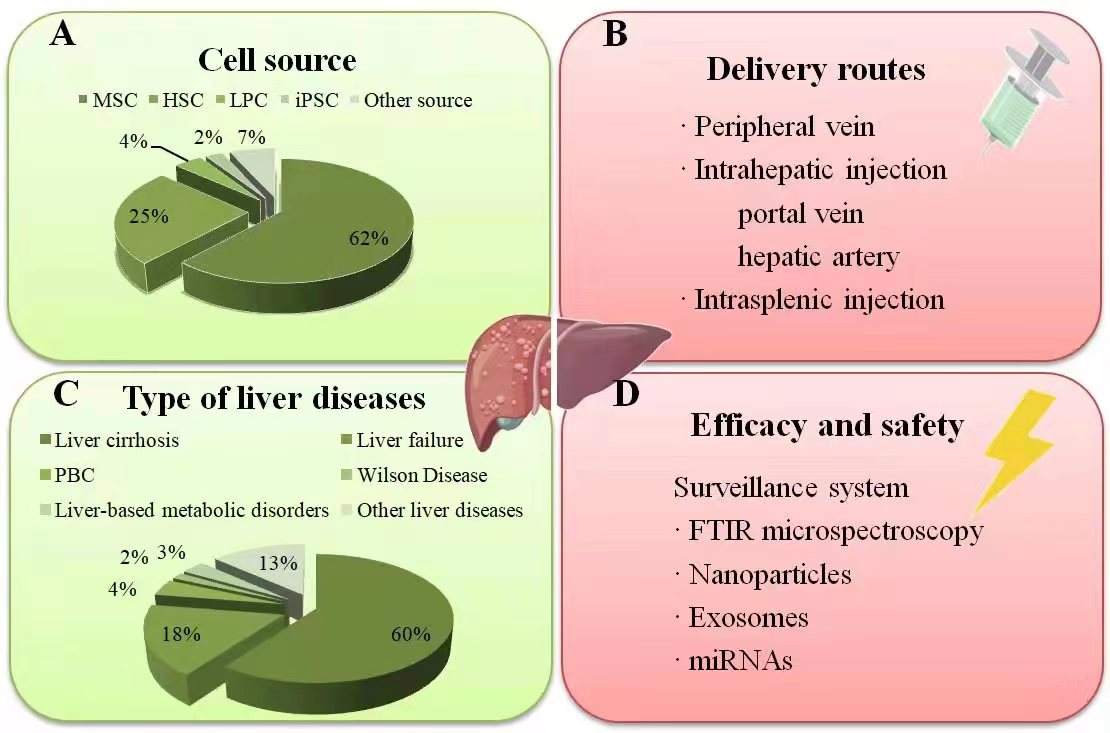
(A)临床肝脏治疗中应用的不同干细胞类型的百分比:MSC是最常用的类型,其次是HSC。
(B)注射途径主要经外周静脉注射,其次是肝动脉和门静脉,少数经脾内注射。
(C) 干细胞移植治疗各种肝病的百分比。
(D) 用于监测肝病干细胞植入相关功效和安全性的监测系统。
干细胞治疗肝硬化
肝硬化代表多种慢性肝病进展的晚期阶段。当肝脏因乙型/丙型肝炎感染、酗酒、脂质堆积和接触有毒物质等因素而受到损伤时,活化的肝星状细胞会产生过量的胶原蛋白和基质蛋白,最终导致肝纤维化。虽然早期纤维化具有可逆性,但肝硬化则相反,往往是不可逆的。
干细胞治疗的多种前瞻性机制已被提出用于肝硬化治疗。这些包括干细胞直接分化为功能性肝细胞、抑制肝星状细胞活化并诱导其凋亡、通过旁分泌作用调节炎症微环境以及释放营养剂以刺激现有肝细胞的再生。一项荟萃分析表明,间充质干细胞可以改善肝硬化患者的临床状态和实验室指标。这表明干细胞疗法可能是一种有效且安全的选择,特别是在肝硬化治疗的最初六个月内。
此外,辨别哪些患者最有可能从干细胞移植中受益也至关重要。据推测,干细胞治疗的疗效可能会根据肝硬化的根本原因而有所不同。据此,广泛的对照试验提供了证据支持采用间充质干细胞移植作为改善病毒性肝硬化和酒精性肝硬化肝功能的可行干预措施。尽管如此,一项排除病毒相关性肝硬化患者的试点研究并未观察到 MSC 治疗对肝硬化的广受追捧的治疗效果。
根据现有文献,被归类为Child-PughC级、年龄低于60岁、计划肝移植或与标准药物一起辅助使用的肝硬化病例被认为是干细胞治疗的合适候选者。相反,患有晚期肝硬化相关并发症(如复发性静脉曲张出血、中重度肝性脑病、出血倾向、HCC、持续感染或肝/门/脾血栓形成)的患者被认为不适合干细胞移植。然而,最佳的干细胞类型、理想的移植途径以及合适的注射频率和细胞剂量需要通过大规模随机对照试验进一步阐明。
干细胞治疗肝功能衰竭
肝衰竭是一种危及生命的综合征,以腹水、黄疸、出血倾向和肝性脑病为特征,死亡率很高。它分为急性肝衰竭(ALF)、慢性肝病ACLF和慢性肝衰竭(CLF)。肝细胞损失导致肝衰竭,这使得ACLF成为干细胞研究的另一个优先领域。
MSC的抗炎作用使其有望用于ACLF治疗。RCT系统评价和荟萃分析证明MSC疗法在改善ACLF和肝硬化病例的肝功能、白蛋白、凝血或MELD评分方面具有功效。亚组分析显示干细胞治疗对ACLF具有短期生存益处。大多数MSC临床试验处于I期或II期。人类肝脏类器官的进步,包括与芯片上器官灌注的集成,为ACLF中的功能性肝脏类器官带来了希望。
干细胞治疗自身免疫性肝病(AILD)
AILD包括一系列以免疫功能障碍为特征的慢性肝病,包括原发性硬化性胆管炎(PSC)、原发性胆汁性胆管炎(PBC)和自身免疫性肝炎(AIH)。AILD患者的治疗选择往往有限且预后不良,尤其是那些对初始药物治疗反应不足的患者。在这种情况下,干细胞疗法是AILD的一种潜在有效的替代疗法。
目前,临床研究主要针对PBC。一项初步研究纳入了7例对熊去氧胆酸 (UDCA) 反应不完全的PBC病例。这些患者每月接受培养的脐带来源的MSC输注(0.5×106细胞/kg)3次。在48周的随访中,所有患者都能很好地耐受治疗,没有明显的副作用,并且大多数患者都获得了缓解。另外,血清γ-谷氨酰转移酶(GGT)和碱性磷酸酶(ALP)水平显着下降。
对于AIH和PSC,干细胞疗法的应用仅限于动物模型和病例报告,这强调需要进一步的实验和临床研究来确定疗效和安全性。
干细胞治疗威尔逊病(WD)
WD是一种以ATP7B缺乏为特征的常染色体隐性遗传病,ATP7B是一种主要在肝细胞中表达的铜 (Cu) 转运 ATP酶。这种缺乏会导致铜积累,引起不同严重程度的肝脏、神经和精神症状。WD患者的终生治疗通常可以维持铜平衡。然而,目前的药物疗法并不能治愈并且具有严重的副作用。肝移植还面临着供体短缺和神经系统失控患者的挑战。因此,干细胞疗法探索恢复肝胆铜排泄和改变WD进展的潜在治疗方法。
目前,只有一项随机对照试验在60名WD患者中比较了BM-MSC移植加青霉胺与单独青霉胺的比较。青霉胺是一种平衡铜摄入和排泄的螯合剂,具有严重的副作用并且不能治愈WD。有趣的是,该研究表明BM-MSC 联合青霉胺可积极影响WD相关的肝纤维化,且MSC治疗的不良反应很少。
干细胞治疗肝脏代谢紊乱
干细胞疗法有望成为肝脏代谢疾病的一种治疗选择。研究表明,移植相当于患者肝脏约1/10的肝细胞质量足以使酶缺乏正常化。
先天性肝脏代谢缺陷包括一组以参与各种代谢途径的单一酶缺乏为特征的疾病。这些缺陷会导致肝功能受损和远处器官功能障碍。这些情况通常在新生儿期出现。先天性肝脏代谢缺陷中最显着的两种疾病是克里格勒-纳贾尔 (CN) 综合征和尿素循环缺陷 (UCD)。
目前,这些疾病尚无有效的治疗方法,导致大约10-50%的受影响儿童需要肝移植。干细胞有可能恢复受影响个体的肝酶活性。与此相一致,异源人类成人LPC(HHALPC)的安全性和有效性在一项涉及14名UCD 和6名CN儿科患者的I/II期、多臂、开放标签前瞻性研究中得到初步证实。随后的II期临床研究正在进行中,以进一步探索HHALPC的用途。值得注意的是,HHALPC是通过门静脉内输注施用的;然而,临床医生需要警惕门静脉血栓形成的可能风险。
另一项涉及6个CN和5个UCD的部分随机I/II期研究显示,肝素和比伐卢定的组合具有较高的安全性,并且可以限制MSC输注引起的血栓形成至亚临床症状。这种方法表明在移植过程中抑制MSC促凝血活性方面取得了重大进展。
干细胞移植途径
干细胞治疗有多种途径,例如外周静脉给药、肝内注射(通过肝动脉或门静脉)和脾内注射。外周静脉输注因其给药方便且创伤小而仍然很重要。然而,值得注意的是,这种全身输送方法可能会导致肺部细胞过度积累,而免疫细胞可能会减轻这种现象。
另一方面,肝动脉输注是第二常见的移植途径,据信与外周静脉相比显着有效。这是由于减轻了循环中的细胞磨损,同时促进细胞归巢到受损的肝脏。然而,这种侵入性手术存在血栓形成和门静脉高压出血的风险。门静脉内注射是肝内注射的可行替代方案,可以更快地植入并防止脱靶积累。然而,在选择这条路线之前,应彻底评估患者的病情和潜在风险,如门静脉血栓形成。脾内注射虽然在技术上比肝内注射简单,但会带来额外的并发症,需要仔细考虑。
干细胞移植的数量和频率
目前的文献中移植干细胞的最佳数量和频率仍不确定。在大多数临床试验中,干细胞移植是基于患者的体重,这似乎是一种合理的方法。关于干细胞治疗慢性肝病的频率,尚缺乏共识。一些研究表明多次输注可以增强和维持疗效,而其他研究表明两次注射和单次注射之间没有显着差异。
最近的荟萃分析表明,多次注射可以有利地降低死亡率和MELD评分,而单次注射则有利于改善白蛋白 (ALB) 和总胆红素 (TBIL) 水平。此外,一些研究人员提出,延长初始注射和后续注射之间的间隔可能会增强干细胞治疗的长期治疗效果。
新的改进策略
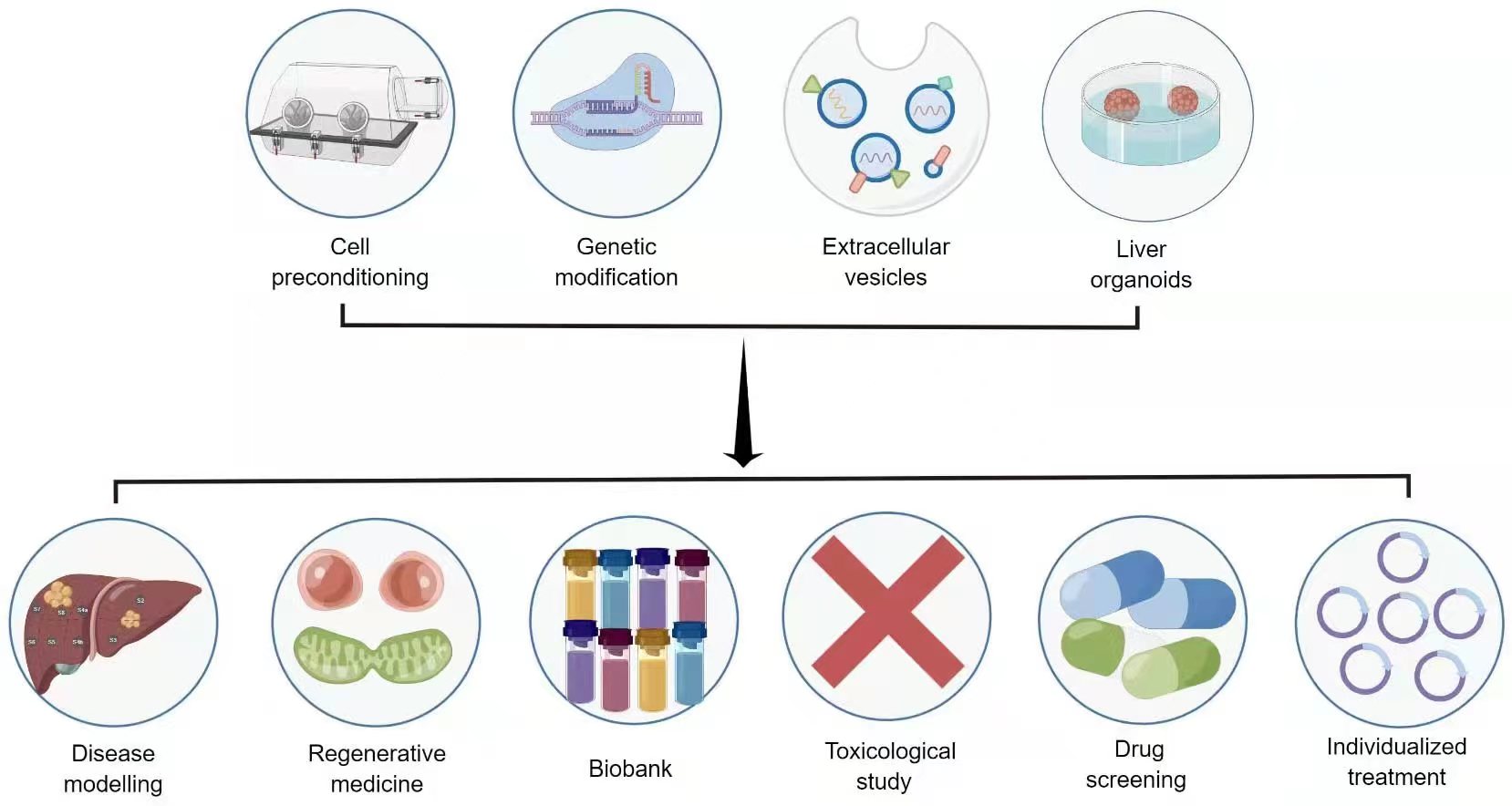
虽然干细胞疗法在肝脏再生医学中具有变革潜力,但在临床转化应用之前需要解决一些复杂的问题。这些挑战包括细胞活力差、细胞间通讯不足、分化有限、迁移欠佳和细胞外基质 (ECM) 生成量低。因此,旨在增强干细胞功效的生物医学技术正在接受严格的研究。这些包括预处理、干细胞来源的外泌体、基因修饰和三维培养(图3)。
结论
根据现有的临床前和临床研究,干细胞疗法成为解决肝脏疾病的一种可行的替代方案。然而,由于现有数据的有限性和多样性,必须对潜在的治疗机制和全面的随机对照试验进行更多探索。这项工作将有助于确定最佳干细胞类型、适当的剂量和注射频率以及合适的给药途径。认识到干细胞治疗的固有限制,干细胞预处理、基因工程干细胞、无细胞疗法和肝类器官的进步可能预示着肝脏再生的新时代。
参考资料:Jing Wang, Qun Li, Wenbo Li, Nahum Méndez-Sánchez, Xiaofeng Liu, Xingshun Qi. Stem Cell Therapy for Liver Diseases: Current Perspectives. Front. Biosci. (Landmark Ed) 2023, 28(12), 359.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请及时跟本公众号联系,我们将在第一时间处理。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号