间充质干细胞(MSC)是多能干细胞,其旁分泌和免疫调节潜力使其成为中枢神经系统(CNS)再生的有希望的候选者。大量研究表明,间充质干细胞可以促进免疫调节、抗细胞凋亡和轴突重新延伸,从而恢复功能性神经回路。因此,间充质干细胞的治疗效果已被评估用于各种中枢神经系统疾病,包括脊髓损伤、脑缺血和神经退行性疾病。
介绍:损伤和神经退行性疾病通常会导致神经元损失和中枢神经系统 (CNS) 轴突损伤。成熟的哺乳动物中枢神经系统中的神经元无法自发再生。人们付出了巨大的努力来认识中枢神经系统再生衰竭的机制,但仍然缺乏完整的理解。广泛的再生策略,特别是通过增加神经元存活和轴突重新延伸,已取得了不同程度的成功。
间充质干细胞(MSC)是研究最广泛的多能干细胞之一,存在于多个器官中并且可以源自各种组织。它们分化为几乎任何终末期谱系细胞的能力和强大的旁分泌作用使间充质干细胞成为内源性再生的有希望的候选者。此外,间充质干细胞可以通过全身和局部递送途径安全有效地移植。
大量研究表明,间充质干细胞移植可以调节神经元生长和轴突重新延伸,并改善中枢神经系统损伤或退化后的神经系统功能。在这篇综述中,我们讨论了间充质干细胞治疗神经系统疾病作用及其潜在的相关机制[1]。
间充质干细胞三大作用机制助力修复神经系统损伤
一、间充质干细胞的免疫调节作用
间充质干细胞的抗炎作用主要是通过分泌各种酶和可溶性因子及其对T淋巴细胞的旁分泌作用来实现的,包括幼稚CD4+T细胞、Th1细胞、Th2细胞、Th17细胞、CD4+FoxP3+调节性T细胞细胞 (Treg) 和CD8+T细胞。它们还具有多种抗炎作用,包括影响B细胞的趋化特性、抑制白细胞介素2 (IL-2) 诱导的自然杀伤 (NK) 细胞活化,下调 NK激活受体,并影响骨髓细胞的功能,如单核细胞、树突状细胞和巨噬细胞(图1)。
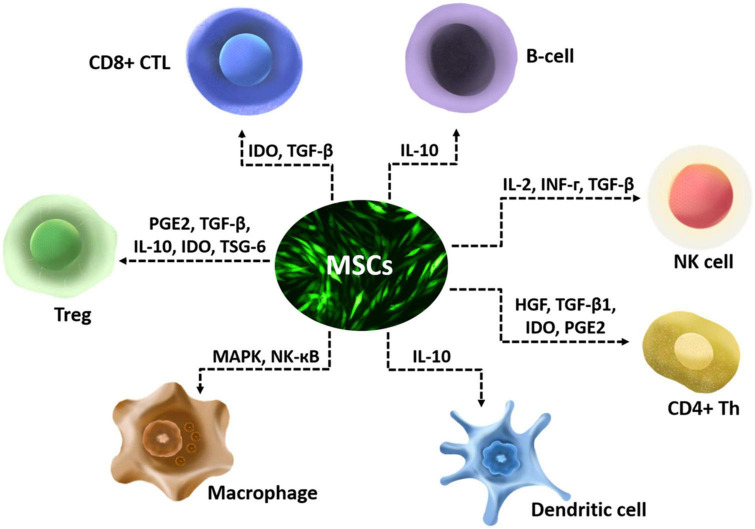
MSC通过破坏免疫细胞的激活、增殖、成熟、细胞溶解活性、细胞因子产生或抗体产生来调节免疫细胞。中枢神经系统及其屏障充满了先天性和适应性免疫细胞,它们在疾病中与神经胶质细胞相互作用。免疫细胞和神经胶质细胞之间的相互作用已被证明在中枢神经系统的再生能力中发挥着关键作用。间充质干细胞对免疫细胞的作用可能参与免疫细胞与神经胶质细胞的相互作用,进而影响中枢神经系统的再生。
大量数据发现,间充质干细胞可分泌多种可溶性分子,包括肝细胞生长因子(HGF)、转化生长因子-β1(TGF-β1)、吲哚胺吡咯2,3-双加氧酶(IDO)、前列腺素E2(PGE2)、白细胞介素等。(IL)-13、IL-10、IL-12p70、IL-17E和IL-27发挥抗炎潜力 。从BM、AT、牙髓、沃顿胶 (WJ) 和胎盘旁分泌抗炎因子(例如TGF-β)中分离的人MSC,可促进神经保护作用。促炎细胞因子、基质刚性、葡萄糖水平和缺氧可以增加MSC产生的TGF-β。另一方面,TGF-β也已被证明通过MSC中的SMAD2/3磷酸化发出信号来调节MSC本身的生物学。通过分泌生物活性和营养因子的能力,间充质干细胞对细胞再生和新组织生长产生显着影响。
二、间充质干细胞的抗凋亡作用
体外研究表明,BM-MSC可以调节肌萎缩侧索硬化症 (ALS) 中神经元和胶质细胞对细胞凋亡的反应 。其他研究还表明,脑内、静脉内或脑室内MSCs移植可以改善内源性神经细胞的凋亡。浸润的炎症相关免疫细胞释放大量活性氧,导致受伤区域的程序性细胞死亡。MSCs可能抑制氧化应激并增加脑中抗凋亡Bcl-2基因的表达。既往研究表明,miRNA包括miR-134、miR-138-5p、miR132-3p、miR-21-3p和miR-22-3p在这些MSC介导的脑中抗凋亡作用中发挥重要作用。
三、间充质干细胞的轴突再延伸效应
损伤后轴突再生被定义为轴突再生和随后损伤区域的神经支配,从而导致中枢神经系统功能的恢复。轴突再延伸被定义为轴突长时间的再生,长距离进行从头生长以达到其目标。人们普遍认为,来自受损区域周围外部环境的许多外在因素限制了轴突的重新延伸,例如硫酸软骨素蛋白多糖(CSPG)、髓磷脂相关糖蛋白(MAG)、少突胶质细胞髓鞘糖蛋白和Nogo-A。阻止这些抑制信号被认为是促进轴突重新延伸的一种有前途的方法。
间充质干细胞已被证明可以帮助神经突克服Nogo-A、MAG和CSPG的抑制作用。在MSC/神经元共培养中,MSC相对于Nogo-A和 MAG 促进脊髓神经元粘附和神经突延伸。除了抑制外在因素外,MSC还为HGF、表皮生长因子 (EGF)、神经营养蛋白-3 (NT-3) 和GDNF重建功能性局部回路提供了有利的微环境。
间充质干细胞治疗脊髓损伤
脊髓损伤会导致神经组织立即丧失,随后受伤脊髓节段以下的感觉和运动功能会出现永久性缺陷。SCI常见的有前景的实验疗法包括神经营养因子、针对抑制分子的酶和抗体、活化的巨噬细胞、桥接支架和干细胞移植。基于干细胞的再生医学已成为治疗SCI的一种新的有前景的治疗方法。间充质干细胞具有创造修复环境的潜力,这是探索间充质干细胞用于神经系统再生医学的主要动机。
早在2021年,耶鲁大学和日本札幌医科大学的研究者在国际期刊《Clinical Neurology And Neurosurgery》共同发布了一项研究成果。在此项试验中科研人员利用干细胞修复脊髓损伤,旨在探究干细胞的可行性、安全性与有效性。

招募的13位脊髓损伤患者在接受自体间充质干细胞治疗后,有12名患者在6个月后神经功能得到明显改善,并且超过一般患者关键技能(如走路和用手)有了实质性改善。该试验证明:间充质干细胞治疗脊髓损伤安全、有效。为脊髓损伤患者带来了新希望。
间充质干细胞干细胞治疗脑缺血
缺血性中风会引起广泛的神经炎症反应,这似乎是脑损伤扩散的原因。然而,旨在使用细胞抑制剂或介质减少缺血性中风后免疫反应的实验疗法尚未成功。在这种情况下,使用干细胞的新治疗策略已成为一种有前途的工具。最常用的干细胞是MSC,因为它们具有强大的营养能力。间充质干细胞潜在治疗活性的可能机制包括神经保护、免疫调节以及中风中神经发生、突触发生、星形细胞发生、少突胶质细胞发生和血管发生的激活。目前的研究表明间充质干细胞发挥的有益作用主要与分化和免疫调节机制有关。
2016年,国际期刊杂志《HHS Author Manuscripts》发表了一篇移植改良骨髓间充质干细胞治疗中风的临床结果,加利福尼亚州斯坦福大学医学院和斯坦福医疗保健中心神经外科发现中风患者的临床结果(欧洲中风量表、美国国立卫生研究院中风量表和Fugl-Meyer总分)有所改善。

与此同时,2019年,美国中风杂志发表了一项静脉注射同种异体间充质干细胞治疗慢性中风的安全性和初步疗效的I/II期研究结果,报道称,在这项随机、安慰剂对照研究中,慢性中风患者静脉输注同种异体间充质干细胞表明行为有所改善。

间充质干细胞治疗神经退行性疾病
中枢神经系统疾病的患病率不断上升,归因于神经退行性疾病,包括阿尔茨海默病 (AD)、帕金森病 (PD)、亨廷顿病 (HD)、肌萎缩侧索硬化症 (ALS)、多发性硬化症 (MS) 和多系统萎缩症 (MSA) )。此类疾病的一个共同特征是进行性神经元死亡,导致神经功能障碍。尽管近年来我们对神经退行性疾病病理学的认识有所提高,但尚未实现精确可靠的治疗方法。目前常见的治疗方法只是缓解症状,并不影响这些疾病的主要病理特征。间充质干细胞在细胞治疗方面具有巨大的潜力,因为它们可以分化为神经命运并分泌多种因子,这些因子能够促进神经保护或再生机制。此外,移植后,间充质干细胞具有归巢神经损伤的能力,这意味着它们有可能用作治疗药物给药的载体。
间充质干细胞治疗阿尔茨海默病:2018年3月初,根据日本再生医学安全法案,日本福冈三一诊所使用AstroStem治疗AD的安全性和有效性获得了日本九州认证专业委员会的批准,认证结果同时递交给了日本厚生劳动省九州分局,并于2018年4月11日正式获批。2018年4月12日起,该诊所开始使用AstroStem治疗AD,目前已经开始对3例韩国AD患者进行首次细胞治疗,方案仍是这些患者在2h内分别注射2亿个细胞,未来他们将每2周接受1次治疗,总共治疗10次,目前试验尚在进行之中。
异体间充质干细胞治疗老年阿尔茨海默病的临床应用也有报道。此前,美国Longeveron生物制药公司,宣布自2016年10月至2020年9月招募33例50~80岁的AD患者参与Ⅰ期临床试验,以评估其骨髓异体MSCs产品对老年AD患者治疗的安全性和有效性,这项随机、安慰剂对照和双盲的临床试验,将在佛罗里达州迈阿密大学米勒医学院、迈阿密犹太卫生系统和大脑研究所进行。
Longeveron公司的异体MSCs产品来源于年轻健康供体的骨髓,对比从老年AD患者自体脂肪中提取的MSCs,年轻健康供者中获得的高质量的干细胞,很可能具有治疗效果上的优势。根据剂量分为2组,一组接受2×107个细胞的外周静脉注射,另一组接受1×108个细胞外周静脉注射。该项目已在ClinicalTrail上注册,目前还在进行中。
间充质干细胞治疗帕金森病:2018年6月,中科院院士科研团队在猴模型中测试了脐带来源间充质干细胞治疗帕金森病的安全性和有效性,展示了长达2年的评价数据,表明干细胞分化的神经细胞相对安全,且有明显效果。为我国首项基于干细胞的I/II期帕金森治疗临床研究提供了临床前数据支持。

2020年,美国、西班牙科学家合作,研究人员将间充质干细胞回输到两名帕金森病患者的面部组织中,发现可以持续减少患者的运动和非运动症状,降低药物剂量,帮助两位帕金森患者缓解了病情。该研究被发表在临床神经科学杂志《Journal of Clinical Neuroscience》上。
间充质干细胞治疗渐冻症:以色列研究团队开展自体骨髓MSC治疗渐冻症的临床研究,19例患者接受MSC鞘内注射,9名患者同时接受1次静脉注射,前6个月的观察中ALSFRS平均分数保持稳定,在MSC治疗后Treg细胞的数量短期内有所增加。
该团队继续开展1和2期临床研究,其中1/2期有12名患者和2a期有14名患者(20-75岁),经过肌肉注射联合鞘内注射MSC,大部分患者自我感觉改善良好,根据肺活量(FVC)和ALSFRS-R评分,这些患者治疗后6个月在疾病进展恶化速率方面至少有25%的改善。
基于MSC的治疗是一种安全可行的技术。由于临床前和临床研究已经证明间充质干细胞治疗神经退行性疾病的有效性,许多研究开始关注增强疗效的方法。
其他中枢神经系统疾病
尽管间充质干细胞治疗中枢神经系统疾病的临床应用目前仍处于起步阶段,但间充质干细胞的研究在过去十年中迅速扩大。除了神经退行性疾病、脑缺血和脊髓损伤之外,大量动物模型研究也证明了间充质干细胞治疗癫痫方面的作用。在癫痫大鼠模型中,BM-MSC可以通过抑制神经元细胞死亡和异常苔藓纤维发芽来减少癫痫发生。UCB-MSCs可能会增强GABA神经递质水平并改善戊四唑诱导的大鼠慢性癫痫的氧化应激损伤。
此外,在一期开放标签研究中,间充质干细胞可以成为抗癫痫药物耐药性癫痫患者细胞治疗的安全且有前途的候选者。为了提高MSC在癫痫小鼠模型中的治疗效果,已使用基因工程MSC,例如IL-13工程MSC,其显示出增强的神经保护和疾病缓解作用。
增强间充质干细胞治疗效果的方法
尽管间充质干细胞是中枢神经系统再生的有希望的候选者,但低治疗效果限制了其临床应用。不同的培养条件可能会导致MSC的存活、归巢和关键功能特征发生改变。
马德里加尔等人发现低氧条件下的细胞培养通过增加HGF、TGF-b、VEGF、TSG-6的分泌对MSC的治疗特性具有潜在影响,这对中枢神经系统再生很重要。
其他人证明促炎刺激和三维生长刺激MSC的营养因子分泌。显然,培养条件将极大地影响间充质干细胞的治疗效果。除了培养基之外,开发的治疗策略也可以增强间充质干细胞的治疗效果,例如递送途径和时机。尽管对于间充质干细胞的最佳输送途径尚未达成共识,但脑室内移植可能是最有效的。
通过回顾之前的临床前和临床研究,Park等人发现,与静脉内和实质内途径相比,间充质干细胞的脑室内移植可能与中枢神经系统再生的内源性增强有关。脑室内移植的间充质干细胞以时间依赖性方式减轻脑损伤。在脑室内出血大鼠模型诱导后2至7天给药时,显示出显着的神经保护作用。
结论
越来越多的证据表明间充质干细胞可以成为促进中枢神经系统再生和功能恢复的潜在疗法。间充质干细胞的治疗作用极其复杂。证明它们在神经元存活、轴突重新延伸、突触重新形成和髓鞘再生过程中与其他细胞的确切相互作用可能有助于研究人员优化基于间充质干细胞的疗法的效果。间充质干细胞的最佳条件培养、输送途径和时机可能是提高治疗效果的有前途的策略。
总之,研究中枢神经系统中的间充质干细胞可以深入了解中枢神经系统再生和修复的确切机制,有助于优化基于细胞的治疗。
参考资料:[1]:Li M, Chen H, Zhu M. Mesenchymal stem cells for regenerative medicine in central nervous system. Front Neurosci. 2022 Dec 13;16:1068114. doi: 10.3389/fnins.2022.1068114. PMID: 36583105; PMCID: PMC9793714.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号