现代研究表明,间充质干细胞 (MSCs) 静脉注射后,可以穿过血脑屏障 (BBB),从而产生各种再生效应。
血脑屏障 (BBB)对于大脑健康至关重要,它是控制物质进入大脑的守门人。
最近的研究结果表明,某些细胞,包括干细胞,可以跨越这一障碍,为治疗神经系统疾病开辟了新的可能性。
本文探讨了什么是血脑屏障,血脑屏障的组成部分以及其的复杂性、保护功能以及间充质干细胞跨越血脑屏障改变神经治疗策略的革命性潜力。
什么是血脑屏障
血脑屏障(BBB)是大脑和脊髓周围的一个重要保护层。它调节物质进出大脑。这些细胞由大脑血管内壁的脑内皮细胞组成,它们与相邻细胞形成紧密连接,称为连接粘附分子,从而形成一道坚固的屏障。
BBB的组成部分和功能
- 脑内皮细胞:形成BBB的主要结构。
- 紧密连接:细胞之间的这些连接确保了强大的屏障。
- 选择性通透性:控制哪些物质可以进入或离开大脑。
血脑屏障的组成部分
脑毛细血管内皮细胞与营养调节:脑毛细血管内皮细胞是血脑屏障的重要组成部分。它们通过选择性地允许葡萄糖和氨基酸等必需营养物质通过,同时阻止有害物质通过,帮助维持脑代谢并支持神经元功能。它们还调节脑血流,这对于向大脑提供氧气和营养至关重要。
血管内皮生长因子和血脑屏障形成:血管内皮生长因子 (VEGF) 是血脑屏障形成和功能的关键因素。这种蛋白质有助于创建和维持脑毛细血管内皮,这对于血脑屏障的屏障功能至关重要。血脑屏障还能阻止大多数免疫细胞(如白细胞和T细胞)进入大脑,从而有助于保护神经组织免受炎症和损伤。
脑室周围器官和血脑屏障的薄弱点:然而,大脑中有一些区域,被称为脑室周围器官,这里的血脑屏障较弱,某些物质更容易进入。例如,脂溶性分子和脂溶性分子可以通过血脑屏障,而其他物质,如必需氨基酸,则使用独特的运输系统穿过血脑屏障。
脑脊液屏障和大脑支持:脑脊液 (CSF) 是血脑屏障的另一个重要组成部分。它包围着大脑和脊髓,提供结构支撑并帮助清除废物。脑脊液屏障由脑室内壁的上皮细胞形成,在脑脊液和循环血液之间形成隔离屏障。
BBB功能紊乱及其对大脑健康的影响:在某些情况下,如脑肿瘤或缺血性中风,血脑屏障的功能可能会受到干扰,导致血脑屏障通透性增加。这会使血液中的物质进入大脑,可能对脑细胞造成伤害并影响大脑功能。保持血脑屏障的完整性对于整体大脑健康和神经系统的正常运作至关重要。
血脑屏障对大脑健康的重要性
血脑屏障(BBB)是中枢神经系统的重要组成部分,在保护大脑和维持大脑健康方面发挥着至关重要的作用。它是由脑毛细血管、神经胶质细胞、膜内蛋白和细胞连接组成的复杂血管器官,控制大脑对营养物质的吸收并排除有害物质。
血脑屏障确保只有小分子和脂肪酸等必需物质才能进入大脑,而肿瘤坏死因子和活性氧等有害元素则被挡在外面。这道屏障由脑血管腔表面的一层连续细胞构成,并由神经胶质细胞等邻近细胞支撑。
正常的血脑屏障功能对于大脑发育、神经元兴奋性和神经组织的整体健康至关重要。血脑屏障功能障碍会导致各种问题,包括炎症和脑损伤。因此,了解血脑屏障的细胞生理学及其与血管系统的相互作用对于开发治疗和预防脑部疾病的疗法至关重要。
对血脑屏障的研究为大脑健康提供了宝贵的见解,而继续研究这一领域,例如研究动物大脑和研究松果体在心血管调节中的作用,将进一步加深我们对这一复杂而重要的屏障的理解。通过保持血脑屏障的完整性,我们可以帮助确保大脑正常运作并促进整体大脑健康。
血脑屏障对干细胞治疗的影响
血脑屏障(BBB)是大脑中的一个重要结构,由复杂的血管和细胞网络组成。它起着保护盾的作用,控制物质在血流和中枢神经系统(CNS)之间的通过。
这种屏障对于维持脑稳态至关重要,并对神经系统疾病干细胞疗法的疗效起着至关重要的作用。
影响干细胞跨血脑屏障传递的因素
屏障功能:血脑屏障可以阻止某些干细胞进入中枢神经系统,从而影响其治疗潜力。一项研究表明,在短暂性全脑缺血后早期注射的人类真皮衍生间充质干细胞无法穿过受损的血脑屏障。
给药时机:干细胞疗法的成功与否取决于细胞给药时间与BBB损伤的关系。颞叶癫痫模型的研究表明,在癫痫持续状态导致BBB损伤后,选择恰当的时机给药DPSC或BM-MSC可增强CNS归巢,减少神经退化和其他并发症。
细胞外囊泡的作用:间充质干细胞衍生的细胞外囊泡(如外泌体)可以穿过血脑屏障。这些囊泡具有治疗前景,可通过静脉或鼻腔内途径输送,避免侵入性神经外科手术。
BBB显著影响干细胞在治疗神经系统疾病中的输送和有效性。彻底了解BBB的功能和干细胞给药的战略时机是优化其治疗潜力的关键。
间充质干细胞穿过血脑屏障
间充质干细胞 (MSCs)经静脉注射后,已显示出穿过血脑屏障 (BBB)的能力。这些细胞具有使其能够迁移到炎症区域的固有特性。
MSC释放各种分泌物,促进神经再生并缓解这些部位的疼痛。包括 Kim等人的研究在内的研究已证实,静脉注射的MSC可以穿过BBB,阿尔茨海默病小鼠模型证明了这一点,证明了它们在大脑中具有再生作用的潜力MSC和BBB研究。
间充质干细胞的关键属性
炎症归巢:MSCs自然迁移到炎症部位。
分泌物释放:它们分泌有助于神经再生和缓解疼痛的物质。
穿越BBB能力:静脉注射MSCs可使其穿过BBB。
间充质干细胞已证实具有穿过血脑屏障的能力,在各种动物模型中显示出缓解神经系统疾病的潜力。然而,MSCs穿透血脑屏障的成功率可能因具体情况和给药时间而异。
进一步研究数据
间充质干细胞(MSCs)穿越血脑屏障(BBB)的能力日益得到认可,为治疗神经系统疾病提供了新途径。
值得注意的是,在颞叶癫痫(TLE)动物模型中,牙髓干细胞(DPSCs)和骨髓间充质干细胞(BM-MSCs)在癫痫状态诱导的BBB损伤后全身给药,能有效穿越BBB。
这促进了中枢神经系统归巢,减少了神经变性、神经炎症和神经精神问题。
相互作用
MSCs在神经系统治疗中的应用:其在治疗各种神经系统疾病方面具有巨大的潜力。
TLE模型中的有效性:定时注射DPSC和BM-MSC在减轻TLE中的神经系统并发症方面显示出良好的效果。
鼻腔内和静脉内给药:MSC中的细胞外囊泡 (EV)(包括外泌体)可以穿过血脑屏障。它们在临床环境中具有治疗潜力,可通过静脉内或鼻腔内途径给药,避免神经外科手术。
干细胞疗法治疗神经退行性疾病的机制
据报道,干细胞(包括间充质干细胞、神经干细胞和胚胎干细胞)可以绕过血脑屏障 (BBB) 并成功定位到大脑中的目标,这使得它们成为治疗神经退行性疾病细胞疗法的一种有前途的方法。
跨越血脑屏障
血脑屏障就像一道安全检查站,阻止有害物质进入大脑。然而,干细胞可以穿过这道屏障。当大脑受伤或患病时,血脑屏障会变弱,让干细胞得以穿过并到达受影响的区域。
尽管血脑屏障是一种选择性屏障,但干细胞可以通过旁细胞或跨细胞途径穿过内皮细胞,随后优先返回大脑炎症或损伤部位,发挥治疗作用。
在中枢神经系统损伤(如创伤性脑损伤、中风、脑肿瘤或衰老)中,较低的紧密连接完整性和旁细胞间隙的形成允许细胞通过旁细胞途径迁移。据报道,MSC还可以消除和分裂内皮细胞之间的紧密连接。
MSCs的系统归巢过程
当干细胞被输入患者体内时,它们会进入血液,并开始一个多步骤的过程,以达到目标。首先,它们减速并附着在血管内壁上。然后,它们遵循特定蛋白质发出的化学信号,引导它们到达正确的位置。
人们认为,间充质干细胞的全身归巢是在一个类似白细胞的多步骤级联过程中与内皮细胞相互作用的结果。间充质干细胞在治疗给药后首先进入血液。在归巢过程中,间充质干细胞首先减速并与内皮细胞壁接触,与内皮细胞表达的选择素系在一起,并开始沿着血管壁滚动。
接下来,VLA-4等整合素受体会在基质细胞衍生因子-1(SDF-1)等G蛋白偶联趋化因子受体的作用下被激活,后者会与CXCR4或CXCR7等间充质干细胞表达的配体结合。激活整合素后,间充质干细胞会阻滞内皮膜,因为间充质干细胞表达的整合素(如VLA-4)会与内皮细胞上的VCAM-1结合。一次性激活增加了细胞停滞所必需的整合素的亲和力;因此,VLA-4/VCAM-1的相互作用可使间充质干细胞牢固地粘附在内皮细胞上。
间充质干细胞(MSCs)的归巢机制
间充质干细胞的一个关键优势是,由于其固有的归巢能力,它们能够针对特定的关注区域。当系统性地施用间充质干细胞归巢时,可以定义为离开循环并迁移到损伤部位。(7)
研究表明,MSC可能拥有类似白细胞的主动归巢机制,使其能够在受伤或发炎的情况下与BBB相互作用并穿过BBB。(1)
移行并迁移至受伤部位
一旦干细胞接近大脑受损区域,它们就需要离开血管并进入脑组织。它们通过挤过血管壁来做到这一点,这一过程称为迁移。离开血管后,干细胞会跟随更多化学信号找到需要它们的确切位置。一旦它们到达正确的位置,它们就可以开始修复损伤。
接下来,MSC会穿过内皮细胞层和基底膜,在基质金属蛋白酶 (MMP) 的分泌作用下,MSC会降解内皮基底膜。或者,MSC会破坏和分裂内皮细胞之间的紧密连接,从而促进它们的迁移。据报道,MSC还会通过质粒足穿透内皮。最后,MSC会迁移到损伤部位,在受损组织释放的各种信号(如生长因子和趋化因子)的引导下进行迁移。
在动物中风模型中,干细胞成功穿过血脑屏障
间充质干细胞具有逆转与中枢神经系统疾病(如多发性硬化症、帕金森病 (PD)和阿尔茨海默病 (AD))相关的神经元损伤的巨大潜力 。(4)
Yilmaz等人开展的研究发现,静脉 (IV) 注射的间充质干细胞 (MSC) 可以穿过血脑屏障,到达中风的脑动脉闭塞 (t-MCAO) 模型。 (5) 通过对大鼠注射放射性标记 (可见放射性化合物) MSC进行全身成像,证实了MSC的脑向性 (向脑内移动)。
在中风后的最初两个小时内,MSC会暂时穿过肺部,并随着时间的推移继续在脑缺血区域内迁移,穿过血脑屏障。该研究通过全身成像得出结论,间充质干细胞(MSC) 在静脉内注射后,可以在穿过血脑屏障后进入中枢神经系统。(5)
间充质干细胞(MSC)为何如此特殊?
间充质干细胞 (MSC) 是一种极好的治疗剂,因为它们易于分离、已确定的安全性,并且有可能针对参与神经元再生的多种途径。
MSC 因其可自我更新、分化、抗炎和免疫调节特性而被广泛用于治疗各种疾病。体外(在实验室环境中进行)和体内(在活体生物体内进行)研究支持了对MSC治疗在临床应用中的机制、安全性和有效性的理解。(6)
间充质干细胞会被困在肺部吗?
研究表明,静脉注射后干细胞在肺部滞留只是一种短暂现象,这意味着细胞最终会到达身体的其他部位(11)。物理尺寸对全身任何细胞的迁移能力都起着至关重要的作用。(见下图)。
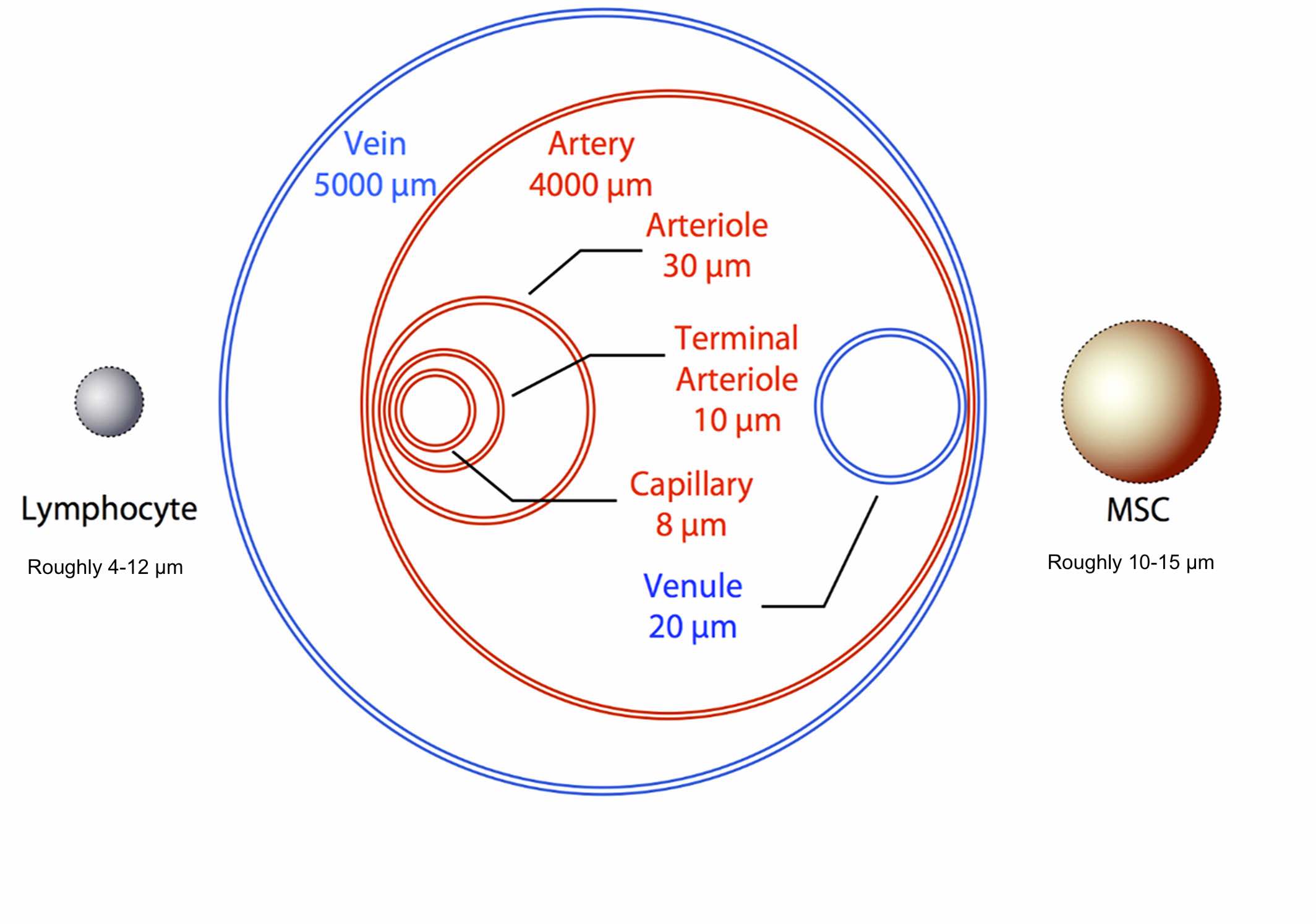
细胞大小可能导致细胞被困在某些区域,从而导致迁移能力丧失。间充质干细胞 (MSC) 的大小取决于其来源(骨髓、脂肪组织、脐带血或脐带组织)。重要的是,内源性MSC较小(约10μm),可通过体循环有效运输 (10)。
根据Major等人在2009年开展的一项研究,单个脐带组织来源的间充质干细胞的平均直径约为11μm(大小与白细胞相似)(9)。间充质干细胞还具有细胞变形性,这可以促进较大细胞通过较小的血管(10)。这些数据表明 MSCs 可以绕过肺部的“首过效应”(滞留在肺部),从而实现整个身体(包括中枢神经系统)的有效循环。
静脉注射的干细胞可以穿过血脑屏障
神经系统疾病通常难以治疗,部分原因是药物难以穿过血脑屏障 (BBB)。然而,通过静脉注射给药时,间充质干细胞可以穿过血脑屏障 (BBB)。研究表明,间充质干细胞迅速迁移到受损的大脑区域。这已通过对移植细胞进行磁共振跟踪得到证实。(1)
人们认为,脑部开口 (BBB) 可使MSCs及其分泌组有效穿过 大脑到达大脑中的所需位置,从而产生神经再生、减少炎症和减轻疼痛等各种再生效果。
我们发现多项研究专注于多发性硬化症、帕金森症、中风和ALS等神经系统疾病,这些研究都观察到了通过静脉注射间充质干细胞的积极结果。(8)
因此,可以确定间充质干细胞可以在多种不同的疾病模型中穿过血脑屏障 (BBB)。(4、3、5)

干细胞及其穿越血脑屏障的能力
总之,干细胞有望用于治疗各种神经系统疾病,因为它们可以穿过血脑屏障 (BBB) 并到达特定的大脑区域。虽然血脑屏障通常会限制大多数物质的通过,但干细胞可以通过不同的机制实现大脑渗透。
其中一种机制涉及间质液,它包围着细胞,可以作为干细胞绕过屏障的介质。此外,干细胞可以与血脑屏障的腔膜和血管内壁细胞相互作用,使它们能够进入脑组织。
在某些情况下,干细胞可以利用某些神经系统疾病或损伤中出现的BBB功能障碍。这使得干细胞更容易渗透到受影响的大脑区域并发挥其治疗作用。
通过研究,我们对干细胞如何穿过血脑屏障的理解已经取得了显著进展,其中包括发表在《冷泉港展望》等著名科学期刊上的研究。随着我们知识的增长,我们可以开发更有效的干细胞疗法来治疗各种神经系统疾病,最终改善患者的大脑健康和生活质量。
参考文献:
(1) Liu, L., Eckert, M. A., Riazifar, H., Kang, D.-K., Agalliu, D., & Zhao, W. (2013). From blood to the brain: can systemically transplanted mesenchymal stem cells cross the blood-brain barrier? Stem cells international. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3753739/.
(2) Conaty P;Sherman LS;Naaldijk Y;Ulrich H;Stolzing A;Rameshwar P; (n.d.). Methods of Mesenchymal Stem Cell Homing to the Blood-Brain Barrier. Methods in molecular biology (Clifton, N.J.). https://pubmed.ncbi.nlm.nih.gov/30196403/.
(3) Kim, S., Chang, K.-A., Kim, J. a, Park, H.-G., Ra, J. C., Kim, H.-S., & Suh, Y.-H. (2012). The preventive and therapeutic effects of intravenous human adipose-derived stem cells in Alzheimer’s disease mice. PloS one. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3458942/.
(4) Trounson, A. (2009, June 11). New perspectives in human stem cell therapeutic research. BMC medicine. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2702289/.
(5) Yilmaz, G., Vital, S., Yilmaz, C. E., Stokes, K. Y., Alexander, J. S., & Granger, D. N. (2011, March). Selectin-mediated recruitment of bone marrow stromal cells in the postischemic cerebral microvasculature. Stroke. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3042505/.
(6) Cona, L. A. (n.d.). Types of Mesenchymal Stem Cells (MSCs) and their Mechanisms of Action. RSS. https://www.dvcstem.com/post/mscs.
(7) Torres Crigna, A., Daniele, C., Gamez, C., Medina Balbuena, S., Pastene, D. O., Nardozi, D., … Bieback, K. (2018, June 15). Stem/Stromal Cells for Treatment of Kidney Injuries With Focus on Preclinical Models. Frontiers in medicine. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6013716/.
(8) Petrou, P., Kassis, I., Levin, N., Paul, F., Backner, Y., Benoliel, T., . . . Karussis, D. (2020, November 30). Beneficial effects of autologous mesenchymal stem cell transplantation in active progressive multiple sclerosis. Retrieved February 23, 2021, from https://academic.oup.com/brain/article/143/12/3574/6012789?login=true
(9) Majore, I., Moretti, P., Hass, R., & Kasper, C. (2009, March 20). Identification of subpopulations in mesenchymal stem cell-like cultures from human umbilical cord. Cell communication and signaling : CCS. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2676292/.
(10) Krueger, T. E. G., Thorek, D. L. J., Denmeade, S. R., Isaacs, J. T., & Brennen, W. N. (2018, August 1). Concise Review: Mesenchymal Stem Cell‐Based Drug Delivery: The Good, the Bad, the Ugly, and the Promise. Stem Cells Translational Medicine (AlphaMed Press). https://stemcellsjournals.onlinelibrary.wiley.com/doi/full/10.1002/sctm.18-0024.
(11) Fischer, U. M., Harting, M. T., Jimenez, F., Monzon-Posadas, W. O., Xue, H., Savitz, S. I., Laine, G. A., & Cox, C. S. (2009, June). Pulmonary passage is a major obstacle for intravenous stem cell delivery: the pulmonary first-pass effect. Stem cells and development. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3190292/.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号