过敏性鼻炎是一种非常普遍的鼻粘膜慢性炎症性疾病,对患者的健康和生活质量造成重大负担。目前的过敏性鼻炎疗法无法恢复免疫稳态或受到特定过敏原的限制。迫切需要过敏性鼻炎的潜在治疗策略。
间充质干细胞 (MSC) 是源自中胚层的多能干细胞,可以很容易地从各种来源中分离出来。由于其多向潜能和免疫调节能力,间充质干细胞为多种临床病症提供了一种很有前途的治疗选择,许多临床试验已经开始测试间充质干细胞对多种疾病的治疗效果。MSC具有强大的免疫调节作用和迁移至炎症部位的能力。
最近,间充质干细胞的疗法已被证明可有效治疗各种炎症和自身免疫性疾病。此外,几种AR动物模型表明,MSCs可以有效改善AR的症状。更重要的是,间充质干细胞对过敏性炎症中的先天性和适应性免疫反应具有显着的免疫调节特性。在此,首都医科大学附属北京同仁医院耳鼻喉头颈外科报告了MSCs在过敏性气道炎症中的免疫调节作用。

过敏性鼻炎中的免疫反应
由吸入季节性或常年性过敏原引发的鼻粘膜过敏性免疫反应包括由IgE介导的肥大细胞立即释放化学介质,以及以招募其他效应细胞(包括嗜酸性粒细胞、嗜碱性粒细胞和Th2细胞)为特征的晚期反应,这些细胞对AR的免疫病理学有很大贡献。此外,上皮细胞、第2组先天淋巴细胞(ILC2s)、抗原呈递细胞、B细胞和调节性T细胞都参与了过敏性免疫反应(图1)。

鼻粘膜中的过敏性免疫反应是由吸入季节性或常年性过敏原引发的,其特征是IgE介导的反应和2型炎症。上皮细胞和包括嗜酸性粒细胞、Th2细胞、ILC2、M2巨噬细胞、抗原呈递DC和B淋巴细胞在内的各种炎症细胞参与过敏性免疫反应。由于各种炎症细胞、多种细胞因子、趋化因子和这些炎症细胞产生的有毒颗粒蛋白的复杂相互作用,慢性炎症在鼻粘膜中发展。
目前治疗过敏性鼻炎的策略
目前AR的治疗选择包括患者教育、避免刺激物和过敏原、药物治疗和过敏原免疫治疗 (AIT)。药物疗法,包括鼻用糖皮质激素、抗组胺药、白三烯受体拮抗剂 (LRA) 和肥大细胞膜稳定剂,靶向参与过敏性炎症的免疫细胞和重要介质以控制症状(图1)。药物疗法的选择取决于症状的严重程度、治疗的有效性和安全性、当前的治疗、对治疗的历史反应以及对睡眠和工作效率的影响。
间充质干细胞在治疗过敏性鼻炎中的作用
关于AR的治疗策略,现有的主要药物疗法只能治疗症状和炎症,但不能逆转免疫失衡状态。AIT是目前唯一旨在调节免疫系统的治疗方法;但仅限于特定的过敏原,长期治疗有诱发全身过敏反应的风险。因此,迫切需要潜在的治愈性疗法。
干细胞疗法的出现给治疗AR带来了新的机遇和挑战。研究调查了MSCs在治疗各种过敏性疾病中的效率。2009年,一项研究表明脂肪来源的MSCs可以在小鼠模型中治疗AR,从那时起,越来越多的研究证明了MSCs在AR动物模型中的治疗效果。
在AR小鼠和大鼠模型中,MSCs有效减少了打喷嚏和揉鼻子的次数,并通过减少炎症细胞的浸润减轻了鼻粘膜的局部炎症;减少IgE、组胺、白三烯和2型细胞因子的释放;和降低血清IL-4和IL-6水平。来自各种资源(包括iPSC、BM、脂肪组织、人类UC、扁桃体和人类脱落的乳牙)的MSC的作用已经得到评估。
在MSC治疗的AR动物模型中,MSC治疗的效果持续时间为5至30天。MSC治疗AR的长期疗效需要进一步评估。尽管尚未完全证明MSCs在AR患者中的治疗效果,但已经注册了多项临床试验以确认MSCs的效果(表2)。
表2. 基于间充质干细胞治疗过敏性鼻炎和哮喘的临床试验。所有信息均来自http://clinicaltrials.gov/。
| NCT号 | 阶段 | 状况 | 分配; 掩蔽 | 干预措施;剂量 | 注册人数 | 地位 | 国家 |
|---|---|---|---|---|---|---|---|
| NCT05151133 | 一期 | 过敏性鼻炎 | 非随机化;单身(结果评估员) | 单次注射hUC-MSC;低剂量(0.5×106 个细胞/kg),或中剂量(1.0×106 个细胞/kg),或高剂量(2.0×106 个细胞/kg) | 18 | 招聘中 | 中国 |
| NCT05167552 | 一期和二期 | 过敏性鼻炎、慢性鼻窦炎 | 非随机化;打开标签 | 接受OM-MSCs或标准治疗的AR患者,以及接受OM-MSCs和标准治疗的CRS患者;北美 | 60 | 尚未招聘 | 白俄罗斯 |
| NCT03137199 | 一期 | 哮喘 | 非随机化;打开标签 | 单次静脉注射hBM-MSCs;2×107个细胞,或1×108 个细胞 | 3个 | 终止 | 美国 |
| NCT05147688 | 一期 | 肺部疾病、哮喘、慢性阻塞性肺病 | 不适用;打开标签 | hUC-MSCs单次静脉输注;1亿个细胞 | 20 | 招聘中 | 英国 |
| NCT02192736 | 一期和二期 | 哮喘 | 不适用;打开标签 | 鼻内施用来自hUC-MSC的营养因子,每周一次,持续4周;北美 | 20 | 未知 | 巴拿马 |
| NCT05035862 | 一期 | 哮喘 | 不适用;打开标签 | 单次静脉输注干扰素-γ引发的BM-MSCs;2 ×106个细胞/kg,或5×106个细胞/kg | 12 | 招聘中 | 美国 |
间充质干细胞治疗的免疫调节机制
在经MSC处理的AR小鼠中,MSC可增强Treg的作用,恢复Th1/Th2 细胞的免疫平衡,并调节2型免疫反应的关键细胞和分子。MSC免疫调节作用的潜在机制与细胞间接触以及细胞外囊泡 (EV) 和可溶性因子有关(图2)。
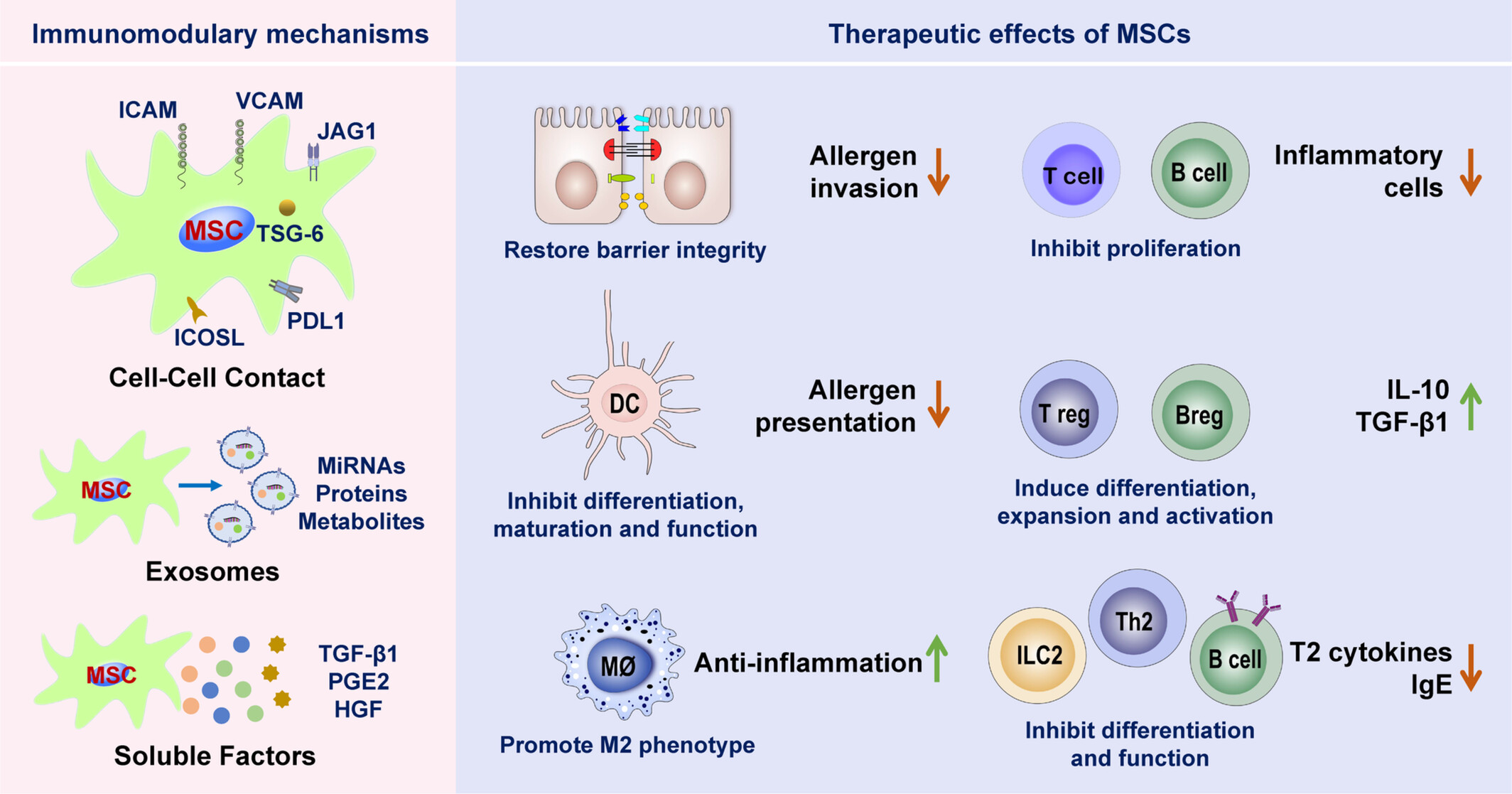
MSCs可以增强Treg细胞的作用,恢复Th1/Th2细胞的免疫平衡,促进M1巨噬细胞向M2巨噬细胞的转变,恢复上皮屏障的完整性,调节2型免疫反应的关键细胞和分子。MSCs免疫调节作用的潜在机制与细胞间接触、细胞外囊泡和可溶性因子有关。
细胞间接触的免疫调节:活化的MSCs迁移并与各种免疫细胞相互作用以调节其功能,研究表明细胞与细胞的接触在MSCs的免疫调节作用中起着重要作用。
EV介导的免疫调节:外泌体是由直径从30到200nm不等的细胞产生的EV。由于外泌体携带核酸、蛋白质、脂质和代谢物,它们是健康和疾病中短距离和长距离细胞间通讯的重要介质。MSC可以释放外泌体/EV,越来越多的人认为它们是负责MSC治疗功能的关键旁分泌因子,并已在免疫调节中用作无细胞疗法。与其亲本细胞相比,MSC-EVs保留了其免疫抑制作用,可能具有更高的安全性,并且可以在不丧失功能的情况下储存。
基于外泌体在药物递送中的性能,外泌体被设计用于递送多种治疗有效载荷,例如小分子和核酸药物,以实现靶向药物递送,这在基于 MSC的鼻内递送治疗AR中具有前景。
可溶性因子介导的免疫调节:各种研究已经证明了MSCs产生的可溶性因子在免疫调节中的重要作用。
越来越多的证据表明,MSC分泌的可溶性因子可以调节T细胞介导的免疫反应。Tregs通过产生IL-10和TGF-β在维持对过敏原的免疫耐受中发挥关键作用。已发现2型免疫反应和Treg之间的失衡在过敏性疾病的免疫病理学中是有效的。
结论与展望
尽管有适当的指南指导的药物治疗,10%–20%的过敏性鼻炎患者对治疗没有反应并且对他们的症状仍然不满意。与现有仅缓解过敏症状的药物疗法相比,MSCs对先天性和适应性免疫反应具有显着的免疫调节特性,可增强Tregs的作用,恢复Th1/Th2细胞的免疫平衡,对抗2型免疫反应。
因此,间充质肝细胞治疗不仅可以缓解过敏性鼻炎的症状,还可以恢复免疫系统的稳态,是一种很有前途的治疗过敏性鼻炎的策略。
参考资料:王明,赵 南, 王春, 金正斌, 张丽。 间充质干细胞的免疫调节特性:过敏性鼻炎的潜在治疗策略。过敏。 2023 年;00 : 1-16。doi: 10.1111/all.15729
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号