神经干细胞是开发再生疗法的一种有吸引力的工具,并且正在针对多种神经系统疾病的临床试验中进行测试。人神经干细胞可以从中枢神经系统分离,或者可以在体外源自多能干细胞。胚胎来源在伦理上存在争议,而其他来源的特征不太明确和/或效率低下。
最近,有报道从脊柱裂和脑室内出血患者的脑脊液中分离出NSC。如果确保重编程细胞的遗传和表型稳定性,直接重编程可能成为另一种选择。
在这里,我们讨论了用于生产临床应用细胞疗法的可用神经干细胞来源的优点和缺点。我们回顾了现有的安全性和有效性临床数据。并讨论目前神经干细胞移植的临床研究方向。
什么是神经干细胞?
神经干细胞(neural stem cells, NSCs)是指具有分化为神经元、星形胶质细胞和少突胶质细胞的能力,能自我更新并能提供大量脑组织细胞的细胞群。
狭义的神经干细胞是指成体神经干细胞,指的是分布于胚胎及成人中枢及周围神经系统的干细胞。简单的说,就是在成年哺乳动物的大脑中分离出来的具有分化潜能和自我更新能力的母细胞,它可以分化各类神经细胞,包括神经元、星形胶质细胞和少突胶质细胞。

我们所讲的神经干细胞指的就是成体中存在于脑中的中枢神经干细胞,其实在外周也有一些“神经干细胞”称为“神经嵴干细胞”,可以分化成外周神经细胞、神经内分泌细胞和施旺细胞,还可横向分化成色素细胞和平滑肌细胞(这个也叫转分化)。
NSC有可能迁移到受损区域以促进功能和结构组织修复。此外,NSC具有分泌可刺激内源性修复机制的营养因子(例如胶质细胞源性和脑源性神经营养因子)的能力。与间充质干细胞(MSC)类似,NSC可以发挥免疫调节作用,神经干细胞移植已被证明可以抑制T细胞增殖。所有这些特性使得NSC对于再生疗法具有吸引力,特别是考虑到自我修复能力有限以及大多数中枢神经系统 (CNS) 疾病缺乏有效的治疗方法。
到目前为止,大多数临床试验都使用胎儿NSC(fNSC),但来自其他来源(例如多能干细胞(PSC)的 NSC也越来越多地进入临床阶段。此外,原发性NSC的新来源,例如脊柱裂的脑脊液 (CSF) 或脑室内出血 (ICVH) 早产儿的脑脊液 (CSF) 已被报道,并且可能在不久的将来可用(图1)。
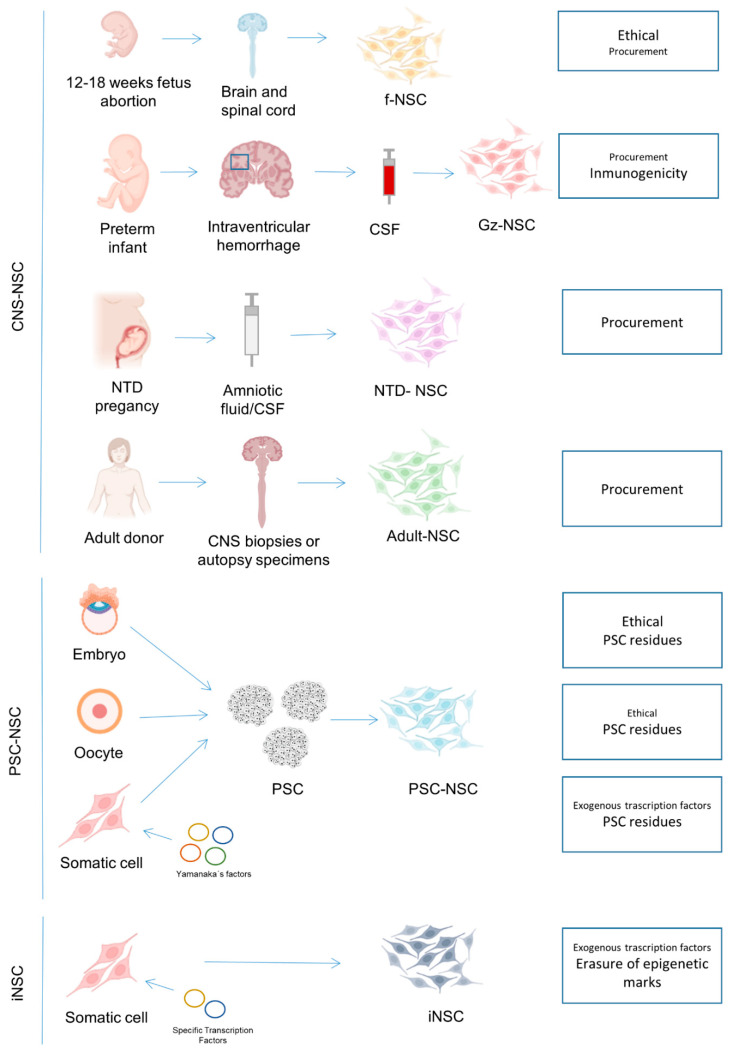
CNS:中枢神经系统;PSC:多能干细胞;fNSC:胎儿神经干细胞,CSF:脑脊液;Gz-NSC:生发区神经干细胞;NTD:神经管缺陷;iPSC:诱导多能干细胞;ESC:胚胎干细胞;pESC:孤雌生殖干细胞;ntESC:核移植胚胎干细胞;iNSC:诱导神经干细胞。
神经干细胞(NSC)的主要来源:
来源于神经组织:目前从哺乳动物胚胎期大部分脑区、成年期的脑室下区、海马回的颗粒下层、脊髓等部位均成功分离出神经干细胞
来源于胚胎:胚胎干细胞、胚胎生殖细胞等细胞的定向诱导分化而来。
来源于血液系统:骨髓间质干细胞、成年多能祖细胞及脐血细胞。
来源于永生化细胞系:C17.2细胞系、MHP36细胞系、NT2细胞系
体核细胞转移技术获得神经干细胞:将体细胞核植入去核的卵母细胞浆中。
4种来源的神经干细胞的优缺点
| 来源 | 优点/特点 | 缺点/风险 | 临床研究 |
| 人流产胎儿胎脑海马组织 | 纯度活性最高,生物学功能最强 | 来源限制,无法量产伦理问题 | 有 |
| IPS细胞诱导分化 | 自体来源,无伦理限制可量产 | 技术性太强,纯度待定,有一定致瘤性风险 | 有 |
| 间充质干细胞诱导分化 | 可量产 | 纯度和神经干生物学功能难评估,存在诱导分化技术风险 | 无 |
| 胚胎干细胞诱导分化 | 可量产 | 伦理问题,来源稀少,存在诱导分化技术风险 | 有 |
中枢神经系统的神经干细胞
从人胎儿神经外胚层中分离出NSC
迄今为止进行的大多数临床试验都采用从人类胎儿中枢神经系统(大脑和/或脊髓)获得的NSC(表格1)。大多数情况下,组织是从选择性终止妊娠中收集的,这引起了重大伦理问题,并受到许多人基于道德和宗教理由的反对。反堕胎活动人士提出了使用胎儿组织可能鼓励妇女堕胎的想法,尽管没有证据表明使用胎儿组织用于治疗或商业目的会增加选择堕胎的数量。然而,fNSC的使用存在社会争议并受到严格监管,在一些国家被禁止。



使用自然流产中的fNSC可以部分绕过这些问题,但这些流产很少见且不可预测,因此很难规划有效扩大规模的程序。此外,来自自然流产胎儿的细胞可能含有严重的遗传缺陷,需要在细胞分离之前进行仔细的筛选和选择(例如,仅使用由创伤引起的流产)。
与早期移植试验相比,胎儿中枢神经系统组织在解剖后立即移植到患者体内以确保活力,而fNSC体外培养的优化解决了使用新鲜组织的许多主要供应和后勤障碍。另一方面,包括体外细胞扩增步骤,将fNSC的监管分类更改为药品 (FDA/EMA),并随之要求遵守当前的良好生产规范 (GMP) 和其他法规。
从脑脊液中分离出神经干细胞
我们和其他人最近报道,原发性神经干细胞可以从被诊断患有严重脑室内出血 (IVH) 或神经管缺陷 (NTD) 的婴儿的CSF中分离出来,收集用于诊断或治疗目的。
我们最近证明,神经干细胞可以很容易地从收集的CSF中回收,并且细胞可以有效地扩增和储存,并且不会致瘤。
从活检和尸检材料中分离出神经干细胞
NSC也可以从成人和胎儿中枢神经系统活检或尸检标本中分离出来。它们已从不同的大脑区域中分离出来,包括皮质、室下区、海马体、中脑和脊髓。
多能干细胞衍生的神经干细胞
NSC也可以通过多能干细胞(PSC)的分化获得。人PSC可以源自囊胚期胚胎(胚胎干细胞,ESC)的内细胞团,通过未受精卵母细胞的化学激活(孤雌生殖干细胞,pESC)或核移植(ntESC)获得或通过体细胞的表观遗传重编程产生具有一组确定的转录因子的细胞(诱导多能干细胞,iPSC)(图1)。
诱导神经干细胞
诱导从体细胞类型直接重编程为NSC (iNSC),无需经过多能状态,可以通过使用特定的转录因子 (TF) 以及有时借助药理化合物来实现。这个过程会导致给定细胞类型的转录组谱发生变化,并获得另一种细胞类型的转录谱,从而失去其自身的表型。最初的研究遵循山中伸弥的策略,将成纤维细胞直接重新编程为神经元。这提供了一种利用强制外源基因表达来获得NSC的新策略,但所得神经细胞仅分裂几次。
人神经干细胞移植的临床研究方向
1、帕金森病
目前神经干细胞移植技术应用到临床研究中的应用最多的是帕金森病。
帕金森病 (PD) 是最常见的神经退行性疾病之一,与运动和非运动功能障碍有关。PD涉及黑质 (SN) 中多巴胺能 (DA) 神经元的丢失。目前建立的治疗方法包括药物治疗和深部脑刺激,可以暂时改善症状,但不能治愈该疾病。因此,在过去的二十年里,细胞替代疗法至少在实验中已证明是PD患者和PD动物模型的潜在治疗方法。
PD患者的室管膜下区、颗粒下区和嗅球的神经前体细胞/NSCs数量在死亡后有所减少,提示PD患者神经前体细胞/NSCs的产生受损,这是多巴胺能的结果神经丧失。这表明NSC/神经祖细胞与PD之间存在密切关系。
因此,神经干细胞移植可能成为治疗帕金森病的一种新的神经功能恢复策略。神经干细胞移植可以融入中枢神经系统周围环境,建立适当的微环境,增强多巴胺能神经传递。神经干细胞可以通过识别微环境中靶标的细胞和非细胞区域来分化为多巴胺能细胞。通过将分化的多巴胺能神经元整合到现有的黑质纹状体多巴胺能通路中,可以缓解PD的症状。
2、脑卒中
缺血性卒中是威胁人类健康的主要疾病之一,具有高发病率、高致残率和高病死率等特点。静脉溶栓治疗和血管内治疗是目前治疗急性脑梗死最有效的方法,但治疗时间窗短,易出现出血并发症。多种神经保护药物在动物实验中被证实有效,而临床试验结果却不尽如人意。
不同类型的干细胞如胚胎干细胞(embryonic stem cells, ESCs)、间充质干细胞、诱导性多能干细胞和神经干细胞(neural stem cells,NSCs),作为缺血性卒中后的细胞替代疗法被广泛研究,使脑梗死患者的神经修复成为可能。
NSCs作为一种具有自我更新能力的多能细胞,主要通过以下两种方式治疗缺血性卒中:
(1)通过内源性神经再生使神经细胞活化;
(2)通过外源性NSCs移植,发挥细胞替代和旁分泌效应等多种功能,促进神经再生与修复。
3、渐冻症
渐冻症全称为肌萎缩侧索硬化症 (ALS) ,目前是无法治愈的:利鲁唑和依达拉奉是唯一获准用于治疗ALS的药物,但它们的疗效不大。干细胞作为无法治疗的神经系统疾病,特别是ALS的新型治疗剂,前景广阔。
我们和其他团体先前的研究已经证明,人类神经干细胞 (hNSC) 有能力与脑组织整合,并在神经系统疾病的啮齿动物模型中显示出治疗效果:这些研究表明,移植后,hNSC的后代能够有效地整合到宿主脑实质中并在其中存活,可能通过旁观者效应引发有益作用,包括释放生长因子和免疫调节。
2019年,国际期刊杂志《Stem Cells Transl Med》发表了一篇《肌萎缩性脊髓侧索硬化症椎管内注射神经干细胞I期临床试验结果:长期结果》的文献综述。

结果表明源自自然流产的捐赠胎儿的非永生化人类神经干细胞提供了一种高度可重复和标准化的良好生产规范生产方法。这种方法为渐冻症提供了一种可行且安全的治疗方法。
4、阿尔茨海默病(老年痴呆症)
阿尔茨海默症是一种复杂的疾病,病因至今尚无定论。
医学上普遍认为它可能是一组异质性疾病,在多种因素(包括生物和社会心理因素)的作用下才发病。从目前研究来看,该病的可能因素有家族史、头部外伤、重金属污染、氧化应激压力、甲状腺病、病毒感染等。
但令人遗憾的是,目前全球医学界对这种病仍束手无策,没有能够治愈阿尔兹海默症的特效药及治疗。仅有的几种药物只能在一定程度上改善患者的认知功能。针对阿尔兹海默病的治疗只能早期控制一些症状,但是不能阻断病情的进展,开发新的治疗方法,已迫在眉睫。
近年来,干细胞移植治疗神经退行性疾病越来越受到关注。干细胞移植对神经退行性疾病发展过程中的多个缓解具有干预作用,如修复受损突触、调节炎性反应和神经保护等。目前,最常用于治疗神经退行性疾病的干细胞类型有NSCs、间充质干细胞(MSCs)和诱导多能干细胞(iPSCs)等。其中,神经干细胞移植治疗阿尔茨海默病被认为具有巨大潜力,可能在多个环节起作用,如保护毛细血管、减少Aβ和tau沉积、缓解炎性反应和促进神经发生等。
2023年10月,来自中国天津中医药大学第一附属医院赵岚团队在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表了题为“Neural stem cells promote neuroplasticity: a promising therapeutic strategy for the treatment of Alzheimer’s disease”的综述。

该综述发现,神经可塑性可在整个生命期存在,且随着年龄的增长而其能力不断下降,且在衰老和阿尔茨海默病患者中受损明显。因此,促进神经可塑性可能是缓解阿尔茨海默病的一个有前途的策略。神经干细胞不仅能减轻淀粉样蛋白β和tau蛋白水平,也能促进突触可塑性和神经发生以修复哺乳动物大脑的微环境,这被认为是改善阿尔茨海默病有巨大潜力的新疗法。
结论
神经干细胞移植的治疗潜力已得到科学界的广泛认可,但迄今为止进行的临床研究结果表明,要提高其疗效还需要进一步的研究。胚胎来源存在争议且受到严格监管,阻碍了研究的进展。iPSC衍生的神经干细胞被认为是开发细胞疗法的一个有前途的来源,因为它们不会带来伦理问题,而且是一种可扩展的 “取之不尽 “的来源。
参考资料:Fernandez-Muñoz B, Garcia-Delgado AB, Arribas-Arribas B, Sanchez-Pernaute R. Human Neural Stem Cells for Cell-Based Medicinal Products. Cells. 2021 Sep 9;10(9):2377. doi: 10.3390/cells10092377. PMID: 34572024; PMCID: PMC8469920.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请及时跟本公众号联系,我们将在第一时间处理。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号