近期在Cell Discovery上由长征医院、仁济医院和中科院等单位合作,完成一例自体内胚层干细胞来源胰岛组织治疗2型糖尿病的案例,效果出色。

上海长征医院完成世界首例,干细胞治疗2型糖尿病,3月停掉胰岛素,12月停掉阿卡波糖,14月停掉二甲双胍
患者为59岁男性,有25年2型糖尿病病史,2017年6月出现终末期糖尿病肾病并接受肾移植,2019年11月起血糖控制不佳,血糖水平在3.66-14.60mmol/L之间,平均血糖偏移幅度(MAGE)为5.54mmol/L。
由于对低血糖的主要担忧以及考虑血糖控制不佳对供体肾脏长期生存的不利影响,患者同意使用自体内胚层干细胞衍生的胰岛组织的肝内移植。
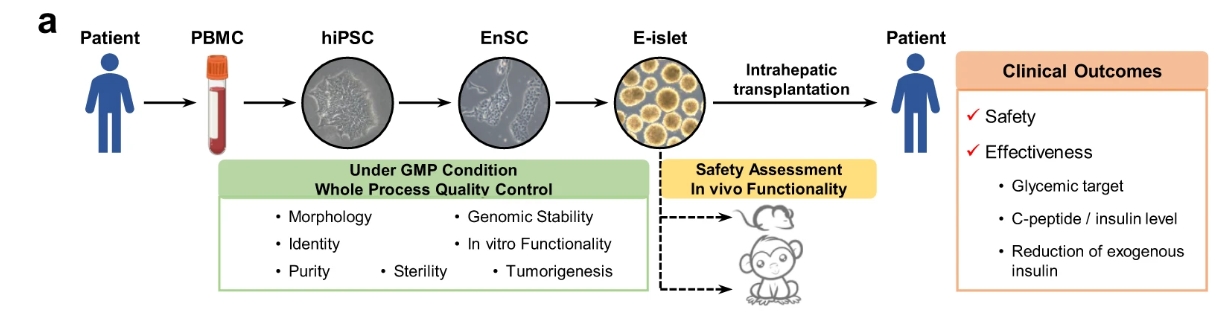
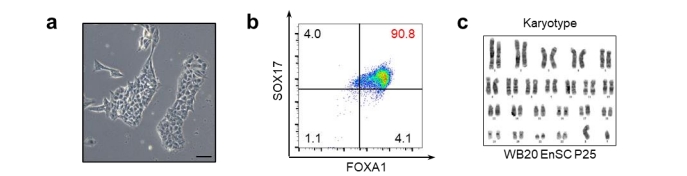
由上图可见该细胞是通过自体外周血诱导多能干细胞建立了内胚层祖细胞(EP),然后再将其衍生为胰岛组织。
前期的研究证实,将内胚层干细胞EnSC或内胚层干细胞衍生胰岛移植到免疫缺陷动物中,未检测到肿瘤形成或表明细胞增殖的囊性/导管结构。
患者接受了经皮经肝门静脉移植,给予了120万个IEQ的胰岛组织,符合临床胰岛移植注册的监管指南。在指定访视时,在基线、第4、8、12、16、20、24、36和48周以及之后的指定时间点通过混合膳食耐受性试验 (MMTT) 检查内分泌功能和糖尿病特异性参数,使用24小时实时连续血糖监测系统 (CGM) 测量患者的血糖控制。
在长达116周(近2年半)的随访期间,无论是通过上腹部的MRI还是通过血清肿瘤相关抗原标志物的测量均未检测到肿瘤形成。
在前116周内监测了三个主要临床结局,即血糖目标、外源性胰岛素的减少以及空腹和进餐刺激的循环 C 肽/胰岛素水平。
早在移植后第2周,就观察到患者血糖控制的明显变化,MAGE从5.50mmol/L下降到3.60mmol/L,滴度从56.7%迅速增加到77.8%。在同一时期,超时(TAR)较基线下降了55%,而严重高血糖(>13.9mM)和低血糖(<3.9mM)的事件完全消失。在第4周和第12周之间,观察到动态平均血糖波动显着降低(从 5.50 到2.6mmol/L)和TITR稳步上升(从81%到90%)。第32周后,患者的滴度已轻松达到99%,此后一直保持下去,而血糖变异性的金标准MAGE从5.50mM降低到1.60mM。
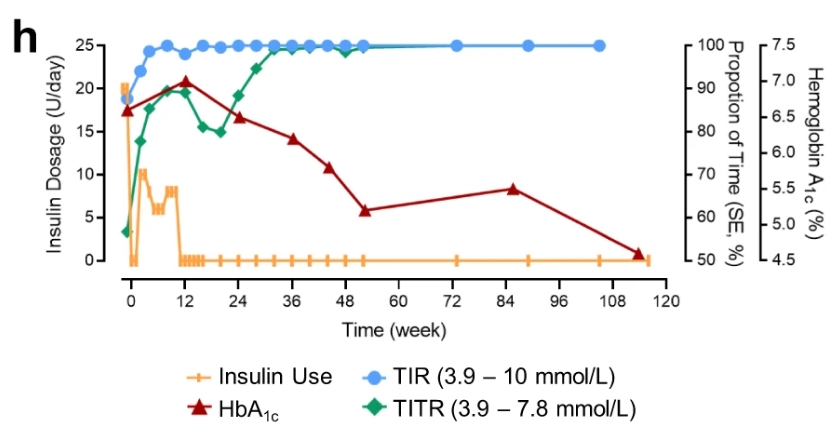
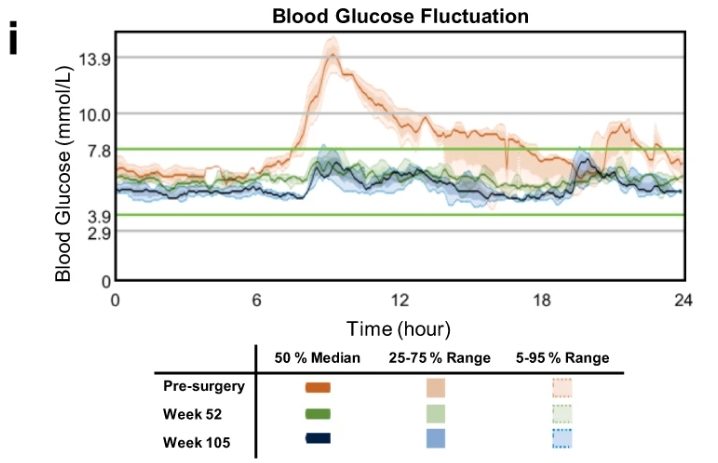
重要的是,在术后 116 周的整个随访期间未观察到低血糖或严重高血糖发作。此外,MMTT显示手术后血糖变异性趋于稳定,表现为稳定的空腹血糖浓度和餐后血糖浓度的显着降低(基线时最大值为21.3 mM,第105周时最大值为9.1 mM)。血红蛋白 A1c 水平从 6.6%(基线)下降到 5.5%(第 85 周)和 4.6%(第 113 周)。
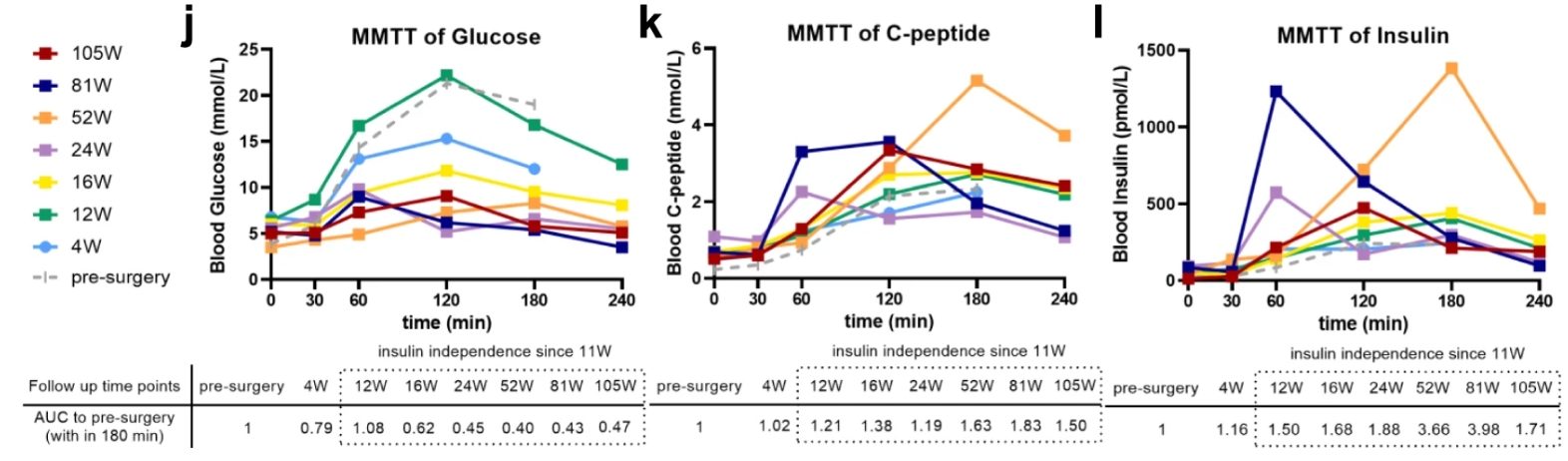
与术前水平相比,术后平均空腹C肽水平(0.68 nmol/L)增加了3倍。
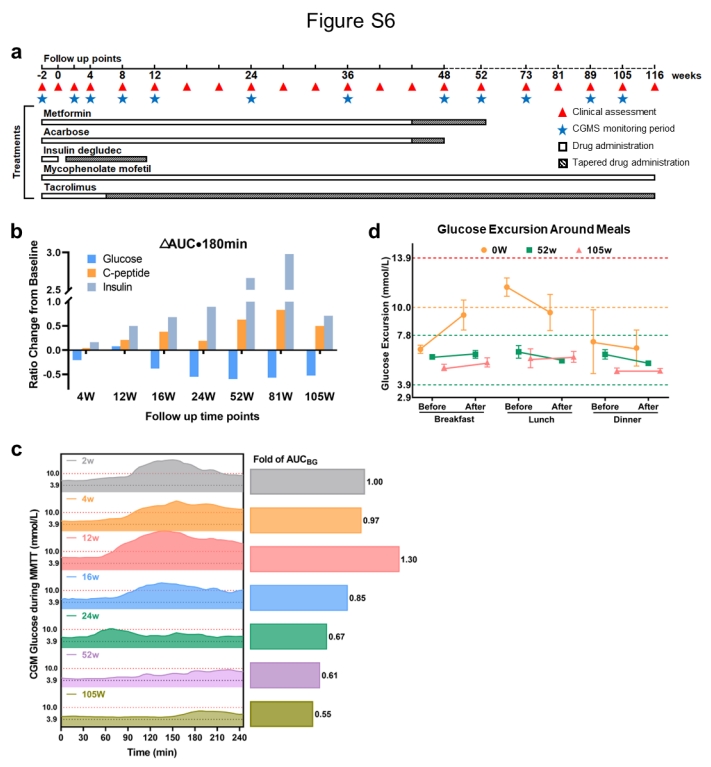
值得注意的是,胰岛素需求逐渐减少,直到第11周结束时完全停药,口服抗糖尿病药物从第44周开始逐渐减少,并在第48周(阿卡波糖)和第56周(二甲双胍)停药。
总的来说,这是国际上首次使用自体衍生胰岛治疗胰岛功能受损的T2D患者的人体组织替代疗法。
前27个月的数据显示血糖控制有显着改善,并提供了干细胞来源的胰岛组织可以挽救晚期T2D患者胰岛功能的第一个证据。移植物耐受性良好,没有肿瘤形成或严重的移植物相关不良事件。
参考资料:Wu, J., Li, T., Guo, M. et al. Treating a type 2 diabetic patient with impaired pancreatic islet function by personalized endoderm stem cell-derived islet tissue. Cell Discov 10, 45 (2024). https://doi.org/10.1038/s41421-024-00662-3
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号