卵巢早衰(POI)对女性的生活质量有着深远的影响。由于对这种疾病的病因和复杂性缺乏充分认识,感染患者尚无适当的治疗方法。
近年来,干细胞疗法引起了再生医学学者的关注,并为POI患者带来了良好的治疗效果。多种干细胞,如胚胎干细胞(ESC)、间充质干细胞(MSC)和诱导多能干细胞(iPSC)已被用于治疗卵巢疾病。然而,它们潜在的保护机制仍然未知。毫无疑问,更好地了解干细胞的治疗分子和细胞机制将有助于发现策略,以增加其对POI等多种疾病的临床应用。
近期,“A Cell Press journal”杂志发表了一篇干细胞在治疗卵巢早衰中的保护作用:现状与作用机制的综述文章。本文详细描述了卵巢早衰的发表机制、干细胞治疗卵巢早衰的机制,目前支持干细胞治疗卵巢早衰的证据有哪些,并全面回顾了间充质干细胞治疗卵巢早衰的临床案例。因此,本次综述将为干细胞治疗卵巢早衰中的进一步临床应用提供概念验证。

卵巢早衰的发病机制特点
尽管POI发病机制的确切机制尚不清楚,但卵泡数量减少和激素分泌缺乏是最常见的机制之一。POI的特点是卵巢功能提前终止、卵泡发生受阻以及静息原始卵泡池耗尽。卵泡发生是一个复杂的过程,受多种信号通路以及卵母细胞和周围体细胞之间的串扰调节。在成年女性的生殖寿命中,原始卵泡发育为初级、次级和窦状期卵泡。但是,只有少数卵泡被选择用于排卵,并且大多数原始卵泡因细胞凋亡而丢失。因此,原始卵泡池是生育力和生殖健康的决定因素。如前所述,卵泡凋亡率增加和卵泡数量峰值减少是POI的标志。
然而,在POI女性中并未发现原始卵泡完全缺失,并且一些卵泡仍保留在这些患者的卵巢中。因此,激活这些休眠卵泡可以被认为是一种有前途的治疗方法。为此,确定该过程中涉及的病理机制可以被视为新的治疗靶点。卵巢早衰的发生涉及多种机制,包括卵巢炎症、纤维化、颗粒细胞(GC)凋亡、自噬不足和过度氧化应激(图1)。
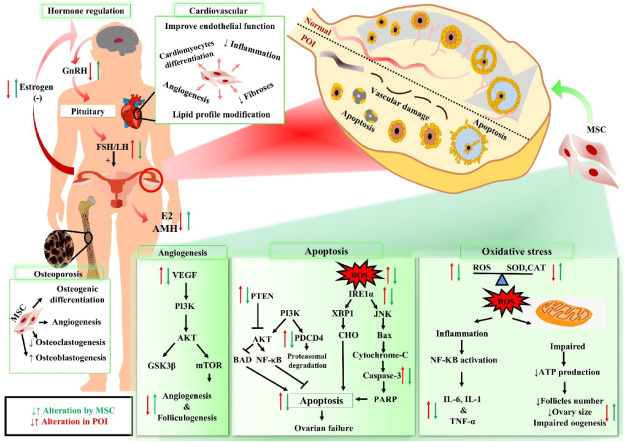
表1:干细胞治疗卵巢早衰的临床前研究
| 干细胞 | 剂量 | 运输方式 | 年 | 研究成果 | 机制 | 参考号 |
|---|---|---|---|---|---|---|
| BM-MSC-EV | 125μg溶解在 100 μL PBS 中 | IV | 2020年 | ↑ E2 和 AMH ↓ FSH ↑ 基底和窦卵泡数量 抑制 GC 凋亡 | 通过外泌体 mir-144 靶向 PTEN-PI3K/AKT 抑制 GC 凋亡 | 【202】 |
| 骨髓间充质干细胞 | 2×106 | IV | 2021年 | ↑ FSH 和 E2 恢复生育能力 ↑ 卵巢卵泡池 ↓ 卵巢细胞凋亡 ↑ 颗粒细胞增殖和次级卵泡发育 | 通过 TGF-β、Wnt/β-catenin 和 Hippo 途径控制卵巢卵泡的凋亡、增殖和分化 通过上调 FOXO1、GDF-9 和 Fst 基因以及 Bax/Bcl- 细胞凋亡抑制来恢复卵泡发生过程2、半胱天冬酶3 | [71] |
| BM-MSC-EV | 150μg溶解于100 μL PBS | IV | 2021年 | ↓ FSH和LH ↑AMH和E2 ↓ GC凋亡 | 通过靶向p53的外泌体MiR-644-5p改善卵巢功能并减少GC凋亡 | 【204】 |
| AD-MSC | 1×106 | IP | ↑原始卵泡数 ↓闭锁卵泡数 ↑AMH ↓卵泡凋亡 | Connexin43和pnnexin1的表达调控 | 【224】 | |
| AD-MSC-EV | 1×106 | IP | 2018年 | ↑ 卵泡数 ↓ GC 凋亡 | 通过上调 SMAD 抑制 GC 凋亡和 GC 增殖 | 【206】 |
| 男性SC | 2×106 | IV | 2017年 | ↑ 卵泡数量 ↓ GC 凋亡 ↑ 再生和卵巢功能 | 分泌 FGF2 的保护作用 | [141] |
| 男性SC | 1×106 | IV | ↑ AMH、FSHR 和 E2 | 不报告 | [39] | |
| 男性SC | 1×106 | IV | 2019年 | ↑ 卵泡数 ↓ GC 凋亡 | ↓ 促凋亡基因表达(如 Bax) ↑ 抗凋亡基因表达(如 Bcl-2) | [126] |
| 间充质干细胞 | 1×106 | IV | 2021年 | ↑ 卵巢大小和数量 ↑ 初级和次级卵泡 ↓ 闭锁卵泡 ↑ E2 和 ↓ FSH | 通过 AKT 激活发挥抗凋亡和抗炎作用 | [80] |
| 间充质干细胞 | 1×106 | IV | 2019年 | ↑ 卵泡数和 ↓ 闭锁卵泡 ↑ E2 和 ↓ FSH ↑IL-4 和 ↓ IFN-γ 和 IL-2 | 通过调节 Th1/Th2 细胞因子比率恢复卵巢功能和子宫内膜容受性 | [114] |
| 间充质干细胞 | 5×106 | IV | 2019年 | ↑ E2 和 AMH 卵泡生成恢复 ↑ 怀孕率 | 通过 NGF/TrkA 信号通路改善卵巢功能 | [131] |
| 间充质干细胞 | 2×106 | Orthotopically | 2016年 | ↑ E2 和 AMH ↓ FSH ↑ 窦卵泡数量 | TGF-β的表达和PCNA调节 | [144] |
| 间充质干细胞 | 低(0.25×106),中 (1 × 106)和高 (4 × 106) | IV | 2020年 | ↑ E2 和 AMH 恢复动情周期 ↓ GC 凋亡 | 未报道 | [95] |
| 间充质干细胞 | 1×106 | IV | 2022年 | ↑ FSH 和 E2 ↓ 卵泡闭锁 抑制 T 细胞增殖 | 通过 PPAR 和胆固醇代谢途径改善卵巢功能 | 【225】 |
| ID | 阶段 | 地位 | 地点 | 细胞类型 | 剂量 | 路线 | 样本量 | 主要结果 | 次要结果 |
|---|---|---|---|---|---|---|---|---|---|
| NCT02151890 | Ⅰ Ⅱ | 完全的 | 爱资哈尔大学 | 测量 OCT4 标记 | 不适用 | 腹腔镜注射 | 人数 =40 | 怀孕 | 不适用 |
| NCT05138367 | 我 | 完全的 | 丁丽君,南京大学 | UCA-PSC 或 WJ-MSC | 1×107/400μL | 局部(注入卵巢组织) | n=20 | 卵巢血液灌注 和 窦卵泡直径 | 卵巢血流指数 |
| NCT02043743 | Ⅰ Ⅱ | 完全的 | 埃尔拉亚德生育中心 | 骨髓间充质干细胞 | 3-5×106/毫升 | 局部(注入卵巢组织) | 人数 =60 | ↓ 血清 FSH 水平 & ↑ 血清 E2 和 AMH | 更年期症状消失 |
| NCT02644447 | Ⅰ Ⅱ | 完全的 | 中国科学院 | UC-MSC 和带有可注射胶原蛋白支架移植的 UC-MSC | 10×106/毫升 | 局部(直接注射至双侧卵巢) | 人数 =23 | 安全性和耐受性 | 窦卵泡发育数量 及血清E2、AMH、FSH水平 及妊娠率 |
| NCT03816852 | 二 | 积极的 | 石诺生物科技有限公司 | 间充质干细胞 | 9×107/毫升 | 四号 | n=12 | 月经变化 | Kupperman 评分 & 卵泡发育 & 激素水平 |
| NCT03069209 | Ⅰ Ⅱ | 积极的 | 阿拉伯干细胞 | 骨髓间充质干细胞 | 不适用 | 四号 | 人数 =50 | 月经周期恢复 | |
| NCT03877471 | 我 | 积极的 | 中国科学院 | 胚胎干细胞衍生的MSC样细胞 | 3组,每个卵巢低剂量(0.2×107)、中剂量(0.5×107)、高剂量(1.0×107)细胞注射 | 局部(注射至双侧卵巢 | 人数 =28 | 无法使用 | 怀孕、FSH 水平、卵泡功能和子宫内膜厚度增加 |
| NCT05308342 | 不适用 | 招聘 | 丁丽君,南京大学 | 间充质干细胞 | (5×106) 和 (10 × 106) 细胞 | 局部(注入卵巢组织) | 人数=66 | 卵泡发育率 | 卵巢血流指数变化与临床妊娠率 |
| NCT04815213 | 我 | 招聘 | 约旦大学 | 骨髓间充质干细胞 | 20×106/子房 | 局部(注入卵巢组织) | n=10 | 治疗中出现的不良事件的发生率 | 荷尔蒙概况、卵巢变化和子宫内膜变化 |
| NCT02696889 | 不适用 | 招聘 | 伊利诺伊大学芝加哥分校 | 骨髓干细胞 | 不适用 | 局部(注入卵巢组织) | n=3 | 提高诊断荷尔蒙水平 | 改善荷尔蒙水平、恢复月经和成功怀孕 |
| NCT00353197 | 不适用 | 招聘 | 哈达萨医疗组织 | hESC 系的衍生 | 不适用 | 不适用 | n=80 | 不适用 | 不适用 |
| NCT02603744 | Ⅰ Ⅱ | 未知 | 伊朗鲁瓦扬研究所 | AD-MSCs | 3 组,其中(5 × 106), (10 × 106) 和 (15 × 106) 细胞 | 局部(注入卵巢组织) | n=9 | 卵巢肿块 | 荷尔蒙状况 & 窦卵泡数量 & 窦卵泡体积 & 月经复发率 & 怀孕率 |
| NCT03033277 | Ⅰ Ⅱ | 未知 | 中国科学院 | 间充质干细胞 | 不适用 | 局部(注入卵巢组织) | 人数 =320 | 成熟卵泡数 | 荷尔蒙概况、卵巢体积和怀孕率 |
| NCT01742533 | Ⅰ Ⅱ | 未知 | 深圳市北科生物科技有限公司 | UC-MSC 和 hCBMNC | 不适用 | 不适用 | 人数 =40 | 血清促卵泡激素水平 | 子宫和卵巢特征以及不良事件和严重不良事件的发生率 |
| NCT02062931 | Ⅰ Ⅱ | 未知 | 赛义德·巴克里 | BM-MSC 悬浮在富含血小板的血浆 (PRP) 中 | 3-5×106/毫升 | 局部(注射到卵巢组织和韧带) | 人数 =60 | 血清 FSH 水平降低,血清 E2 和 AMH 水平升高 | 荷尔蒙评估、更年期症状的临床消失和怀孕率 |
干细胞治疗卵巢早衰的潜在机制
干细胞可能是治疗管理卵巢早衰患者中缺失的一块拼图(图1、图2)。间充质干细胞在动物模型中的成功结果提高了我们对这些细胞的期望。MSC的功能可以归因于多种机制,包括自我归巢和分化到某个阶段。激活休眠细胞并鼓励它们重新进入细胞周期,是间充质干细胞的另一个特性。间充质干细胞能够迁移到卵巢,并且研究表明卵巢生态位可以吸引来自不同来源的不同类型的干细胞。
间充质干细胞通过细胞融合和旁分泌因子(如细胞因子、生长因子和激素)恢复受损细胞,并将其基因和细胞器(如线粒体)传递给受损细胞。线粒体移植作为一种有前途的治疗策略,不仅被认为可以修复线粒体损伤,还可以调节靶细胞的存活、增殖和分化。最近,一些研究报道,线粒体从干细胞转移到受损细胞可被视为组织损伤的治疗策略。在这些条件下,受损细胞能够从干细胞捕获健康线粒体以产生ATP,并减少炎症反应和细胞凋亡。
间充质干细胞可通过调节受损的环境和不足的生长因子替代、血管再生以及生殖细胞或卵泡的恢复来恢复卵巢功能。间充质干细胞在POI疾病中的各种治疗机制是通过不同的信号通路介导的。
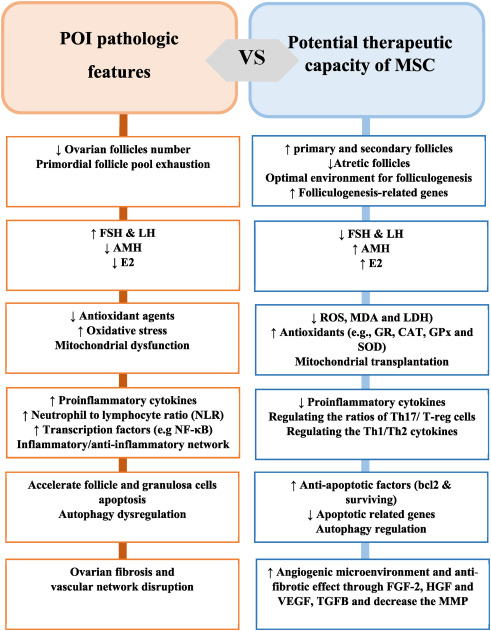
支持间充质干细胞治疗卵巢早衰疾病的临床前和临床证据
卵泡发生和激素调节作用:研究表明,BM-MSC和AD-MSC等MSC可以恢复化疗引起的卵巢损伤,并可以诱导卵泡发生的最佳环境。增加具有正常结构的卵泡数量是间充质干细胞的主要治疗作用。间充质干细胞还可以挽救受损卵巢中的原始卵泡数量并促进卵泡发生。
抗氧化作用:有证据表明,MSC的抗氧化作用可以通过减少ROS、增强宿主抗氧化防御、免疫调节机制、线粒体功能改善以及包括VEGF、HGF和血红素加氧酶-1 (HO-1) 在内的多种因子的分泌来证明(a具有强抗氧化和抗凋亡特性的应激诱导酶),以及PI3K/Akt、FOXO3a、MAPK 和核因子-红细胞2相关因子2 (Nrf2)-ARE途径的激活。间充质干细胞通过其强大的抗氧化和免疫调节作用似乎具有有吸引力的治疗潜力(图1,图2)。
抗炎作用:间充质干细胞通过细胞间接触和可溶性介质,可以调节免疫反应并最大限度地减少炎症相关的组织损伤。据报道,间充质干细胞移植后可最大限度地减少炎症对卵泡的不利影响并提高卵母细胞质量。MSC对POI的有益作用已显示出PI3K/pAkt 和过氧化物酶体增殖物激活受体γ (PPAR-γ) 等多种途径的参与。
对自噬的影响:间充质干细胞增强或抑制自噬途径的能力仍不清楚。据报道,hUC-MSCs中表达的HO-1可以通过激活JNK/Bcl-2信号通路调节的自噬来恢复POI小鼠模型的卵巢功能。
抗凋亡作用:卵巢细胞中MSC的抗凋亡作用与某些因子(例如VEGF、HGF、表皮生长因子 (EGF) 和IGF-1)的产生、外泌体miRNA的分泌、细胞凋亡的调节有关相关基因,包括Bcl-2、Bax、Caspase3,以及ROS产生的下调。
血管生成和抗纤维化作用:间充质干细胞作为血管生成调节剂,通过分化为内皮细胞和血管平滑肌或释放促血管生成因子,如VEGF、基质细胞衍生因子1 (SDF1)、 IGF、单核细胞趋化蛋白-1(MCP-1)和FGF-2(图1、图2)。VEGF和IGF-1与受体结合后,可以通过PI3K/Akt和GSK3β/β-catenin途径修复卵巢血管,增强卵泡形成,改善受损卵巢的结构和功能。SDF1参与MSC向血管内皮细胞的分化。
干细胞治疗卵巢早衰长期的影响
除了POI的短期影响外,过早停用雌激素还会影响作为雌激素作用主要靶点的各种器官。这些影响表现为各种疾病,如心血管疾病(CVD)、骨质疏松症、代谢综合征(MetS)和认知障碍。心血管疾病是导致POI患者预期寿命缩短的主要原因。
因此,这些患者的候选治疗方案最好也能解决这些问题。虽然目前还没有一项全面的研究来探讨间充质干细胞对POI患者长期并发症的治疗效果,但由于间充质干细胞的独特性质,我们认为间充质干细胞除了对卵巢功能有治疗作用外,还可以被认为是治疗这些患者上述长期并发症的合适候选药物。下文将讨论我们的假设。
由于雌激素对胆固醇代谢、减少冠状动脉收缩和动脉粥样硬化斑块的影响,POI女性雌激素水平低可能是增加这些患者心血管疾病风险的一个因素。
间充质干细胞是心脏修复的有效介质,通过刺激修复机制,如免疫调节作用、纤维化抑制、心脏干细胞增殖和心肌细胞分化以及促进细胞凋亡抵抗(图1、图2)。因此,间充质干细胞治疗心脏病患者的可行性和安全性已在多项已完成和正在进行的临床试验中进行了测试,其结果表明间充质干细胞可以改善这些患者的相关临床参数。
骨质疏松症是一种全身性代谢性骨病,其特征是骨质量下降和微结构退化。研究表明骨质疏松症与绝经后雌激素缺乏有直接关系。研究还表明,POI患者的峰值骨量 (PBM) 形成和骨矿物质密度 (BMD) 状态受到低雄激素血症和低雌激素血症的影响。骨质疏松症的主流治疗是通过药物干预刺激成骨或抑制进一步骨吸收。然而,此类治疗无法逆转现有的骨质流失,并且可能会产生副作用,包括颌骨坏死、癌症、血栓栓塞事件和中风。间充质干细胞移植的临床前研究通过成骨分化、血管生成诱导以及骨重塑、形成和吸收之间的协调提供了骨愈合的证据(图1)。
代谢综合征是一种复杂的临床病症,已成为一种威胁性的全球流行病。与正常人相比,受代谢综合征影响的人更有可能患上糖尿病、癌症、骨质流失、心血管并发症和非酒精性脂肪肝 (NAFLD) 等疾病。目前的医疗实践无法为诊断出患有这种综合征的患者提供解决方案。研究发现MSC对多个代谢综合征具有积极影响,并且已被证明是安全有效的。
间充质干细胞治疗卵巢早衰患者中的临床应用
基于间充质干细胞在POI动物模型中的良好治疗效果和一些临床前研究,在POI患者中进行了大量研究间充质干细胞治疗卵巢功能不全的疗效和安全性的临床试验。
第一项临床研究表明,由于卵巢恢复现象,骨髓间充质干细胞移植可能成为POI女性的一种有前景的治疗方法。使用骨髓间充质干细胞可使诊断为POI的女性实现卵泡再生、AMH水平升高并成功怀孕。
其他几项研究报告了骨髓间充质干细胞在一些POI患者中的潜在用途。两项针对10名和30名POI女性的研究报告了类似的方法,表明在自体间充质干细胞移植后恢复了月经并成功怀孕。
根据上述令人鼓舞的数据,除骨髓间充质干细胞之外的其他来源的干细胞也显示出与解决卵巢功能不全有关的类似结果。
中国科学院动物研究所干细胞与生殖生物学国家重点实验室在Cell Prolif 杂志上发表了一篇题为《人脐带间充质干细胞异体移植治疗卵巢早衰的临床分析》的文章。研究人员移植注射GMP临床级脐带间充质干细胞(UCMSCs)到POI患者卵巢,长期随访发现脐带间充质干细胞能够有效地恢复卵巢功能,促进卵母细胞成熟。经体外受精(IVF)和胚胎移植后,4例患者在移植后成功受孕,婴儿均发育正常。

最重要的是,研究结果表明,脐带间充质干细胞移植在一定程度上通过增加卵泡发育和改善卵细胞收集,挽救了POI患者的卵巢功能。此外,闭经时间较短的患者似乎更有可能从治疗中获益,而基本的卵巢状况(如术前胃窦卵泡)是影响干细胞治疗结果的另一个重要因素。
间充质干细胞的良好安全性已在不同的临床应用(例如不孕症)中得到证明。尽管有限的小样本试验表明间充质干细胞在POI女性中一年多的安全性,但长期安全性和不良事件有限。
因此,进一步全面、更大规模的临床研究对于建立标准化制剂并确保间充质干细胞治疗生殖系统的安全性至关重要。
结论和未来展望
卵巢早衰不仅会影响女性的生育能力,还会影响她们的心理健康和其他器官的功能。尽管做出了许多努力,但迄今为止还没有适当的治疗方法。鉴于其免疫原性低、易于获取以及体外大量复制的可能性,干细胞可以被认为是卵巢早衰患者新的有希望的治疗候选者。
临床前数据表明,干细胞可以通过其抗炎、抗氧化、抗凋亡、抗纤维化和血管生成等多种保护机制,迁移到受损的卵巢并改善卵巢功能。然而,干细胞在这种特殊疾病中的确切机制尚未被揭示,并且在临床应用之前应解决一个瓶颈。
移植的间充质干细胞在正常和炎症状态下不同水平的生理免疫反应中的功能、适当的剂量和给药方法、间充质干细胞的寿命和免疫调节活性的稳定性是一个尚未得到解答的重要问题。此外,将间充质干细胞与药物方法或补充间充质干细胞特性的替代细胞类型结合使用可被视为其他潜在策略。目前,可以肯定的是,该研究提供了一个干预卵巢早衰切实可行的治疗方法。
参考资料:https://doi.org/10.1016/j.heliyon.2023.e23271
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号