概述:本文综述了近年来间充质干细胞在治疗骨关节炎中的作用研究,深入探讨其优势并探索潜在的发展方向,旨在为该关键领域的未来研究提供新的见解。
骨关节炎(OA)是一种慢性退行性关节疾病,常见于老年人、绝经后妇女、运动员以及患有糖尿病和高脂血症等代谢性疾病的人。其临床表现包括疼痛、关节僵硬、肿胀、畸形、捻发音和活动受限。OA不仅严重影响患者的生活质量,而且是导致老年人残疾的主要原因。随着全球人口老龄化趋势,OA正成为全球健康的重大威胁。
目前治疗骨关节炎的方法包括物理治疗、药物干预和外科手术。药物干预主要旨在抗炎和镇痛作用,缺乏修复或逆转骨关节炎相关关节损伤的能力。近年来,白细胞介素1(IL-1)受体拮抗剂、阿达木单抗(TNF抗体)等生物制剂逐渐纳入OA治疗;然而,多项临床试验未能证明显着改善。此外,支持物理疗法治疗OA疗效的证据仍无定论。全关节置换术和关节置换术等手术干预对于晚期OA患者来说是可行的选择,可以缓解疼痛并改善关节功能。然而,人工植入物的有限寿命和可变的长期结果,加上潜在的并发症,强调了骨关节炎患者关节损伤修复的明确治疗方式的缺乏。
令人鼓舞的是,最近的研究揭示了干细胞在治疗骨关节炎中的潜在作用。间充质干细胞(MSC)具有自我更新能力,来源于中胚层胚层,可以从骨髓、脂肪组织、滑膜、脐带、牙髓、羊水、真皮和外周血中采集。间充质干细胞表现出向成骨和软骨形成谱系的多谱系分化潜力,并分泌免疫调节因子、细胞因子、生长因子、细胞外囊泡(EV)和其他生物活性物质,从而有助于组织稳态和再生,并发挥免疫调节功能。
目前,大量临床前和临床研究支持OA动物模型和患者接受基于MSC的干预后,临床症状得到显着改善,受损软骨得到修复。在本文中,我们讨论了干细胞治疗骨关节炎的最新进展,阐明了干细胞治疗作为治疗骨关节炎的新方法的现状。
骨关节炎的发病机制
OA的发病与软骨代谢失衡、软骨下骨硬化和滑膜炎症密切相关,涉及巨噬细胞、T细胞、软骨细胞、破骨细胞和成纤维细胞等多种细胞类型。衰老、创伤、肥胖、生物力学、昼夜节律改变等因素可导致软骨细胞肥大或凋亡、代谢紊乱、细胞衰老、软骨稳态破坏,从而促进OA的发生。
在OA的早期阶段,软骨细胞中的线粒体功能障碍导致活性氧 (ROS) 过量产生,从而诱发氧化损伤。该过程通过激活磷脂酰肌醇-3-激酶 (PI3K)/蛋白激酶 B (Akt)和Caspase途径触发软骨细胞凋亡。软骨细胞的代谢紊乱,例如葡萄糖转运蛋白(GLUT1)的过度表达,导致葡萄糖摄取增加和晚期糖基化终产物的过量产生,最终导致软骨退化。脂质代谢和胆固醇调节的异常也导致OA的发病机制。
各种炎症和趋化因子,包括粒细胞-巨噬细胞集落刺激因子(GM-CSF)、IL-1、IL-6、IL-7 和 IL-8、单核细胞趋化蛋白-1(MCP-1)、MCP-2、MMP1、MMP3、MMP10 和 MMP13,可破坏干细胞或祖细胞诱导的组织再生,引起邻近细胞衰老,促进OA进展,并导致疼痛和活动障碍等症状。
炎症细胞的招募和激活是OA发病和发展的关键因素。单核细胞/巨噬细胞系细胞分化成破骨细胞后聚集在软骨下板,引起软骨下骨和关节软骨的灶性变性,导致软骨损伤。在76%的OA患者膝关节中,活化巨噬细胞聚集,其数量与OA的严重程度和关节症状(如疼痛、关节间隙变窄和骨质增生形成)相关。此外,巨噬细胞还能产生神经生长因子(NGF),导致OA疼痛。巨噬细胞分泌B细胞活化因子(BAFF),促进促炎细胞反应(Th1 和 Th17),抑制抗炎细胞反应(Th2)。OA晚期的滑膜纤维化是导致关节僵硬、滑膜增生和功能受限的关键因素。
间充质干细胞治疗骨关节炎的机制
间充质干细胞是源自中胚层的具有自我更新能力的多能干细胞。它们表达表面标志物,包括CD73、CD90 和CD105,但缺乏造血分化标志物的表达,例如CD11b、CD14、CD34、CD45、CD19、CD79a或HLA-DR。
间充质干细胞在治疗自身免疫性疾病和组织/器官修复方面已表现出显着的功效。在骨关节炎治疗中,间充质干细胞在几个方面发挥着关键作用(图1)。
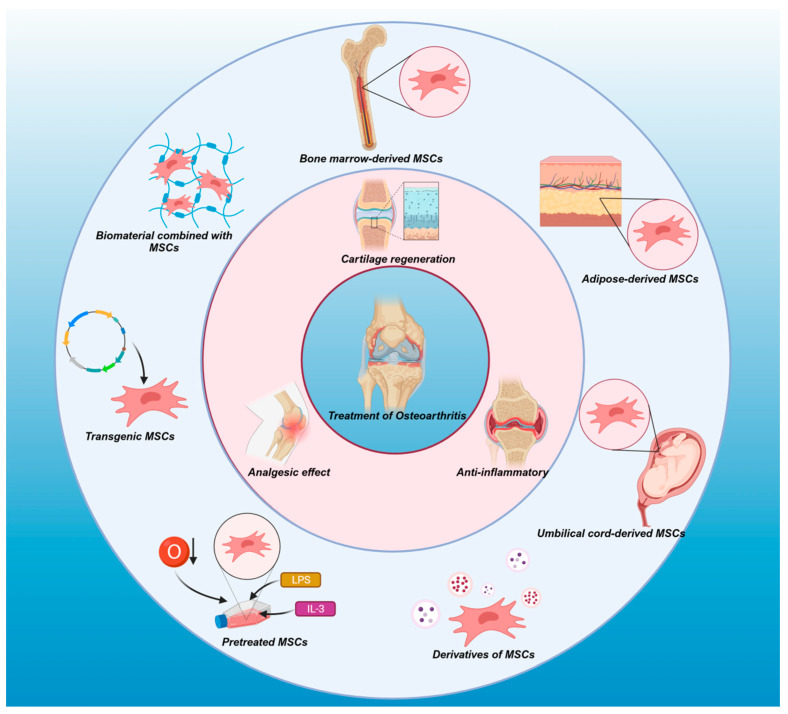
图1:不同来源的间充质干细胞(MSC)——包括衍生物、预处理的间充质干细胞和转基因间充质干细胞,以及与间充质干细胞结合的生物材料——有助于软骨再生、抗炎反应、免疫调节和镇痛作用。这些多功能应用使 MSC 成为骨关节炎 (OA) 的潜在治疗剂,为减缓 OA 的进展提供了前景。
软骨再生
间充质干细胞具有促进软骨形成和修复的能力。间充质干细胞可以通过分化成软骨细胞或刺激现有软骨细胞中软骨形成激素的上调来实现这一目标。在OA的背景下,间充质干细胞可以从软骨下骨迁移到受损区域,分化为软骨细胞和成骨细胞,以修复软骨和软骨下骨组织。
抗炎和免疫调节作用
OA致病机制的一个重要方面涉及促炎细胞因子和抗炎细胞因子之间的相对拮抗作用。IL-1β和TNF-α等促炎细胞因子可以独立或与其他细胞因子协同驱动炎症反应。在炎症刺激下,受损的滑膜细胞或其他细胞释放IL-1β、IL-6、IL-8、TNF-α和具有血小板反应蛋白结构域的MMP以及具有血小板反应蛋白基序的解整合素和金属蛋白酶(ADAMTS)。
间充质干细胞具有特定的免疫调节特性,产生免疫调节物质,下调免疫炎症过程并促进组织再生,减轻关节炎炎症。在OA治疗中,MSC通过抑制成熟树突状细胞的发育、抑制IL-2诱导的自然杀伤(NK)细胞增殖以及降低NK细胞的细胞毒性来抑制先天免疫反应。MSCs抑制细胞凋亡,减缓T细胞和B细胞的发育,并调节适应性免疫。间充质干细胞促进巨噬细胞/小胶质细胞从炎症(M1)表型向抗炎(M2)表型的转变。此外,MSC通过分泌TGF-β和IL-6抑制NK细胞的炎症反应。
间充质干细胞的镇痛作用
疼痛是骨关节炎的主要表现,显着影响患者的功能和生活质量。近年来,研究人员发现间充质干细胞治疗骨关节炎不仅能促进软骨恢复,还能显着减轻疼痛、改善功能。环氧合酶2/前列腺素 E2 (PGE2)通路与 OA 中BM-MSC的镇痛机制有关。
王等人还发现源自经TGF-β1修饰的MSC的外泌体通过抑制血管生成、抑制软骨细胞钙化和破骨细胞活性,减轻OA中的软骨损伤和疼痛。
杨教授团队报告了脐带间充质干细胞治疗44例严重膝骨关节炎(KOA)的临床研究结果。研究显示,视觉模拟量表(VAS)评分、美国膝关节协会评分(AKS)关节评分、AKS功能评分在治疗后3、6、12个月均显着降低,表明脐带间充质干细胞移植治疗严重骨关节炎可以与透明质酸钠相比,能更迅速、显着、持久地缓解关节疼痛,改善关节功能。
在一项I/IIa期试验中,晚期KOA患者接受了单次关节内注射1、10或5万个BM-MSC。与基线相比,患者的疼痛、症状、生活质量以及西安大略和麦克马斯特大学关节炎指数 (WOMAC) 总体评分显着改善。森特诺等人。通过24周的随访磁共振成像(MRI)监测观察发现,自体骨髓间充质干细胞移植可以刺激软骨生长并减轻退行性关节疼痛。
不同来源的间充质干细胞治疗骨关节炎中的应用
不同来源的间充质干细胞表现出不同的特点,具有独特的优势。骨髓和脂肪组织是治疗性MSC的主要来源。其中,UC-MSCs含量最高,来源于脐带和羊膜的MSCs表现出更强的增殖能力。此外,来自脐带、羊膜和脂肪组织的MSC比BM-MSC表现出更高的免疫调节能力,其中胎盘MSC的免疫调节强度最低,但能够分泌更多的细胞生长因子。
骨髓间充质干细胞治疗骨关节炎
BM-MSCs是最广泛使用的治疗性MSCs来源,具有易于获取、细胞增殖快速、分化能力维持能力强以及免疫排斥风险最小等优点。
Lamo-Espinosa JM团队进行的一项临床试验中,招募了55名接受部分半月板切除术的患者,治疗组同时使用了低剂量和高剂量的同种异体BM-MSC。2年随访显示没有临床不良反应,并且根据VAS和WOMAC评分,观察到疼痛显着减轻。分析使用自体BM-MSC的两项关键试验的结果,发现细胞应用后1年获得的 WOMAC反应持续2年和4年,为MSC治疗OA的长期疗效提供了证据。
脂肪源性间充质干细胞 (AD-MSC)
AD-MSCs通常来源于脂肪组织,具有来源丰富、易于采集、创伤小、并发症发生率低、增殖潜力高等特点。AD-MSCs分泌抗炎因子,如IL-10和IL-1,抑制炎症或促进CD4+FOXP3+T辅助细胞的表达。它们可以抑制滑膜巨噬细胞活化,减少炎症因子的分泌,并抑制炎症反应。在免疫系统中发挥调节作用。
在一项旨在评估胫骨内侧开放楔形高位截骨术 (MOWHTO) 关节内注射AD-MSC后软骨缺损再生、功能改善和安全性的随机对照试验中,26名患者被分为ADMSC注射组(n=13)和对照组(n=13)。主要结果是通过定期MRI评估软骨缺陷的持续变化。连续MRI显示AD-MSC组的软骨再生明显优于对照组。在任何病例中都没有发生与治疗相关的不良事件、严重不良事件或术后并发症,这表明关节内注射AD-MSCs可能是MOWHTO后疾病改善的一种有前途的治疗方法。
间充质干细胞
UC-MSCs具有细胞年轻、产量大、增殖特性高、多向分化潜力、免疫原性低等优点。UC-MSCs可以下调软骨降解酶的表达,抑制软骨降解,刺激受损软骨细胞增殖,防止软骨退化。它们还抑制促炎细胞因子,如 TNF-α、IL-1β、TNF-α刺激蛋白6和IL-1受体,从而减少炎症并保护关节软骨。
JuY等人的研究。证明UC-MSCs的增殖能力高于AD-MSCs,并且两种类型的细胞均显着减少ACLT手术诱导的OA的发展。在2020年对双侧KOA患者进行的I期试点研究中,关节内注射UC-MSC导致VAS、SF-36和WOMAC评分改善。
用于治疗骨关节炎的间充质干细胞衍生物
越来越多的研究发现,旁分泌信号传导是干细胞发挥作用的关键机制。间充质干细胞可以分泌多种生长因子和营养物质,促进自身分化为软骨细胞,刺激常驻软骨细胞的增殖和生长,并分泌抗炎和免疫调节因子来调节受损的组织微环境,促进组织再生。
MSC的旁分泌作用是由细胞外囊泡(EV)的分泌介导的。EV包含细胞释放的各种膜结合囊泡结构。根据其大小和生物发生,EV可分为三种亚型:外泌体、微泡和凋亡小体。外泌体是一种亚型,其特征是哺乳动物中各种活性细胞自发产生和分泌的纳米级(40-100nm)囊泡。
与MSC相比,EV保留了相似的生物学特性,但具有生物相容性、低免疫原性、长期稳定性和易于储存等优势。源自BM-MSC的EV可以通过抑制NF-κB通路缓解关节炎症。来自AD-MSC的那些可以通过抑制PI3K/Akt/mTOR通路来保护软骨并减轻炎症。研究发现外泌体miR-92a-3p可以促进软骨细胞的增殖和分化,减少软骨退化,并激活MMPs,从而改善OA。
外泌体miRNA可以介导细胞间通讯和基因调控,包括软骨形成和退化的调控,使其成为治疗OA的无细胞 MSC疗法的理想替代品。除了具有再生软骨的能力外,EV还可以通过增加软骨细胞标志物的表达并同时抑制退化相关基因(包括ADAMTS-5和MMP-13)的表达来延长IL-1β诱导的退变软骨细胞的存活。这有助于上调Col2并重新合成细胞外基质 (ECM)、保护软骨、防止软骨细胞肥大并避免软骨细胞去分化。
MSC-ECM也是一种非细胞成分,含有MSC分泌的各种大分子。在去除 DNA 等引发免疫反应的细胞成分后,ECM保留了天然的生化和生物物理信号。普拉塔斯等人。发现 AD-MSC 的条件培养基可以下调 OA 软骨细胞中IL-1β的产生。
另一种值得注意的细胞疗法是骨髓抽吸浓缩物(BMAC)。该疗法因其成分而引人注目,其中包括多种细胞成分,例如血小板、单核细胞和间充质干细胞。在临床上,BMAC越来越多地被用作肌肉骨骼病理状况的再生疗法,尽管其基于证据的支持仍然有限。多项临床试验表明,BMAC疗法可有效减少OARSI间歇性和持续性关节疼痛以及双侧膝关节VAS疼痛评分。此外,在短期随访期间,KOA患者的疼痛和患者报告的结果有所改善。
间充质干细胞新技术的应用
预处理
间充质干细胞表现出对环境的动态适应性,根据不同的条件调整其调节功能。为了增强 MSC 的体外和体内功能,基本策略包括预处理、基因修饰和优化MSC培养条件。这些程序的实施有望显着提高组织工程和再生医学中间充质干细胞移植的功效。
接受低氧预处理的间充质干细胞可以分泌更多的生物活性因子,包括血管内皮生长因子(VEGF)、肝细胞生长因子(HGF)、胰岛素样生长因子-1(IGF-1)和碱性成纤维细胞生长因子(bFGF) ,导致血管生成和成骨诱导增强。
基因工程
利用基因编辑技术敲除或沉默抑制干细胞成骨或软骨分化的基因以及转染有利于成骨或软骨分化的基因已成为干细胞再生医学领域的一种新颖的研究方法。用重组pIRES2-EG-FP-hBMP-2质粒转染诱导的人UC-MSC显示hBMP-2基因的稳定转录,表明干细胞成功分化为软骨细胞组织。在高血糖条件下,NLRP3的敲除对 AD-MSC 的旁分泌功能具有保护作用。这种保护是通过激活抗凋亡和抗ROS沉积机制来实现的。
间充质干细胞移植和新技术
间充质干细胞与生物材料的结合在治疗骨关节炎方面已显示出显着的疗效。其关键特征在于生物材料与间充质干细胞之间的相互作用,引导间充质干细胞分化为特定的细胞谱系。它们在OA模型中的联合应用已被证明可以促进透明样软骨再生,为MSC的多样化临床应用开辟新途径。
生物材料具有精确的形状和微观结构、性能稳定、无毒、具有良好的生物相容性。当与MSC一起植入软骨缺陷区域时,这些生物材料会降解,有助于MSC的软骨分化并促进新软骨的形成。
结论
间充质干细胞自进入科学视野以来就受到了广泛的研究,其在各种疾病中的作用也被广泛探讨。临床实验证实了间充质干细胞对治疗OA的积极作用。
此外,在使用间充质干细胞后或短期随访期间,几乎没有出现不良反应。虽然大多数研究都支持间充质干细胞疗法在治疗骨关节炎方面的积极作用,但一项第3期随机试验显示,在降低疼痛评分和改善MRI评分方面,BM-间充质干细胞与皮质类固醇相比没有明显优势。
虽然基础和临床研究前沿的进步还需要大量努力,但改进后的细胞疗法有望成为更安全、更经济、更有效的OA治疗方法。间充质干细胞的预处理、基因工程的改进以及与生物材料的结合,进一步扩大了基于间充质干细胞的治疗方法的优势,为治疗骨关节炎以及潜在的其他疾病提供了更多的途径。
未来,我们期待间充质干细胞在骨关节炎及其他领域得到更广泛的认可和应用。
参考资料:Chen Y, Cheng RJ, Wu Y, Huang D, Li Y, Liu Y. Advances in Stem Cell-Based Therapies in the Treatment of Osteoarthritis. Int J Mol Sci. 2023 Dec 28;25(1):394. doi: 10.3390/ijms25010394. PMCID: PMC10779279.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号