干细胞外泌体疗法治疗骨科疾病和创伤疾病
干细胞外泌体疗法治疗断裂
骨折是最常见的大器官外伤,大约10%无法正常愈合。骨折愈合涉及合成代谢组织膨胀阶段和分解代谢组织重塑阶段,该阶段受干细胞、先天性和适应性免疫功能以及稳定性等多种因素控制。骨折的生物药物治疗可以局部给予(例如骨形态发生蛋白,BMP)或全身给予(例如甲状旁腺激素,PTH)。作为一种有前途的替代方案,用于骨折愈合的外泌体疗法主要利用骨髓来源的MSC作为细胞供应者(表1)。
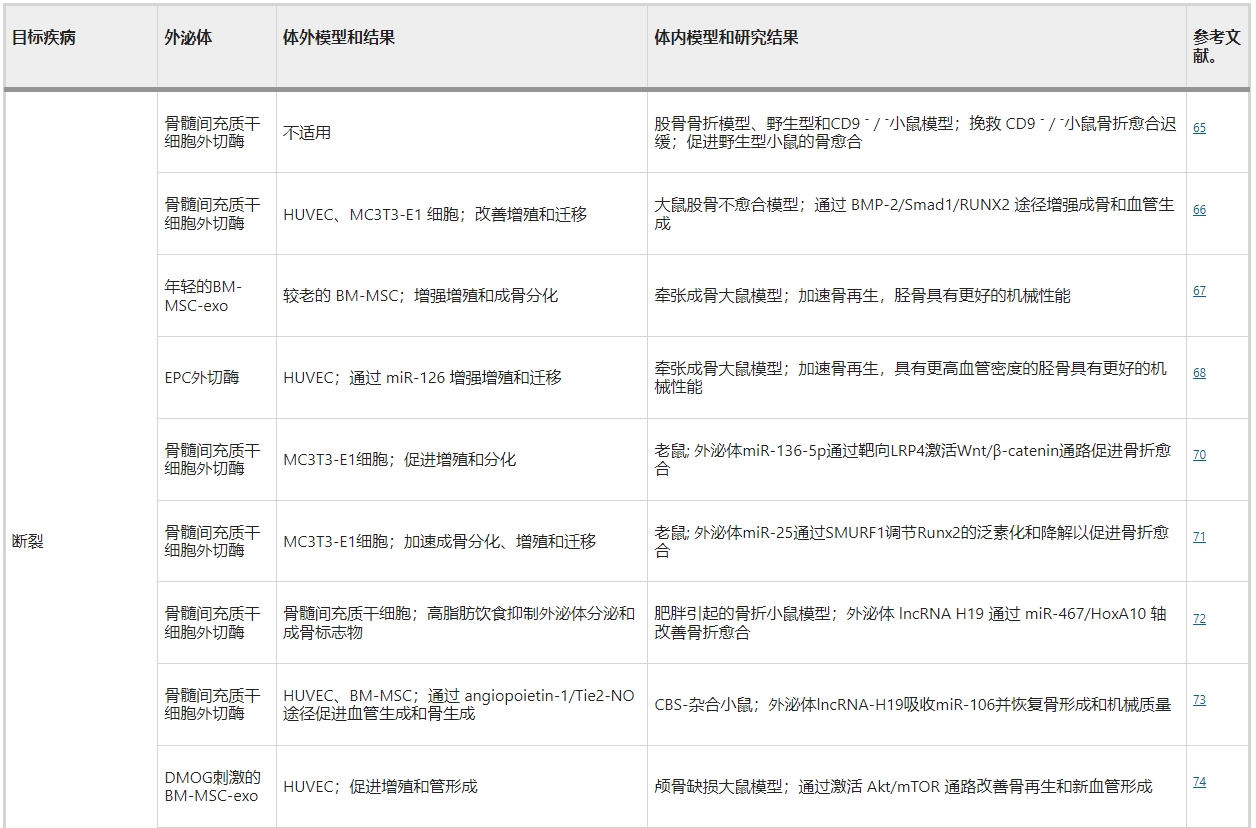
间充质干细胞来源的外泌体如何促进骨折愈合的推测机制如下。
- 首先,骨修复的进展需要多种细胞,例如炎症阶段的炎症细胞、纤维血管阶段的内皮和间充质祖细胞、骨形成期间的成骨细胞和软骨细胞、以及骨痂重塑期间的破骨细胞。
- 其次,大多数这些细胞可以摄取外泌体,特别是成骨细胞和血管内皮细胞,它们与骨折愈合最相关。
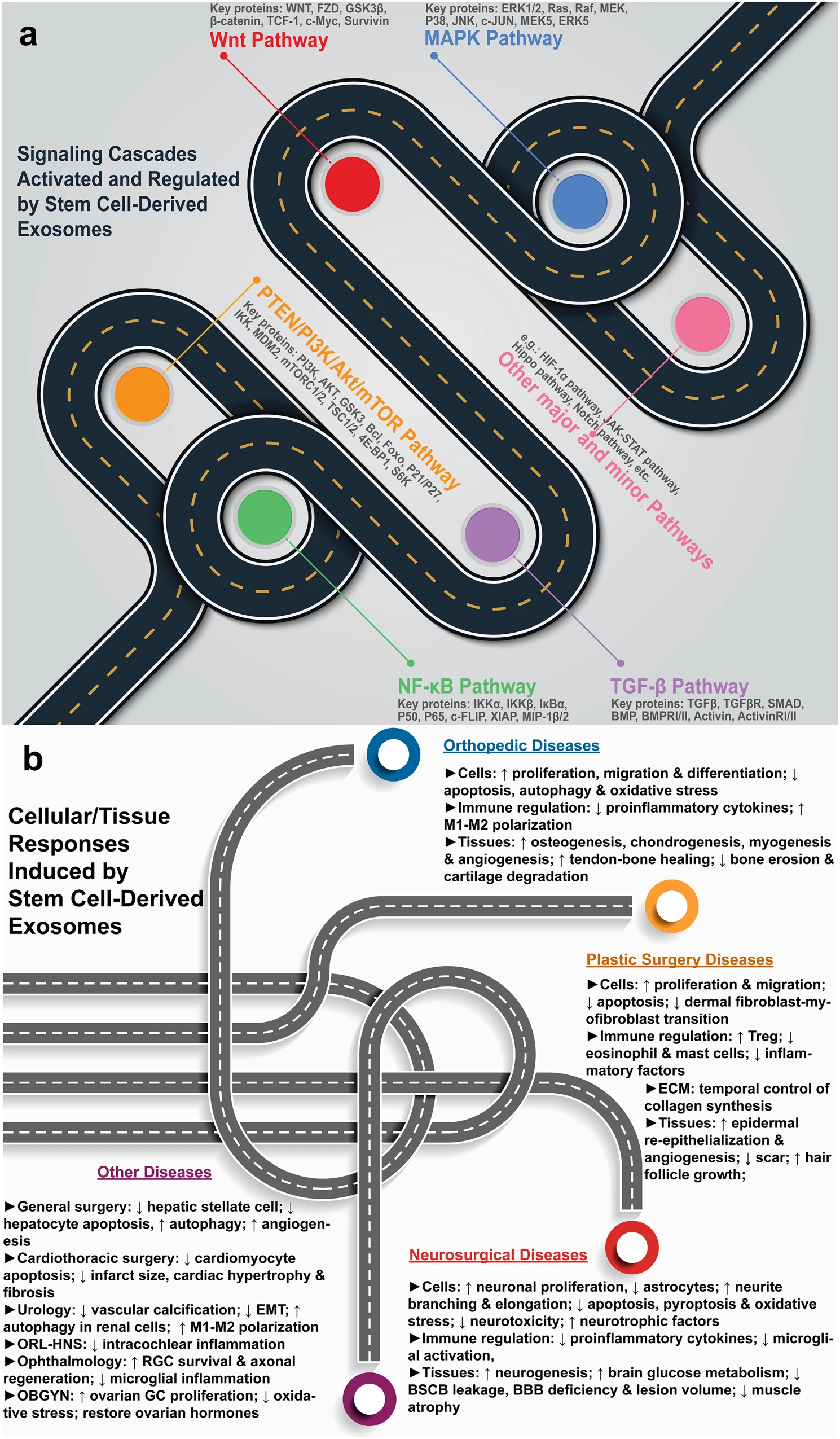
- 最后,外泌体吸收后,受体细胞的基因表达被改变,从而激活各种信号通路(图1a),引起各种细胞和组织反应(图1b)并最终改善骨折愈合。
干细胞外泌体疗法治疗骨关节炎
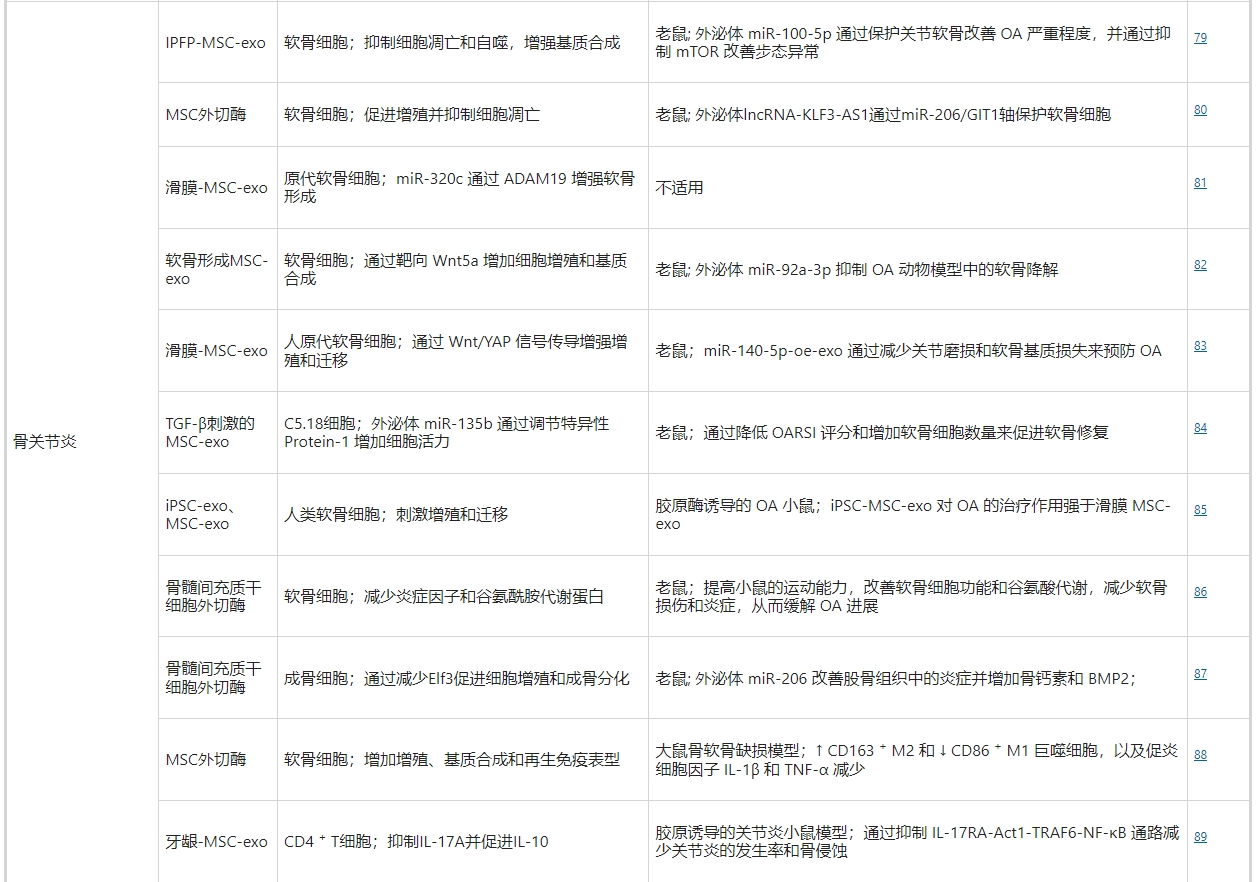
骨关节炎 (OA) 是成人最常见的关节疾病,也是成人活动受限的最常见原因,影响全球约2.4亿患者。OA的病理学已经从被视为仅限软骨发展为影响整个关节所有组成部分的多组织疾病,包括骨、滑膜、肌肉、韧带和关节周围脂肪。临床试验已成功揭示了可阻止结构进展(例如组织蛋白酶K和Wnt抑制剂)或减轻 OA疼痛(例如神经生长因子抑制剂)的全身化合物。作为骨关节炎的潜在治疗选择,大多数MSC衍生的外泌体疗法在体外模型中都使用软骨细胞作为靶标。这些MSC可能源自多种组织,如骨髓、滑膜、牙龈和髌下脂肪垫 (IPFP)。
一些关注软骨形成的研究表明对miRNA的作用特别感兴趣。吴等人发现IPFPMSC衍生的外泌体通过 miR100-5p调节的mTOR自噬途径抑制,保护骨关节炎小鼠的关节软骨免受损伤并改善步态异常。由于在诊所内通过关节镜手术很容易从骨关节炎患者体内回收人类IPFP,因此这种类型的外泌体疗法可能会简化并加速从实验室到临床的过程。
其他研究不仅关注软骨形成,还关注骨关节炎治疗期间的抗炎和免疫调节。例如,MSC来源的外泌体在体外抑制炎症因子、谷氨酰胺代谢活性相关蛋白、谷氨酰胺和GSH/GSSG比值,同时在体内改善小鼠的软骨细胞功能、组织炎症和运动能力,从而缓解骨关节炎进展。
目前,还没有一种“一刀切”的药物可以适合所有骨关节炎患者。缓解OA疾病的药物 (DMOAD) 可能成为下一代骨关节炎治疗方法。间充质干细胞衍生的外泌体治疗OA与DMOAD一致是非常有价值和相关的:两者都能够靶向炎症细胞因子、基质降解酶和Wnt通路。因此,DMOAD开发的新兴方法,例如基于miRNA的模式和靶向细胞衰老,也可能用于完善间充质干细胞外泌体治疗骨关节炎。
干细胞外泌体疗法治疗脊髓损伤
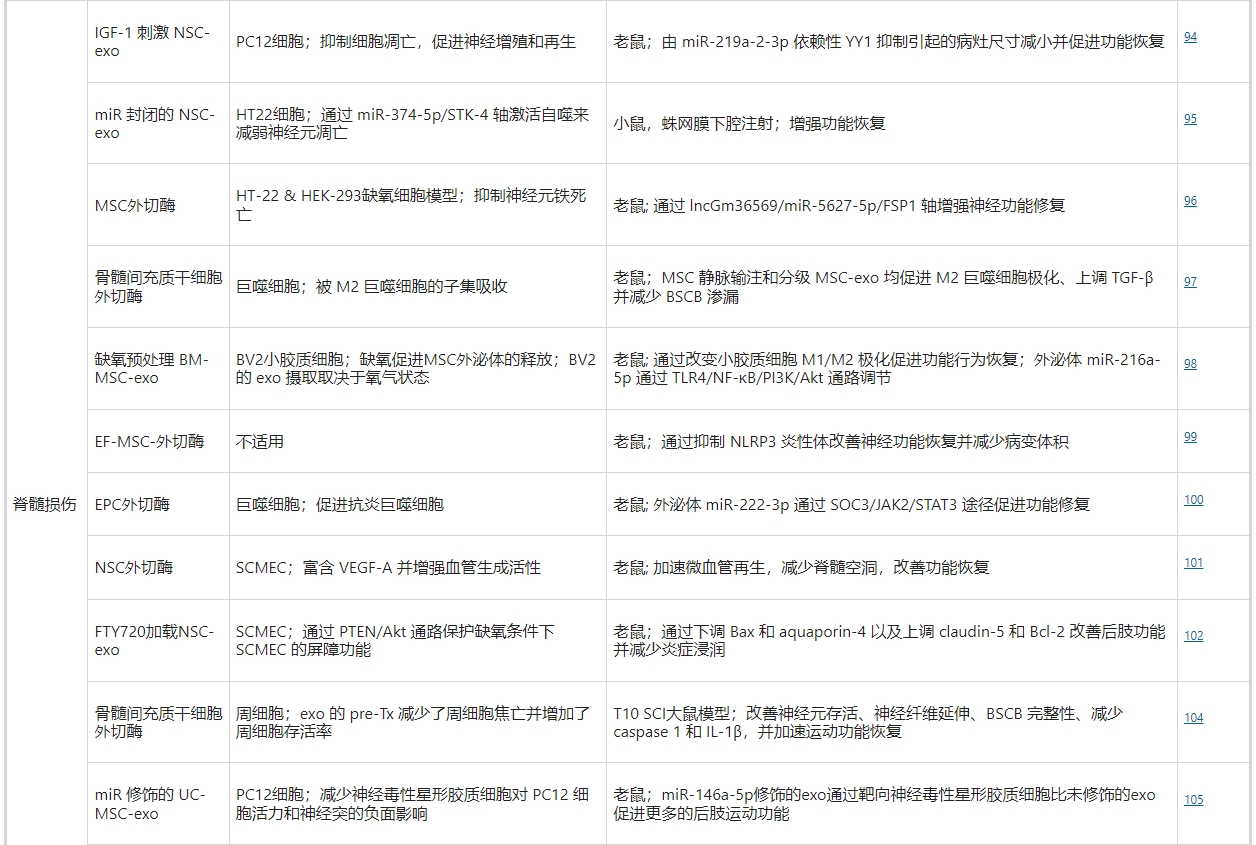
创伤性脊髓损伤(SCI)是一个毁灭性的全球健康问题,给患者和社会带来重大的功能和经济负担。SCI的病理生理学包括机械创伤引起的原发性损伤和以细胞凋亡、水肿、缺血、炎症细胞浸润和兴奋性毒性为特征的继发性级联损伤。尽管进行了手术干预,但涉及药物治疗的临床研究可大致分为神经保护性治疗或神经再生性治疗。针对上述机制链的每个事件,间充质干细胞和神经干细胞衍生的外泌体疗法都可以对脊髓保护和再生产生有益的影响。
一些研究小组以神经元细胞死亡为目标。马等人研究表明,胰岛素样生长因子 1 (IGF-1) 刺激的 NSC 衍生的外泌体可以抑制神经元凋亡,同时通过miR-219a-2-3p/YY1途径促进SCI后的功能恢复。或者,Zhang等人。发现蛛网膜下腔注射NSC来源的外泌体可以通过miR-374-5p/STK-4轴激活自噬来抑制神经元细胞凋亡,从而增强SCI的功能恢复。
干细胞外泌体疗法治疗肌肉和肌腱撕裂
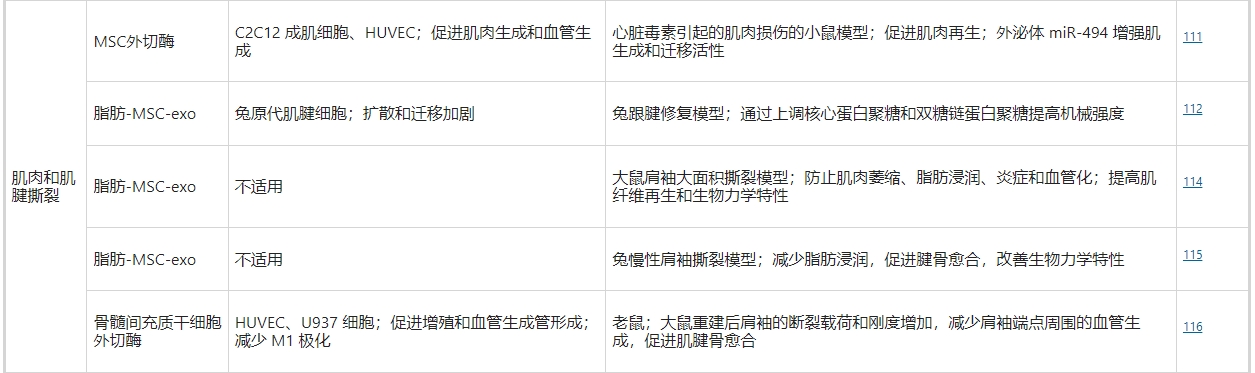
肌肉和肌腱撕裂可能由急性创伤(例如骨折)或慢性过度使用(例如运动损伤)引起。肌肉拉伤和肌腱撕裂的愈合遵循典型的伤口愈合过程,包括炎症、增殖和重塑阶段。已经尝试了多种非手术策略来改善愈合,包括基于细胞和生长因子的疗法。以下概念验证研究表明MSC衍生的外泌体可能成为下一代肌肉骨骼治疗方法。
在大量肩袖撕裂的大鼠模型中,外泌体疗法可以预防肌肉萎缩、炎症和血管化。在慢性肩袖撕裂的兔模型中,外泌体疗法可以防止脂肪浸润并改善生物力学特性。另一组报告称,骨髓间充质干细胞衍生的外泌体可以增加重建后肩袖的断裂载荷和刚度,诱导肩袖端点周围的血管生成,并促进肌腱-骨界面的生长。
干细胞外泌体疗法治疗其他骨科疾病
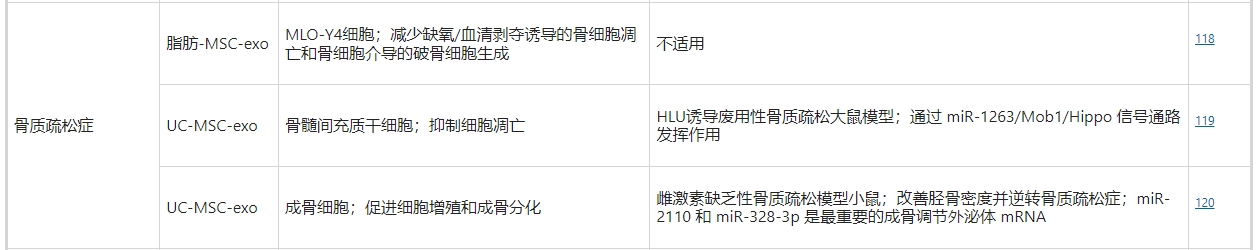
骨质疏松症是一种代谢性骨病,其特点是骨密度低和骨结构弱化,从而增加了骨折的风险。在一项细胞研究中,脂肪间充质干细胞衍生的外泌体可拮抗缺氧/血清剥夺诱导的骨细胞凋亡和骨细胞介导的破骨细胞生成。进一步的动物研究发现,脐带间充质干细胞衍生的外泌体可通过miR-1263/Mob1/Hippo通路抑制骨髓间充质干细胞凋亡并预防废用性骨质疏松症,通过miR-2110和miR-328-3p改善胫骨密度并逆转雌激素缺乏性骨质疏松症。
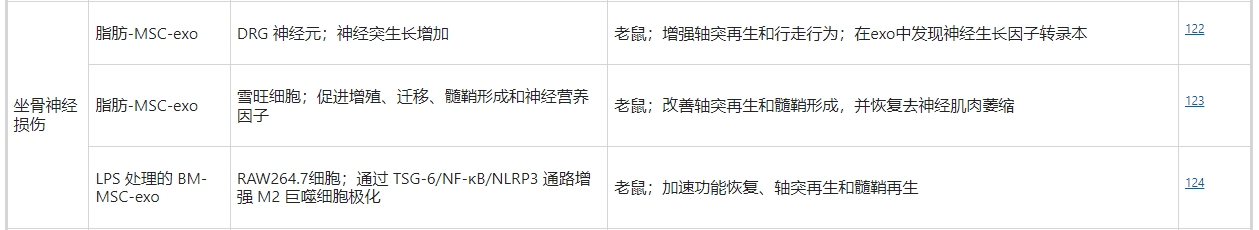
与SCI相比,周围神经损伤(如坐骨神经损伤)更为常见。研究表明,脂肪间充质干细胞衍生的外泌体可以靶向神经元,在体外促进神经元的神经突生长,在体内促进轴突再生和步行行为。经LPS预处理的间充质干细胞衍生外泌体可通过促进体外M2巨噬细胞极化来靶向炎症细胞,并加速体内周围神经再生。
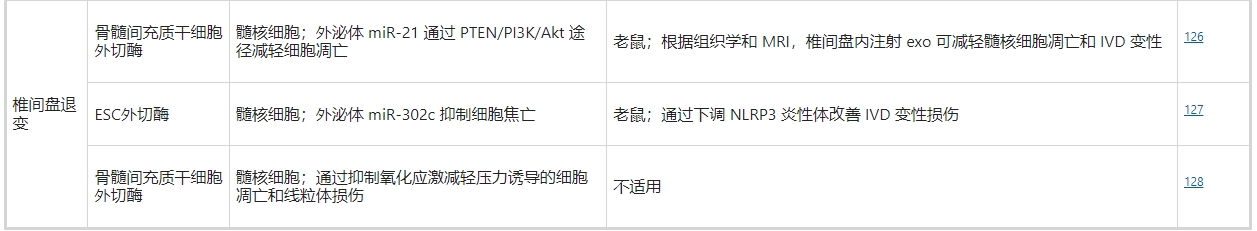
椎间盘(IVD)退化是导致下背痛的主要原因,也是全球残疾总生存年数的主要伤害。其分子过程包括细胞外基质(ECM)变性、炎症、氧化应激、细胞凋亡、衰老和自噬能力下降。新出现的外泌体疗法试图解决这些问题。
- Cheng等人证实,椎间盘内注射骨髓间充质干细胞衍生的外泌体可抑制髓核细胞(NPC)凋亡,并通过外泌体miR-21缓解IVD退化。除了细胞死亡和线粒体损伤外,间充质干细胞衍生的外泌体还能抑制NPCs中的氧化应激。由于IVD变性和OA具有共同的分子疾病谱,利用间充质干细胞衍生的外泌体治疗OA的积极结果可作为IVD变性研究的参考。
股骨头坏死(ONFH)又名股骨头缺血性坏死,是一种影响年轻人的致残性疾病,通常会导致全髋关节置换术。糖皮质激素(GC)诱导的骨坏死是股骨头坏死(ONFH)最常见的病因之一,其发病机制表现在两个方面:股骨头供血受损和成骨活性减弱。
- Liu等人研究发现,iPSC衍生的间充质干细胞外泌体可通过PI3K/Akt 通路促进血管生成和骨生成,从而预防GC诱导的ONFH。
参考资料:Tan, F., Li, X., Wang, Z. et al. Clinical applications of stem cell-derived exosomes. Sig Transduct Target Ther 9, 17 (2024). https://doi.org/10.1038/s41392-023-01704-0
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号