我国存在大量失代偿性肝硬化患者,主要由乙型肝炎病毒(HBV)感染引起。这些患者经历了不可逆转的肝硬化过程。脐带间充质干细胞(UC-MSCs)具有自我更新和多向分化的潜力,这使得治疗失代偿性肝硬化成为可能。
近日,我国研究人员利用人脐带间充质干细胞进行了一项治疗乙型肝炎病毒失代偿性肝硬化的临床研究,临床结果表明输注后,肝功能在短时间内得到改善。ALB在第57天和第85天增加,但在第169天下降到基线水平。从第29天到第157天,PTTA显着改善。IL-8在整个访视期间下降。由此可知hUC-MSCs在治疗HBV相关失代偿性肝硬化患者方面具有巨大潜力,且安全性满意。该综述发表在国际期刊杂志“Stem Cell Research&Therapy”上。

试验注册:该试验已在ClinicalTrials.gov上注册,注册 ID 为 NCT05442437。注册名称为“hUC-MSCs治疗HBV失代偿性肝硬化的临床研究”。该注册表于2022年7月1日发布。
肝脏是人体最重要、最复杂的器官之一。药物、酒精、病毒等因素都可能损害肝脏,导致肝炎、脂肪肝、肝硬化等肝病,是我国最常见的肝病。大多数失代偿性乙型肝炎肝硬化患者对常规治疗不满意。随着病情的发展,患者可能会出现肝性脑病、食管静脉曲张出血、肝功能衰竭、肝肾综合征等危及生命的严重疾病。
间充质干细胞(MSCs)由于具有多向分化潜能和良好的增殖能力,能够产生多种细胞因子和生长因子,还具有造血、免疫调节和抗炎功能,已被动物实验和临床证实。研究表明,我们认为间充质干细胞对于治疗乙型肝炎病毒性肝炎肝硬化失代偿具有很大的潜力,并且很适合细胞移植。
因此,我们设计本临床试验旨在探索乙型肝炎相关失代偿性肝硬化的新治疗方法。该临床试验的主要目的是调查输注脐带间充质干细胞移植治疗乙型肝炎病毒失代偿性肝硬化患者的存活率、肝功能的促进、健康的改善以及患者的安全性和耐受性。我们期待这项试验能为失代偿性肝硬化患者带来新的希望。
干细胞治疗能否改善乙型肝炎肝硬化患者的症状?24例患者长期随访告诉你答案
方法:招募24名参与者并分为3组。hUC-MSCs将通过外周静脉输注3次。进行24周的随访,包括检测肝功能、凝血功能、一般状况、免疫系统等,并记录不良事件。随后将进行1.5年的生存随访。
结果
注册和生存
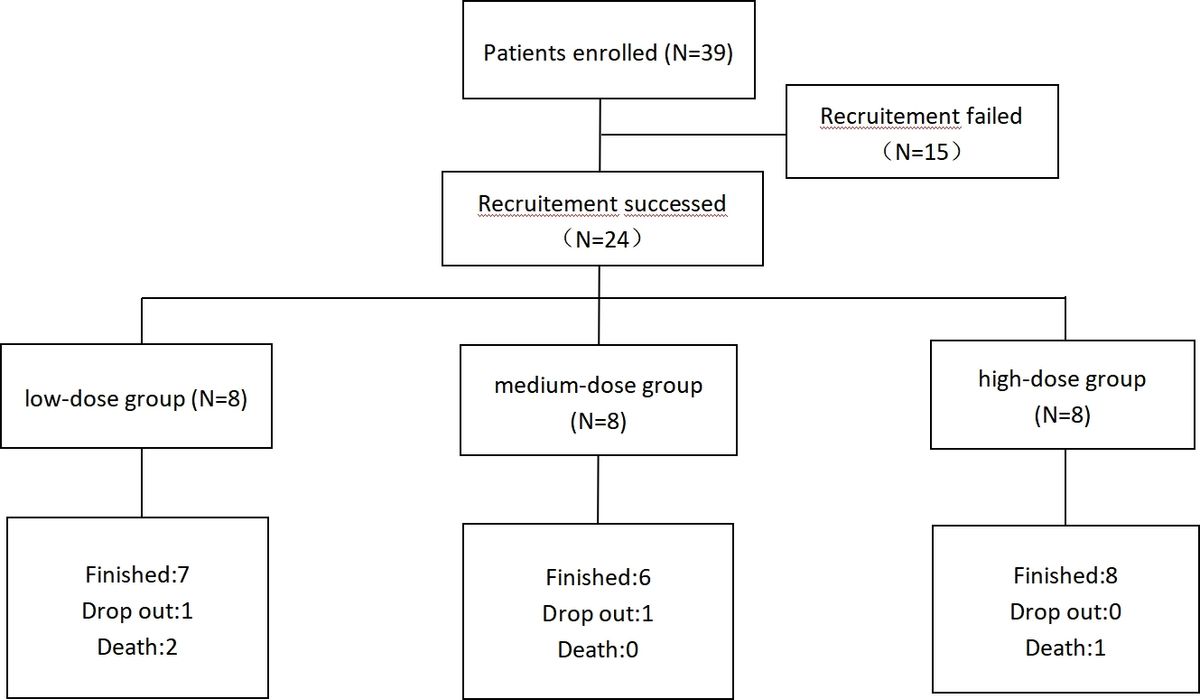
在我们的研究中,我们招募了全部39名患者,其中15名不适合我们的标准。所有24名登记参与者均接受了3次hUC-MSC输注。但低剂量组1例、中剂量组2例尚未完成随访。
对于低剂量组,6个月生存率为75%(八个人中有六个)。一名参与者因在第7次就诊(第85天)时新诊断出肝癌而退出随访。另一位参与者在第七次访问后错过了随访,至今无法联系。2年生存率为50%(8个人中有4人)。除上述撤回一名和退学一名外,还有两名参与者死亡。一名因特拉马引起脑出血死亡(首次输注后23个月),另一名因肝性脑病死亡(首次输注后11个月)。我们的结论是,这2例死亡与hUC-MSC制备无关。
中剂量组的6个月生存率为75%(8个人中有6个)。一名参与者错过了所有后续访问,我们无法联系到他/她。还有另一位参与者由于COVID-19的流行(导致他/她的城市长期实行宵禁)而无法到达医院探望,但我们能够联系到他/她并确认他/她还活着。但此案仍被定义为退学。2年生存率也是75%(8个人中有6个)
高剂量组的6个月存活率为100%(8人中有8人)。2年随访尚未结束,而最后一名患者于2021年12月接受了首次输液,将于2023年12月结束生存随访。然而,根据我们的调查,目前的存活率为87.5%(8 人中有7人)。一名参与者在首次输注后近7个月因肝功能衰竭和肝性脑病死亡。整个研究流程如图1所示。
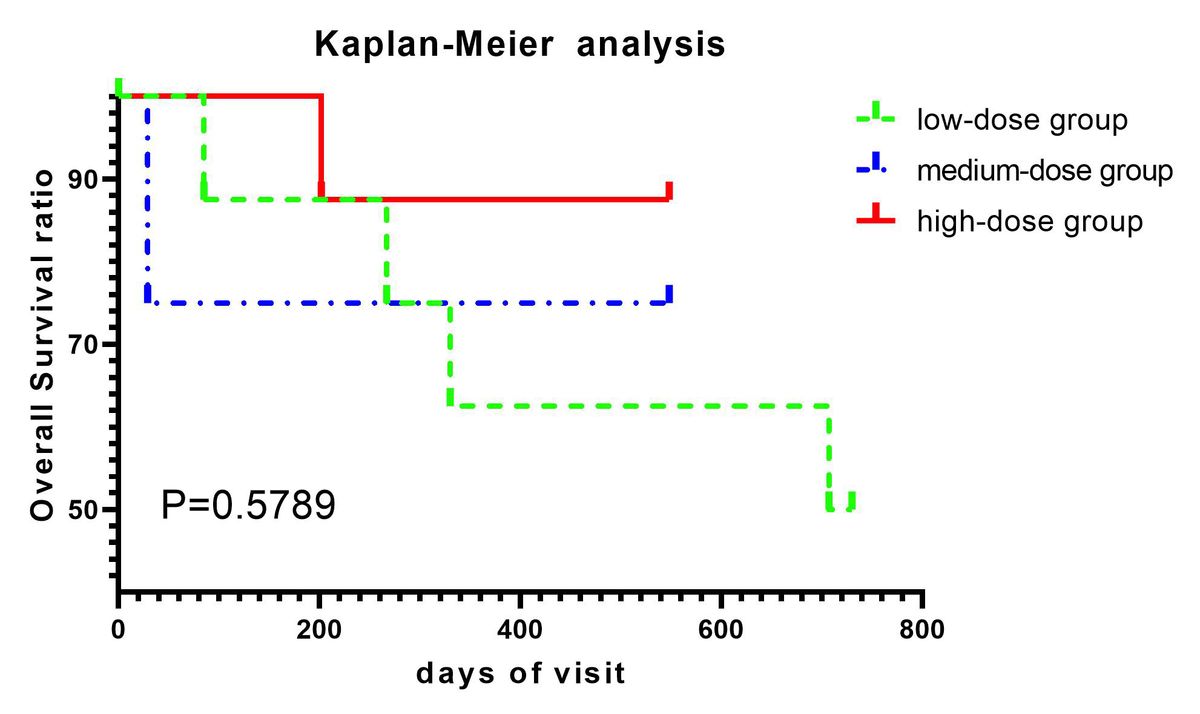
应用Kaplan-Meier生存分析来研究三组的生存情况。如图2所示,低、中、高剂量组的存活率没有显着差异(logrank=0.1741,P=0.9166),推断输注较高浓度的hUC-MSCs可能不会增加生命风险。
肝功能
对于失代偿性肝硬化患者来说,大多数人无法维持与健康人一样良好的肝功能。因此,肝功能的评估是最重要的检查之一。
- 在我们的试验中,我们测试血清白蛋白、丙氨酸转氨酶、天冬氨酸转氨酶、胆碱酯酶、总胆红素、直接胆红素和血清总胆固醇来描述肝功能。我们发现,在第169天,所有这些指标与基线水平没有显着差异。但在后续的走访过程中,一些指标发生了明显的变化,下面将对此进行介绍。这3组之间的变异没有统计学差异。这可能表明剂量对肝功能影响不大。
低剂量组和高剂量组的血清白蛋白水平在第29天和第57天显着升高,并且在第85天所有3组均升高(图3A)。然而,在第169天,三组的Alb水平均下降,并且没有表现出统计学显着性。此外,在整个访视期间,这三组之间的Alb(与基线水平相比)变化没有统计学差异。这些可能表明输注不同剂量的hUC-MSC不会影响血清白蛋白水平。
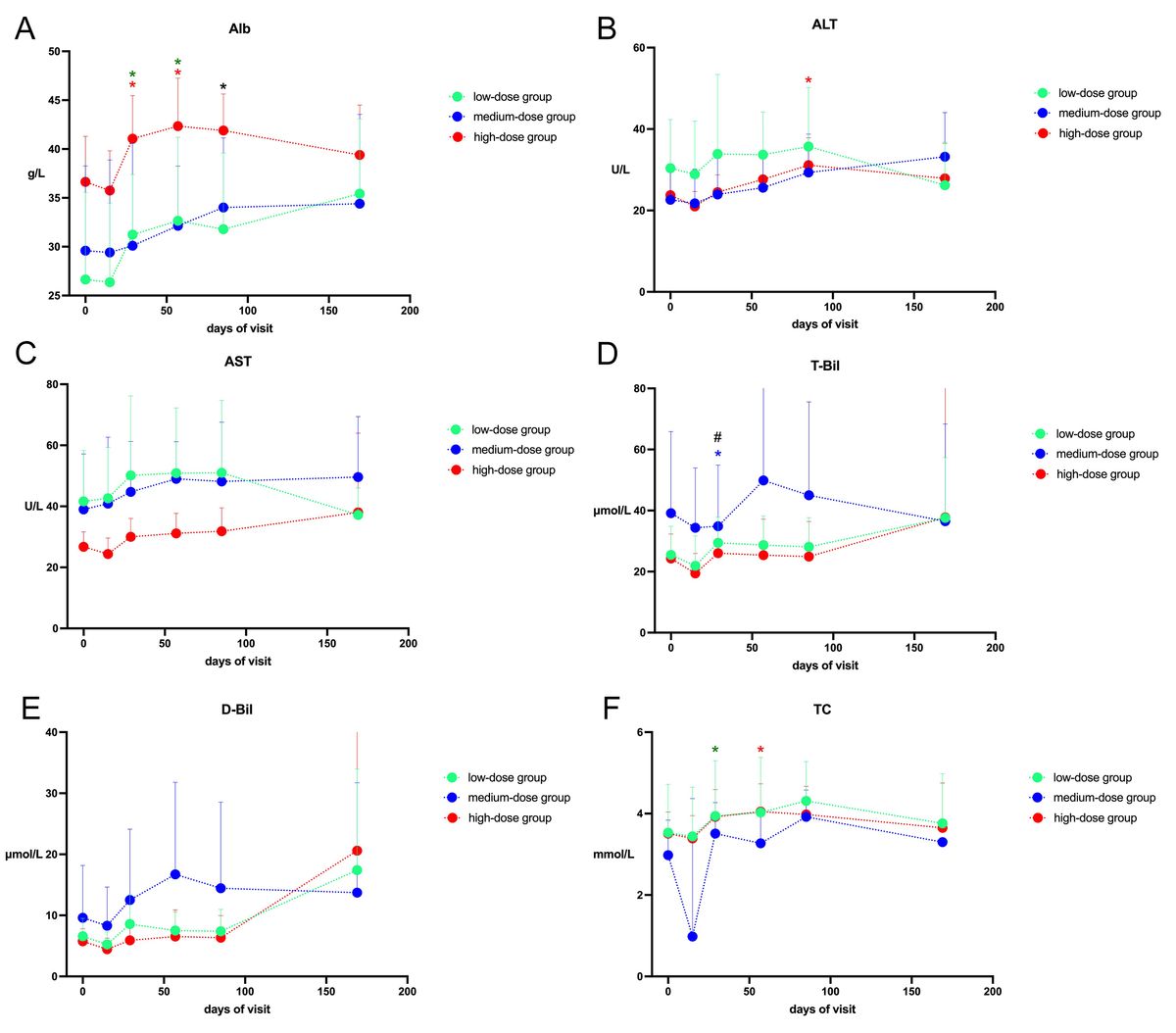
高剂量组仅在第85天ALT水平升高(P=0.0469),且未超过ULN(45U/L)。3组间差异无显着统计学意义。每次访视时ALT水平的变化未表现出显着差异(图3B )。组间AST的变化也没有显示出统计学显着性(图3C)。第29天,高剂量组CHE水平显着升高,第85天低剂量组升高,但两者最高水平仍低于ULN(12500U/L) (S-表1)。随着时间的推移,CHE水平恢复为与基线相比没有差异。同样,各组之间CHE的变化也没有统计学意义。这些指标表明hUC-MSCs可能不会损伤肝细胞。
总胆红素发现,在第29天,中剂量组T-Bil显着增加(P=0.0156),但从第57天开始恢复到正常水平(图3D) 。第29天各组间T-Bil变化有统计学差异(P=0.0108),但hUC-MSCs剂量与T-Bil之间不存在量效关系。如图3E所示,直接胆红素的变化在每次访视中与基线相比均没有表现出显着差异,在这3组之间也没有表现出显着差异。
图3F显示了总胆固醇水平的变化。我们发现,第29天,低剂量组TC水平升高(P=0.0391),并从第57天开始恢复,无差异。此外,高剂量组在第57天表现出显着增强(P=0.0078)。所有3组的TC变化均无显着差异。
凝血功能
大多数失代偿性肝硬化患者没有正常的凝血功能,可能会导致上消化道出血,这是非常危险的。因此,我们测试凝血酶原活性和抗凝血酶III水平来判断参与者的凝血功能。
- 表2显示末次访视时高剂量组的PTTA较基线显着升高(P=0.00156),同时这种变化与低、中剂量组的变化没有明显差异。很明显,高剂量组从第29天开始增强PTTA并持续到最终访视(图4A)。而3组间比较无统计学意义。
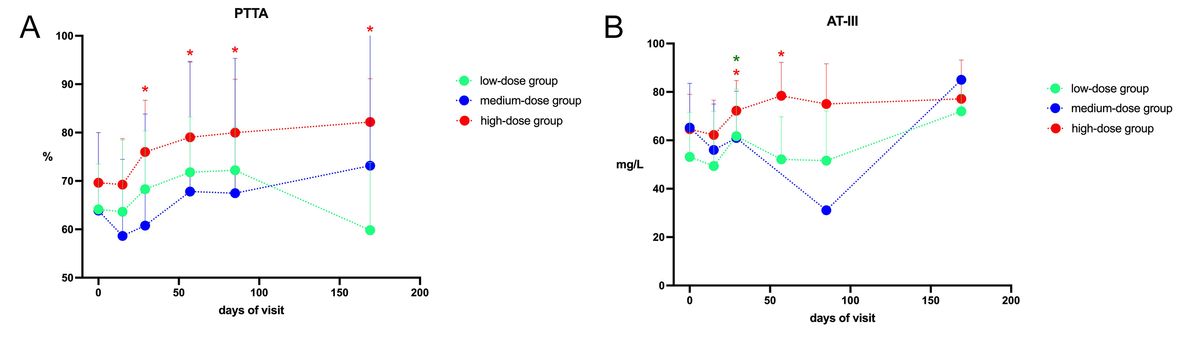
图4B说明了所有访问中AT-III的变化。第29天可以看出,低剂量组和高剂量组AT-III水平显着升高,并且高剂量组AT-III水平在第57天仍然保持较高水平。
临床特征
失代偿性肝硬化患者可能表现出不同的临床特征。为了估计全身状况,创建了许多方法。
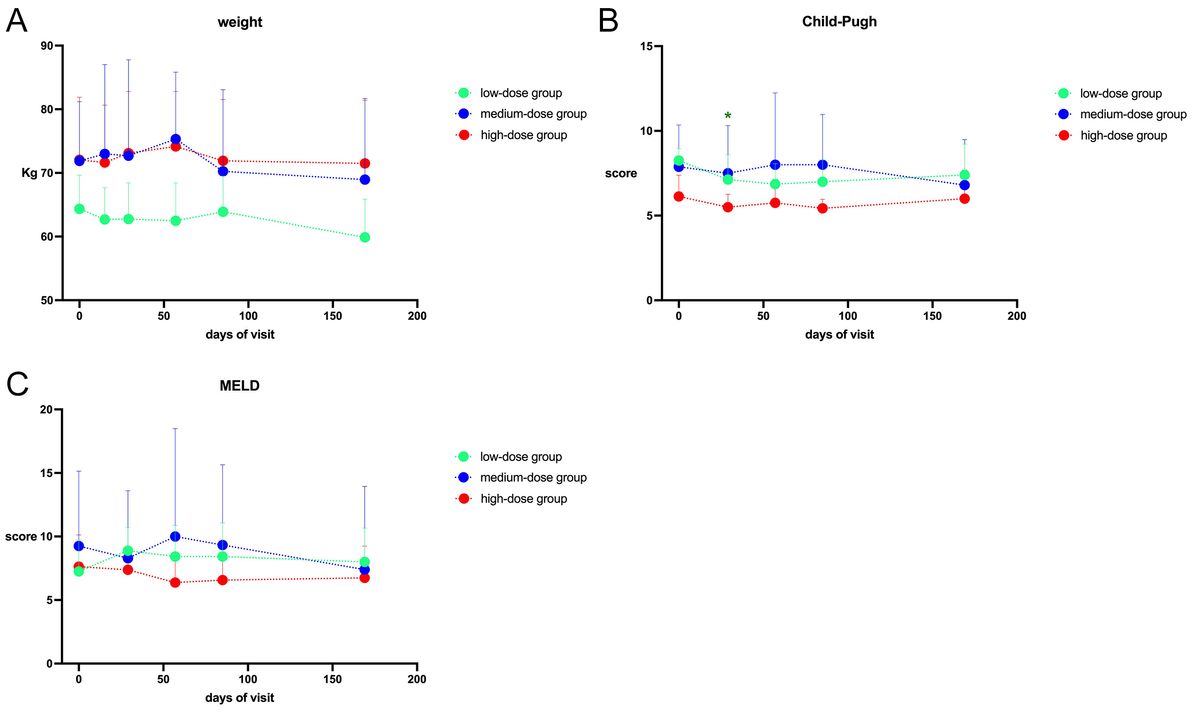
- 在本次试验中,我们应用了最常用的方法:Child-Pugh评分、MELD评分和SF-36量表。根据记录,在最后一次访问中,参与者的体重没有显着变化,并且Child-Pugh和MELD评分与基线相比保持相似。
我们可以看出,参与者的体重保持在稳定的水平,并且3个不同的组显示出类似的变化(图5A)。低剂量组在第57天表现出显着较低的Child-Pugh评分(P=0.0313) (图5B)。组间变异无统计学差异。另外可以发现每次访视MELD评分均无明显变化,3组MELD均无明显变化(图5C)。
我们还记录了所有参与者在基线和所有随访中的症状。这些症状包括腹水、腿部浮肿、吐血、黄疸和食欲不振。
从这些记录中,我们发现在低剂量组中,大多数参与者在基线时有腹水。hUC-MSC治疗后,8名参与者中有5名 (62.5%) 在第29天不再出现腹水。随着时间的推移,人数逐渐减少,最终只有四名参与者中的一名(25%)腹水得到改善。中剂量组中,5人中有3人(60%)腹水消失情况较好。至于高剂量组,8名参与者中有2名(25%)不再出现腹水,而8名参与者中有2名(25%)出现腹水,他们在开始时腹水呈阴性。
大多数低剂量组参与者在基线时出现腿部水肿。在第57天和第85天,7名参与者中的5名(71.4%)改善了水肿症状,但最终只有3名参与者中的1名(33.3%)维持了这种改善。中剂量组5名参与者中有1名(20%)腿部水肿得到治愈。高剂量组的8名参与者中,有1名(12.5%)的水肿情况有所好转,同时8名参与者中的1名(12.5%)水肿情况恶化。
第29天低剂量组仅有1名受试者出现吐血。第一天没有人出现吐血。我们还发现低剂量组中7人中有1人(14.3%)在第29天出现黄疸,但此后有所好转。高剂量组中8人中有1人(12.5%)改善了黄疸。据报道,低剂量组7人中只有1人(14.3%)在第29天出现食欲不佳,但复诊后有所改善。在基线访视中没有人食欲不佳。
免疫功能
失代偿性肝硬化患者由于脾功能亢进和门静脉之间侧支循环的建立而容易受到感染。因此这些患者很容易出现支气管炎、肺炎、腹膜炎或胆道感染。
如图6所示,与上次访视的基线相比,只有IL-8显着下降(P=0.0156),此外3组中IL-8的变化具有统计学意义(P=0.0491)。
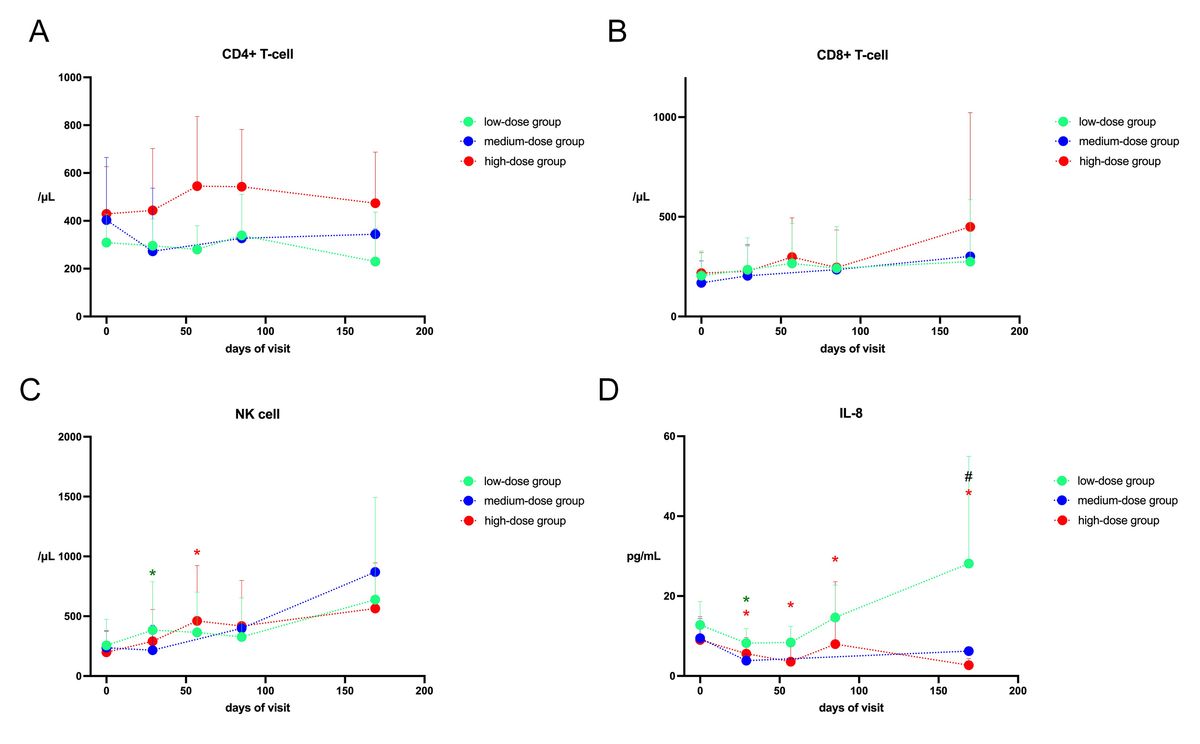
我们对免疫功能进行了详细的测试。我们对所有参与者的10多项指标进行了检测。输注hUC-MCSs后,CD4+T细胞和CD8+T细胞在随访中没有出现明显下降(图 6A、图6B)。
同样,Th1细胞和Th2细胞在4次随访中都没有明显下降。自然杀伤细胞在低剂量组第29天明显升高(P=0.0469),在高剂量组第57天也有所升高,但这些变化在三组间无统计学意义(图6C)。自然杀伤T细胞在整个随访期间没有明显变化。随访期间共检测了7种白细胞介素,不难发现,低剂量组和高剂量组的IL-8在第29天均明显下降,高剂量组的下降持续到第169天(第57天和第169天的P=0.0156)(图6D)。
此外,在第169天,三组之间的差异显著,而高剂量组IL-8的下降更为明显。第57天,低剂量组的IL-17α比高剂量组明显升高,而高剂量组的IL-17α在第57天保持为 0(表9)。
不良事件
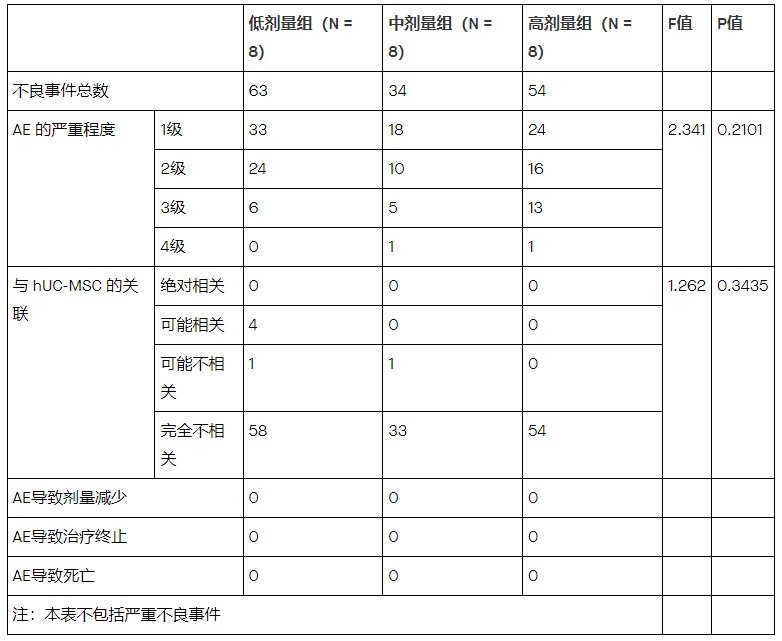
据记录,低剂量组、中剂量组和高剂量组分别发生63次、34次和54次AE(表1)。这些不良事件大多属于1级或2级,低、中、高剂量组所占比例分别为90%、82%和74%。1类和2类AE比例较高,意味着AE影响较轻。4级AE在三组中仅发生0、1和1次。方差分析显示三组之间差异不显着(P=0.2101)。推断该剂量不会增加AE的危险性。
讨论
我们试验中的不良事件大部分属于1级或2级(总比例超过70%),这表明hUC-MSCs的毒性和其他副作用较弱。间充质干细胞治疗膝骨关节炎的I/II期临床试验表明,试验期间未记录SAE、永久性残疾、肿瘤或化脓性关节炎。另一项hUC-MSCs用于治疗复发缓解型多发性硬化症 (RRMS) 的试验声称,尽管检测到部分脱髓鞘病变,但在10年随访期间未观察到肿瘤和器官疾病的发展。
综上所述,间充质干细胞的安全性可靠,为临床应用提供了必要的理论依据。
脐带间充质干细胞的安全性和有效性对于治疗患者至关重要。在试验开始之前,我们查阅了大量的相关文献,找到了脐带间充质干细胞治疗失代偿性肝硬化的理论依据。
- 总结了间充质干细胞治疗肝硬化的几种可能机制,例如直接分化为肝细胞,与肝细胞融合修复,旁分泌大量细胞因子和生长因子促进肝细胞再生,调节免疫系统(CD4+T细胞、CD8+T细胞、NK细胞等)治疗肝脏免疫损伤, MSC条件培养基抑制肝细胞凋亡。此外,Chen还发现间充质干细胞不仅能抑制肝星状细胞的活化,还能通过分泌单核细胞趋化蛋白-1、白细胞介素-6、肝细胞生长因子等减少胶原沉积,从而抑制肝纤维化。
基于这些大量的理论,我们认为脐带间充质干细胞极有可能改善失代偿期肝硬化患者的肝功能。从收集到的数据中,我们得出结论:自输注干细胞以来,也许在2-3个月内,干细胞能改善肝功能,但随着时间的推移,疗效逐渐减弱。因此,我们发现只有PTTA得到了改善,IL-8在最后一次就诊(第169天)时显著下降。
- 作者建议,通过肝动脉或门静脉输注间充质干细胞可能比通过外周静脉输注更能治疗肝硬化患者。一项荟萃分析显示,动脉内注射比外周静脉注射更有效,能改善MELD评分以及ALB和T-BiL水平。有报道称,通过动脉输注可使间充质干细胞更精确地定位在损伤组织中。此外,经外周静脉输注时,间充质干细胞最先到达肺部,其次到达肝脏。因此,我们有了一个新的想法,即通过肝动脉或门静脉输注hUC-间充质干细胞,以使尽可能多的细胞作用于肝损伤组织。然而,新的输注途径难度大、消耗高、风险高,仍是亟待解决的重要问题。
结论
人脐带间充质干细胞在治疗与乙型肝炎病毒(HBV)相关的失代偿性肝硬化患者方面具有巨大潜力,但需要更大的样本量,需要通过RCT试验来确定。在我们的试验中,我们证明人脐带间充质干细胞可以在短时间内改善肝功能,特别是对凝血功能的影响。它对于临床应用来说也足够安全,严重不良事件和肿瘤发展的风险较低。人脐带间充质干细胞对免疫系统几乎没有影响。它在某些方面改善了患者的全身状况。
参考资料:Xian Qin, Jing Chen, Li Du et al. The research of human umbilical cord mesenchymal stem cells therapy in decompensated liver cirrhosis associated with hepatitis virus B: a long-term follow up analysis of a single-center, on-limits and stepped research., 24 January 2024, PREPRINT (Version 1) available at Research Square
[https://doi.org/10.21203/rs.3.rs-3736389/v1]
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请及时跟本公众号联系,我们将在第一时间处理。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号