随着干细胞技术的不断提高,国内干细胞新药逐年增长。从一定程度上,也说明国家对于干细胞技术的推广是非常支持的。
目前,根据美国临床试验数据库统计,全球已有4000多项注册的干细胞临床研究项目,涵盖代谢性疾病(如糖尿病)、呼吸系统疾病(如肺纤维化、慢性阻塞2性肺病)、神经系统疾病(如脑中风、阿尔茨海默病、帕金森综合征、脊髓损伤)、骨关节炎(如类风湿性关节炎、骨关节病)、自身免疫性疾病(如系统性红斑狼疮)、肝脏疾病(如肝衰竭、肝硬化)、美容抗衰老(如女性卵巢早衰、男性勃起功能障碍)等领域。
其中,我国已有60余项间充质干细胞药物临床试验,包括糖尿病足溃疡、骨关节炎、类风湿关节炎、肺纤维化、卒中、银屑病、急性呼吸窘迫综合征、肝衰竭、克罗恩病、移植物抗宿主病等病种。随着更多临床试验数量增加,预计到2028年,中国干细胞市场经济的复合年均增长率将达到16.5%。
间充质干细胞,全称mesenchymal stem cells,简称MSCs,是属于中胚层的一类多能干细胞,主要存在于结缔组织和器官间质中,包括:骨髓、脐带、脂肪、粘膜、骨骼、肌肉、肺、肝、胰腺等组织以及羊水、羊膜、胎盘等,在适宜的条件下可分化为脂肪、骨、软骨等多种组织细胞。
间充质干细胞还具有调节免疫系统的归巢和营养特性,影响受损组织周围的微环境并增强组织修复,从而为基于细胞的治疗提供了广阔的前景。因此,间充质干细胞成为临床试验中广泛使用的成体干细胞也就不足为奇了。
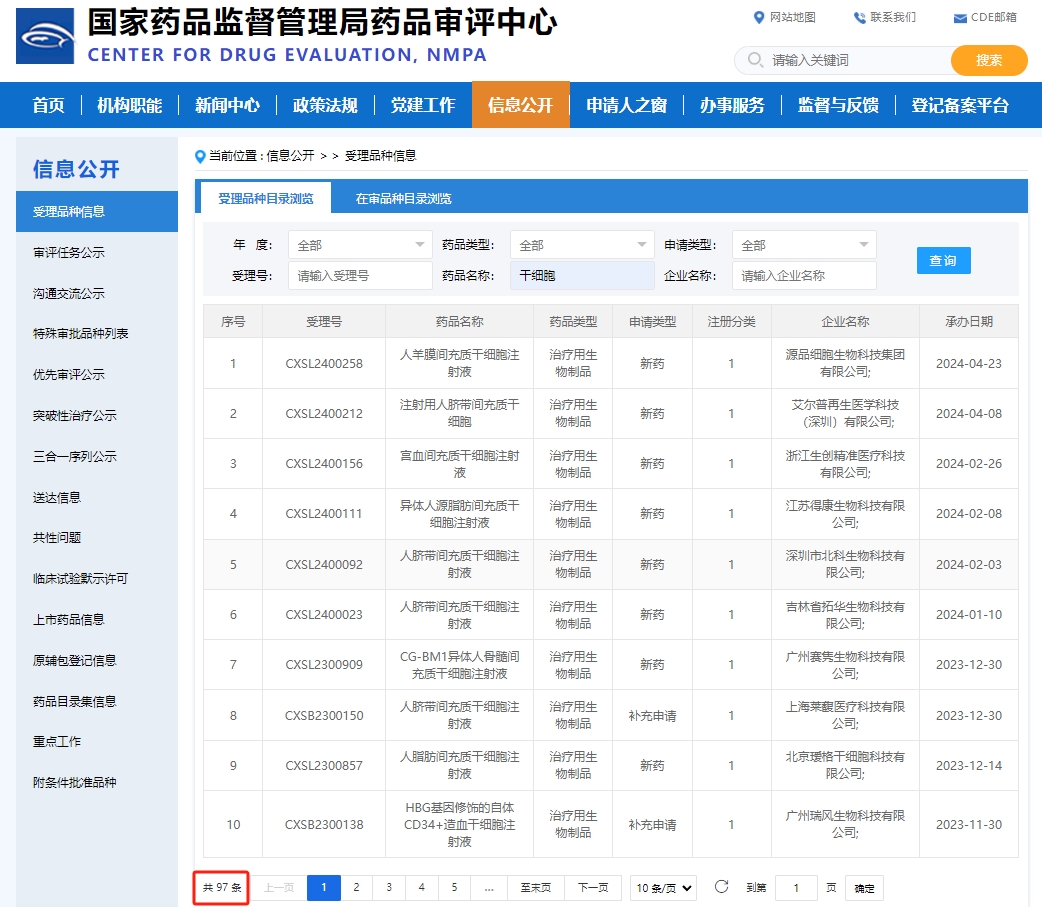
下面是我国2018年-2024年期间,国家药品监督管理局药品审评中心官网,“干细胞”关键词信息公开已受理共计97款干细胞新药。其中,人脐带间充质干细胞占据大半以上的数量。
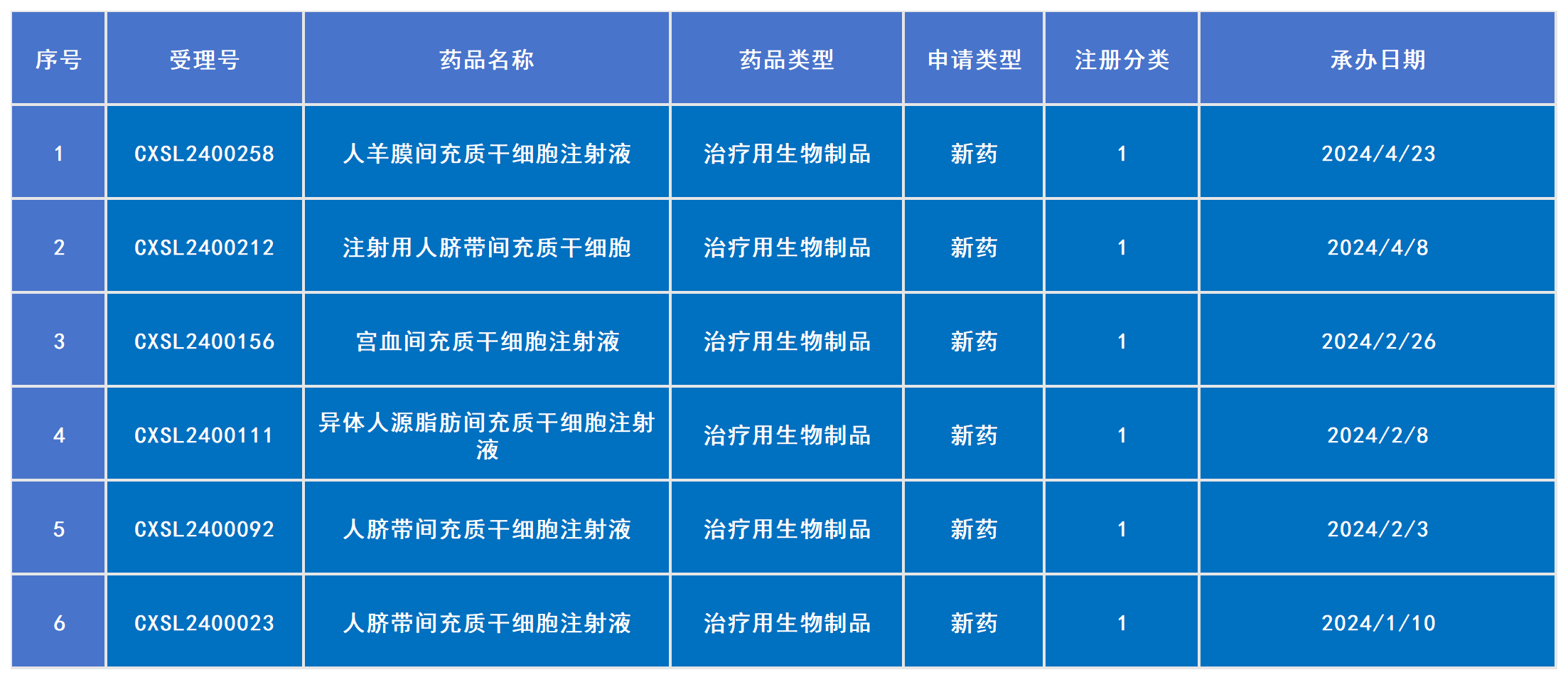
2024年已受理6款干细胞新药(截止发稿时间止)
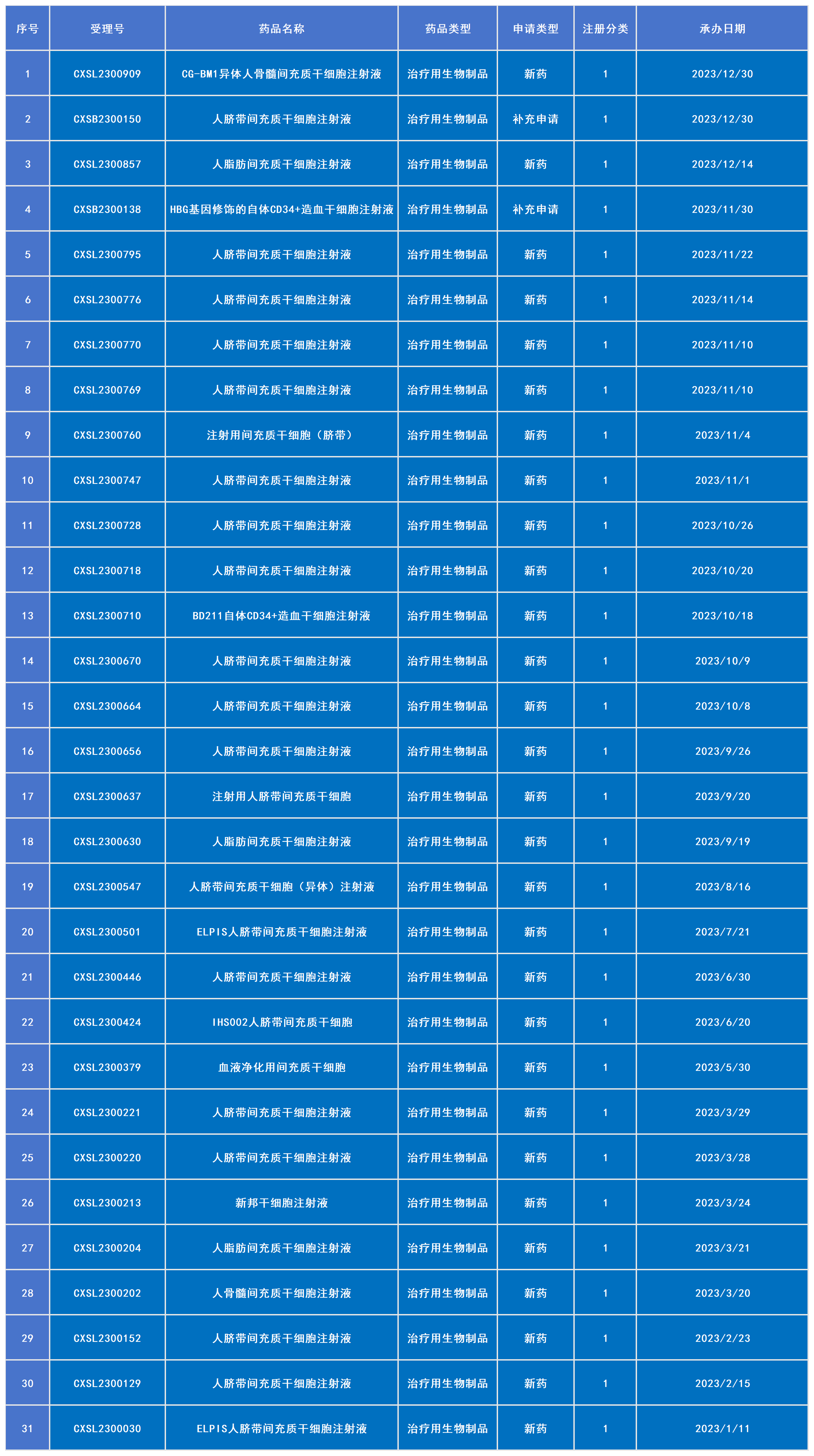
2023年已受理31款干细胞新药(包括2款补充申请)
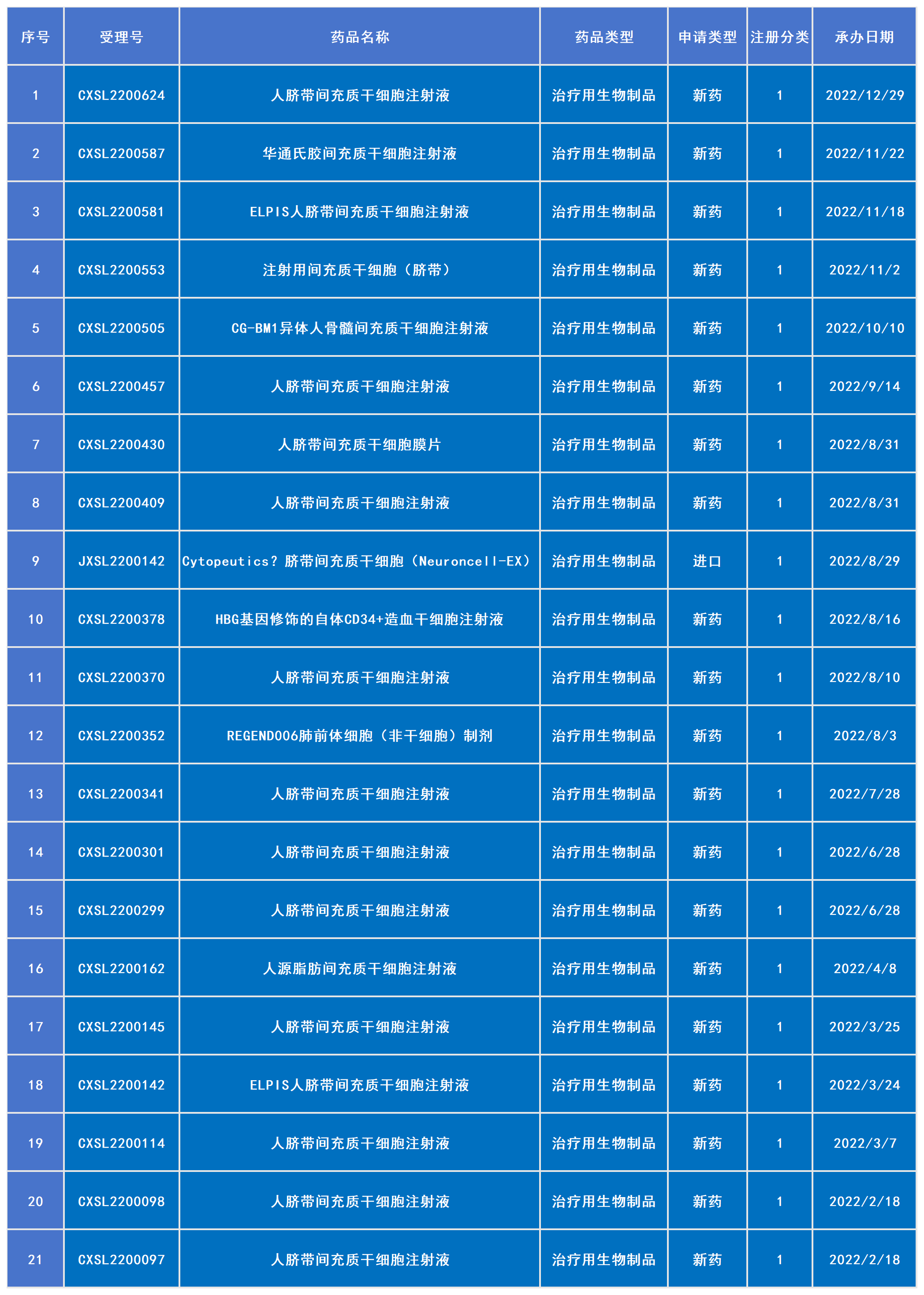
2022年已受理20款干细胞新药(包括1款进口药)
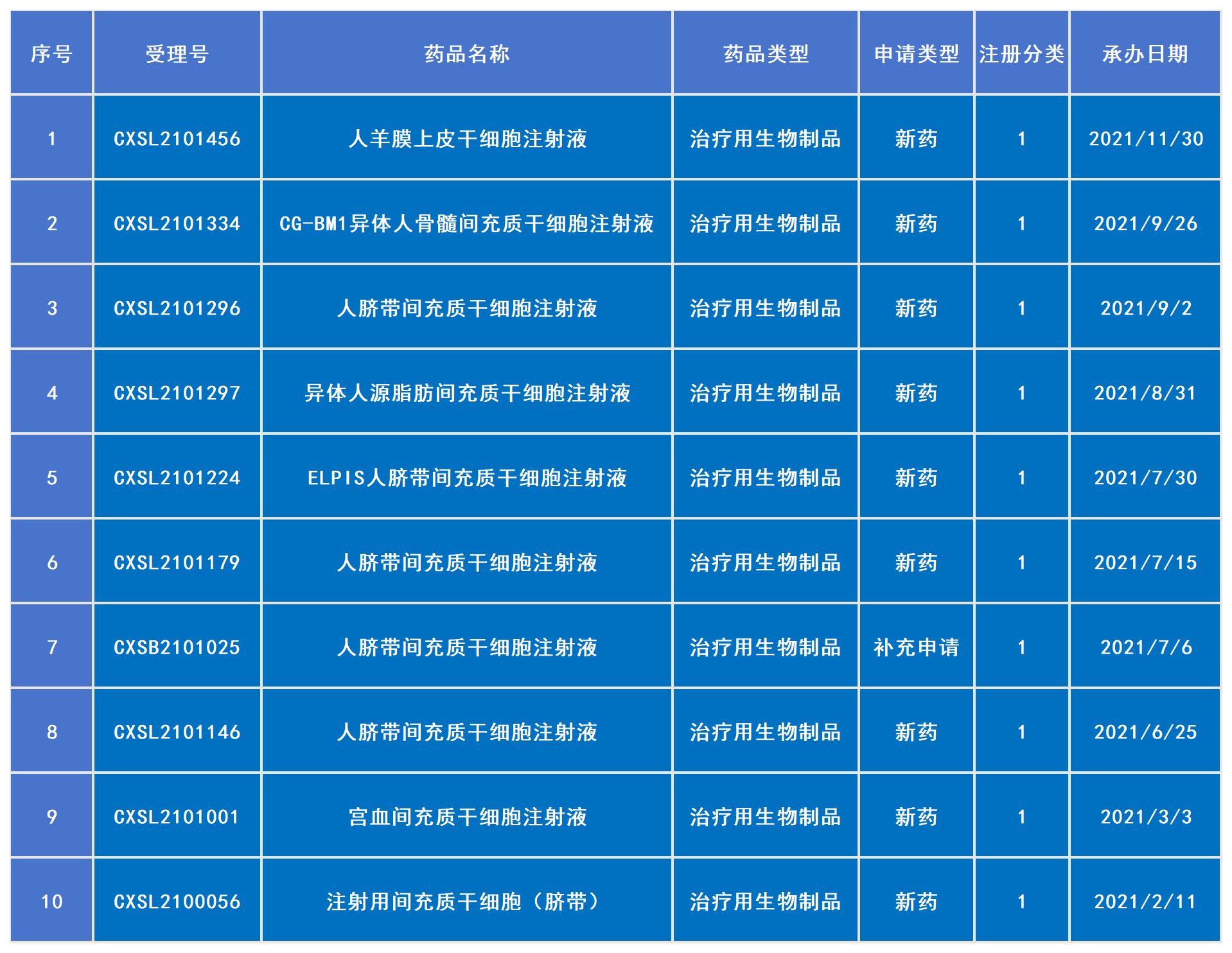
2021年已受理10款干细胞新药(包括1款补充申请)
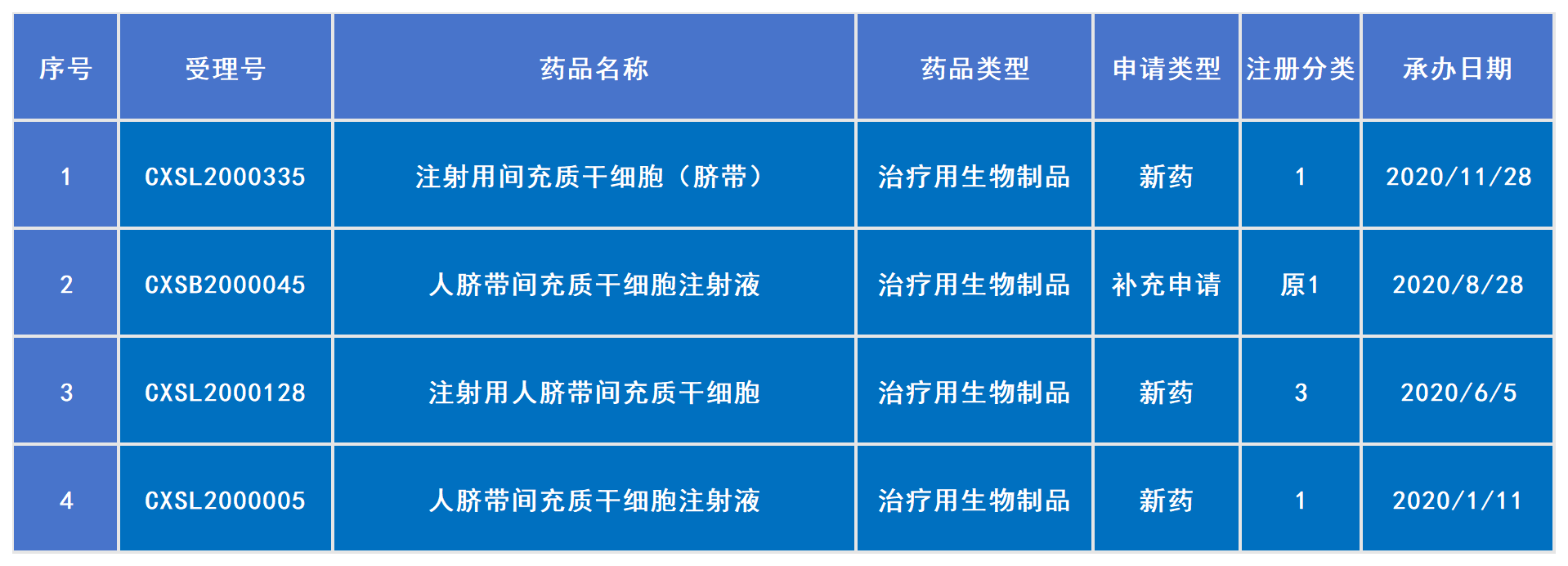
2020年已受理4款干细胞新药(包括1款补充申请)
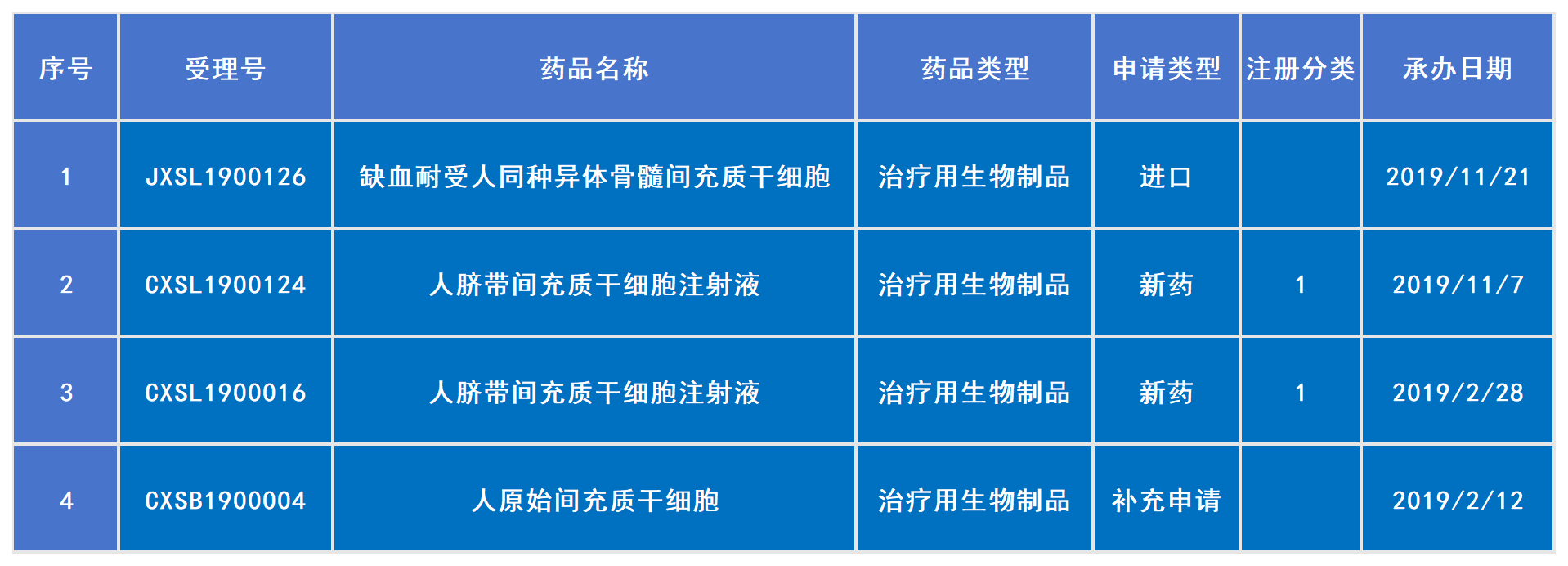
2019年已受理4款干细胞新药(包括1款补充申请,1款进口药)
2018年已受理4款干细胞新药(包括1款进口药)
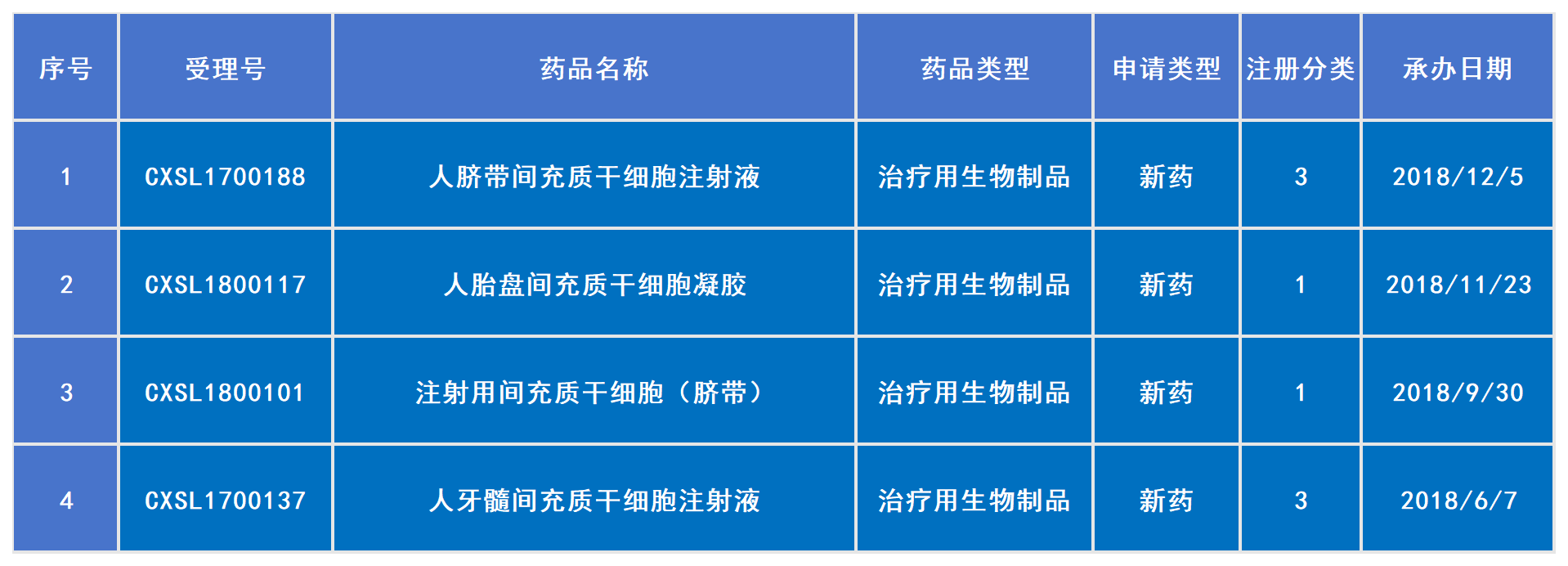
展望未来:目前全球范围内获批的干细胞产品主要集中在日本、韩国、美国、欧盟等地。近几年,我国也在大力扶持干细胞技术的发展,目前已将干细胞发展列入“十四五”发展规划。
相信在不久的将来,干细胞将会像“智能手机”一样,深入影响我们每个人的生活。我们也期待随着干细胞药物研究规模的不断扩大,再生医疗技术能让更多的患者获益!
药品信息来源:国家药品监督管理局药品审评中心官网
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号