导读:近年来干细胞治疗在肝硬化领域展现出巨大潜力,通过其独特的再生能力,可靶向肝脏损伤区域,促进肝细胞再生及肝功能恢复。临床研究证实,干细胞能显著改善肝纤维化指标,提升患者生活质量。干细胞治疗已成为肝硬化创新疗法的研究热点,未来有望开辟肝病治疗新纪元。
肝硬化(Liver Cirrhosis)是一种慢性肝脏疾病,其特征是肝脏结构的长期损伤和纤维化,导致肝脏组织逐渐被纤维组织所替代,形成硬化的结节。这种结构的改变严重影响了肝脏的正常功能,包括代谢、解毒、分泌胆汁和合成蛋白质等。
肝硬化可能由多种因素引起,包括长期酗酒、病毒性肝炎、自身免疫性肝病、遗传性疾病等。患者可能会出现腹水、黄疸、肝性脑病、门脉高压等症状,严重时可导致肝功能衰竭和死亡。
- 相关阅读请浏览(肝硬化的体征和症状是什么?及其治疗方法)
肝硬化治疗方法
肝硬化是中国面临的重要公共卫生问题,具有较高的发病率和死亡率。中国是全球肝硬化发病率和死亡率最高的国家之一,给患者及其家庭以及社会医疗系统带来了沉重的负担。
除肝移植外,目前仍缺乏有效的终末期肝硬化治疗方法,因此在肝硬化早期阶段进行有效抗纤维化治疗显得尤为重要。
5项研究388例患者证实:干细胞治疗肝硬化安全有效,能够显著改善肝功能和生存率!
近年来,随着再生医学的发展,干细胞治疗肝硬化作为一种新兴的治疗方法,利用干细胞的自我更新和分化潜能,为脊肝硬化患者提供新的修复策略。
本文通过分析总结5项干细胞治疗肝硬化的临床试验结果,从而评估干细胞移植作为肝硬化患者的潜在治疗方法的安全性和有效性。
①临床试验一:干细胞改善失代偿性肝硬化患者的肝功能和腹水
2012年2月9日,北京302医院转化肝病研究所生物治疗研究中心在期刊杂志《Journal of Gastroenterology and Hepatology》上发表了一篇关于《人脐带间充质干细胞改善失代偿性肝硬化患者的肝功能和腹水》的研究成果。【1】

共招募了45名患有失代偿性肝硬化的慢性乙型肝炎患者,其中30名接受人脐带间充质干细胞输注的患者和15名接受生理盐水作为对照的患者。
有效性
- 与对照组相比,接受UC-MSC输注治疗的患者的腹水量显著减少(P<0.05)。
- UC-MSC治疗还显著改善了肝功能,表现为血清白蛋白水平升高、总血清胆红素水平降低以及终末期肝病钠模型评分降低。
安全性:在1年的随访期内检测临床参数。两组均未观察到显著的副作用和并发症。
研究表明,脐带间充质干细胞输血在临床上是安全的,可以改善肝功能并减少失代偿性肝癌患者的腹水。因此,脐带间充质干细胞输血可能为失代偿性肝癌患者提供一种新的治疗方法。
②临床试验二:干细胞可改善失代偿性肝硬化乙肝患者的肝功能
2018年,南京军区上海市肝病研究中心在《中国组织工程研究杂志》上发表了一篇关于《输注人脐带间充质干细胞可改善失代偿性肝硬化乙肝患者的肝功能》的研究成果。【2】

人脐带间充质干细胞(hUC-MSC)治疗组招募了17名乙肝患者,对照组包含17名临床匹配的个体。
有效性评估
1.肝功能测试
- 间充质干细胞移植患者肝功能有所改善,白蛋白、胆红素、乳酸脱氢酶及碱性磷酸酶水平有所恢复。
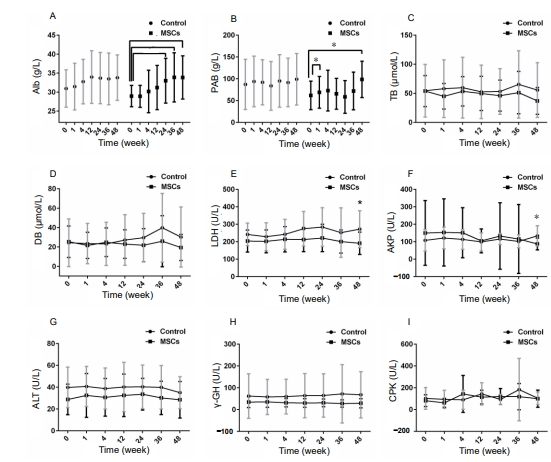
- 治疗后48周,MSC治疗组的Alb水平从(28.9±2.8)g/L升高至(33.9±5.7)g/L,显著高于基线值(P<0.05;图A)。
- MSC治疗患者的PAB从(62.1±32.7)g/L升高至(98.7±41.6)g/L,也显著高于基线值(P<0.05;图B)。
- 治疗后48周,MSC治疗组的LDH和AKP水平明显低于对照组(P<0.05;图E、F)。治疗后48周,LDH值为:MSC治疗组为(191.4±63.7)U/L;对照组为(272.2±105.3)U/L。治疗后48周,AKP值为:MSC治疗组为(87.2±33.7)U/L;对照组为(133.8±58.3)U/L。
2.凝血测试
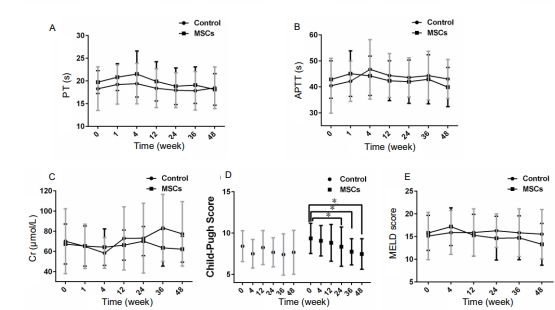
- 治疗后各个时间点,MSC治疗组和对照组患者的PT无明显差异(图A)。
- 在治疗4周后观察到MSC治疗组的APTT更快,并且MSC治疗患者的APTT持续下降直至治疗后48周(图 B)。治疗后48周的APPT值为:MSC治疗组,39.9秒(减少7.5秒);对照组,43.1秒(增加7.5秒)。
- MSC治疗患者血液中的Cr水平与对照组患者相比有所下降(图C),这表明肾功能有所改善。
- MSC治疗组的Child-Pugh评分从基线时的9.4分显著下降至治疗48周后的7.5分(P<0.05;图D),表明预后较好。
- MSC治疗患者的MELD评分也从15.8分下降至13.3分,而对照组的MELD评分从基线时的15.1分略有上升至治疗48周后的15.5分(图E)。
这表明与仅接受常规治疗的患者相比,接受hUC-MSC治疗的患者预后较好。
安全性评估:输注hUC-MSC后,患者的生命体征、心电图结果和肾功能未发现异常变化。
综上所述,间充质干细胞移植治疗乙型肝炎失代偿肝硬化患者肝功能有所改善,白蛋白、胆红素、乳酸脱氢酶及碱性磷酸酶水平有所恢复,且患者Child-Pugh及MELD评分明显恢复。表明人脐带间充质干细胞静脉注射入乙肝肝硬化失代偿患者体内可改善肝功能。
③临床试验三:间充质干细胞治疗失代偿性肝硬化临床试验分析
2021年11月29日,解放军总医院第五医学中心感染病医科王福生院士团队在国际期刊《Hepatology International》上发表了一篇关于《间充质干细胞治疗失代偿性肝硬化:随机对照临床试验的长期随访分析》的研究成果。【3】

本项前瞻性、开放性、随机对照研究纳入了219名HBV相关失代偿性肝硬化(DLC)患者,分为对照组 (n= 111) 和脐带间充质干细胞 (UC-MSC) 治疗组 (n=108),所有患者均在2010年10月至2017年10月期间接受了随访检查。
有效性评估
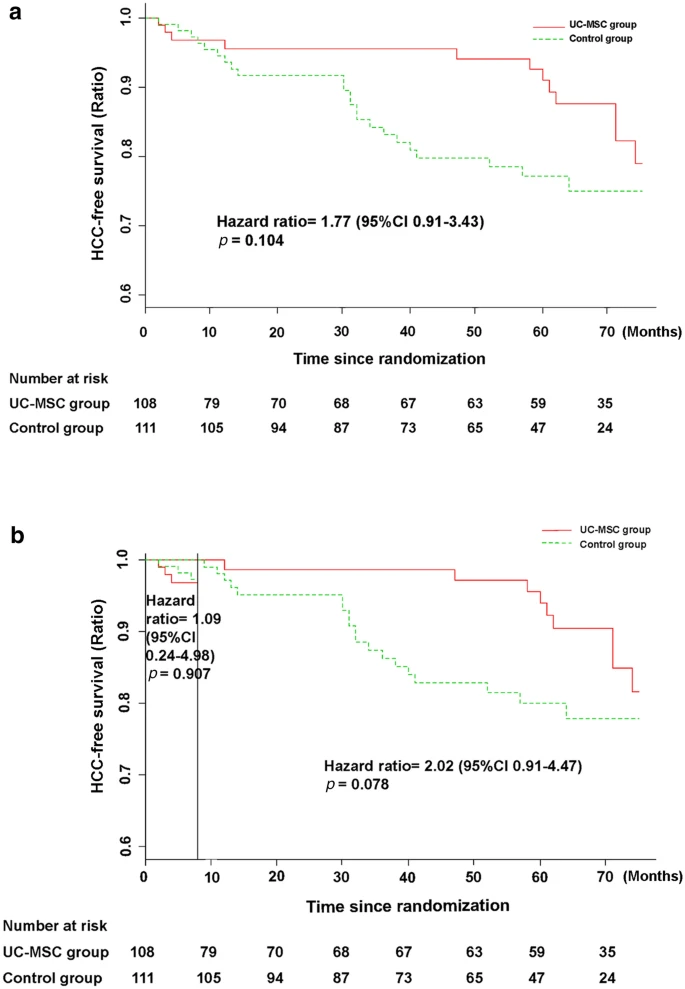
1.脐带间充质干细胞对长期生存的影响
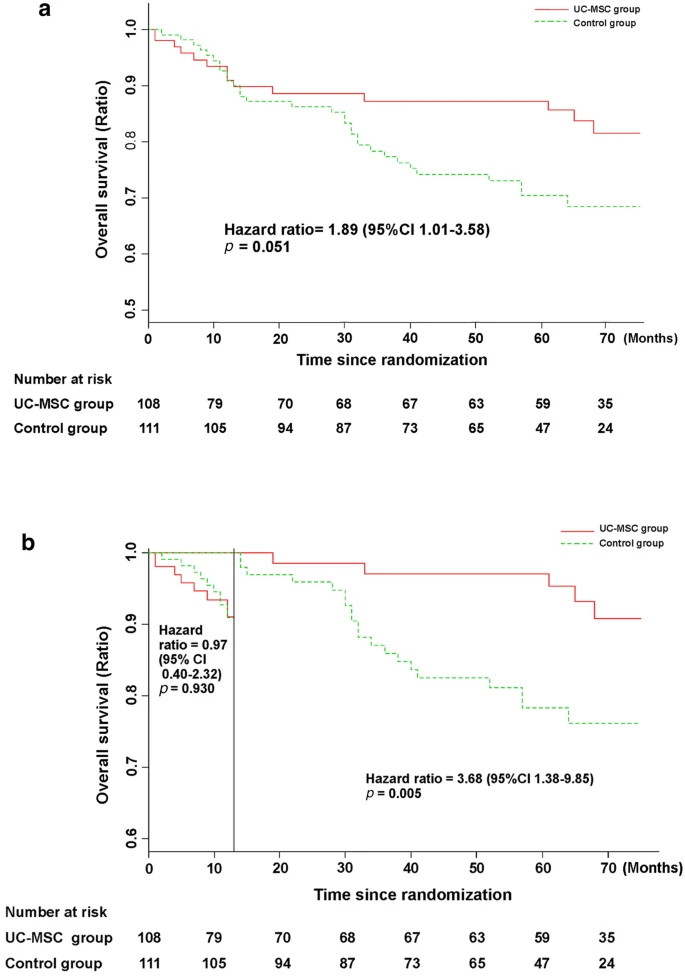
- 在75个月的随访中,UC-MSC治疗组与对照组之间的总生存率无显著差异。(图a)
- 而使用Landmark分析,在13至75个月的随访中,UC-MSC治疗组的总生存率显着高于对照组。(图b)
- 结果表明,尽管UC-MSC治疗可以显著提高失代偿性肝硬化患者的生存率,但UC-MSC治疗相对于传统医学治疗的优越性可能在UC-MSC输注后约13个月才会显现出来。
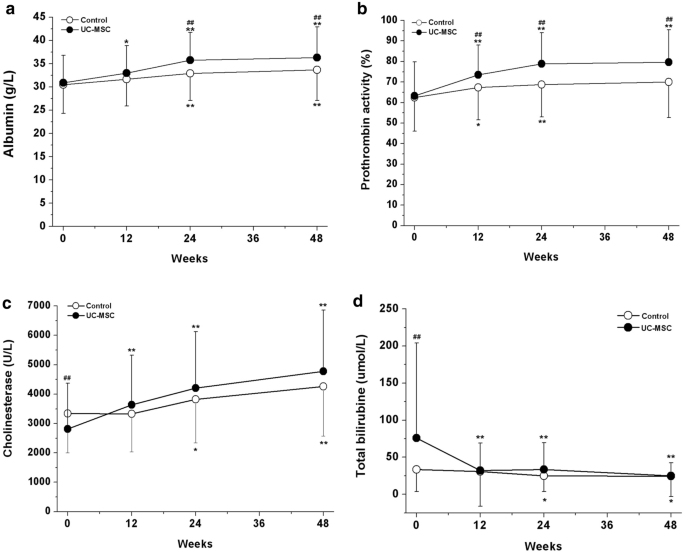
2.脐带间充质干细胞输注对肝功能的影响
- 48周的随访中,两组的ALB水平均较基线水平升高,但UC-MSC治疗组的ALB水平在24和48周的时间点明显高于基线水平(图a)。
- 在48周的随访中,UC-MSC治疗组的PTA水平与基线水平和对照组相比明显升高(图b)。
- UC-MSC输注后,随访48周,CHE水平较基线水平明显升高,TBIL水平较基线水平明显降低,但与对照组相比无明显差异。(图c、d)
- 提示UC-MSC治疗可减轻肝脏炎症,明显改善肝功能。
安全性评估
- UC-MSC组所有患者均能良好耐受UC-MSC治疗。7名患者在UC-MSC输注后2-6小时内出现自限性发热(体温37-38°C),但在12小时内恢复,无需任何额外治疗。未发现其他短期临床不良反应,包括过敏、皮疹或感染。Kaplan–Meier 分析显示,UC-MSC 治疗组与对照组的无肝癌生存率无显著差异(HR=1.77,95%CI 0.91–3.43,p=0.104)(图a)
- 随访的前8个月内,对照组的无肝癌生存率似乎高于UC-MSC治疗组,但在8至75个月之间,UC-MSC组的无肝癌生存率更高。(图b)
- 结果显示,对于失代偿性肝硬化患者,UC-MSC治疗在长期安全性方面和常规治疗相比并不会带来更高的风险。
综上所述,随访13至75个月,治疗组总生存率明显高于对照组。UC-MSC治疗明显改善肝功能,随访48周,血清白蛋白、凝血酶原活动度、胆碱酯酶、总胆红素水平明显改善。UC-MSC组未见明显副作用或治疗相关并发症。
结论:UC-MSC疗法不仅耐受性良好,还能显著提高HBV相关DLC患者的长期生存率和肝功能。因此,UC-MSC药物治疗可能为该疾病提供一种新的治疗方法。
④临床试验四:干细胞回输对失代偿期肝硬化患者远期疗效的影响研究
2022年,空军军医大学西京消化病医院在期刊《中华肝病杂志》上发表了一篇关于《自体外周血干细胞回输对失代偿期肝硬化患者远期疗效的影响研究》的研究成果。【4】

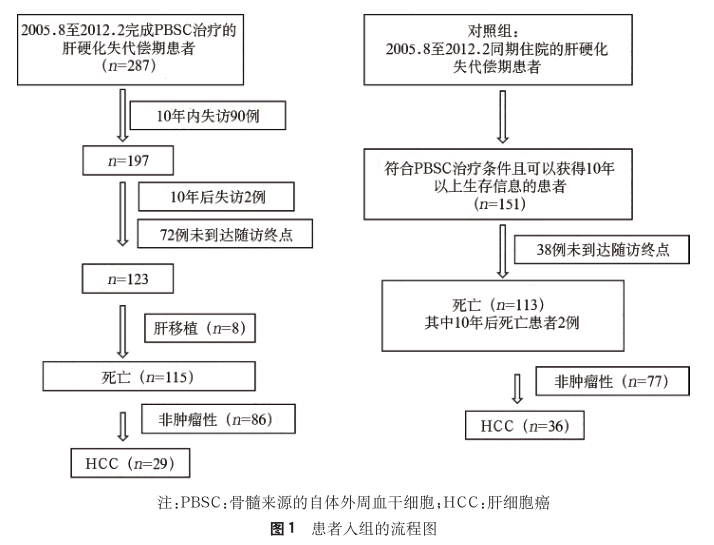
纳入2005年8月至2012年2月空军军医大学第一附属医院消化内科完成PBSC治疗的失代偿期肝硬化患者资料。共287例失代偿期肝硬化患者完成骨髓来源的自体外周血干细胞(PBSC)治疗,90例患者在术后10年内失访。10年后再次失访患者2例。以患者死亡或肝移植作为随访终点,共有123例到达终点,其中肝移植患者8例,72例已随访10年以上尚未到达随访终点。
有效性评估
1.生存率评估
- 在到达随访终点或虽未到达随访终点但至少随访10年以上的197例患者中,有74例的骨髓来源的自体外周血干细胞术后生存期超过10年,肝硬化失代偿期患者PBSC术后10年的生存率为37.56%。
- 对照组共纳入了151例,未达到随访终点患者38例,死亡118例,其中随访10年后死亡患者2例,对照组的10年生存率为26.49%(40/151),两组间差异有统计学意义(P<0.05)。两组的生存曲线见图2。
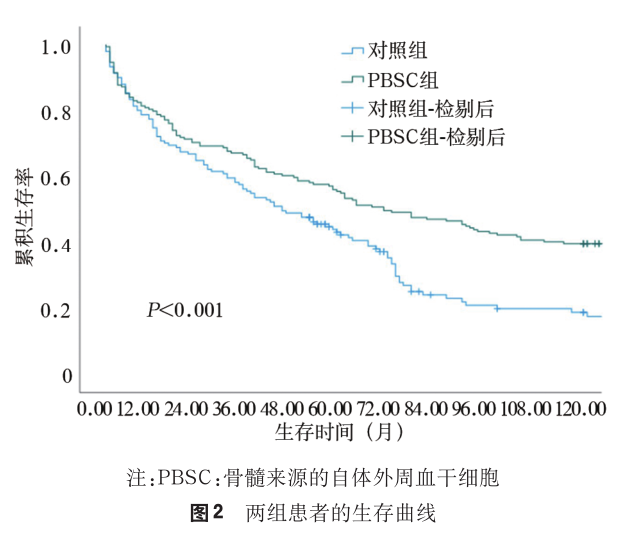
2.肝功能测试评估
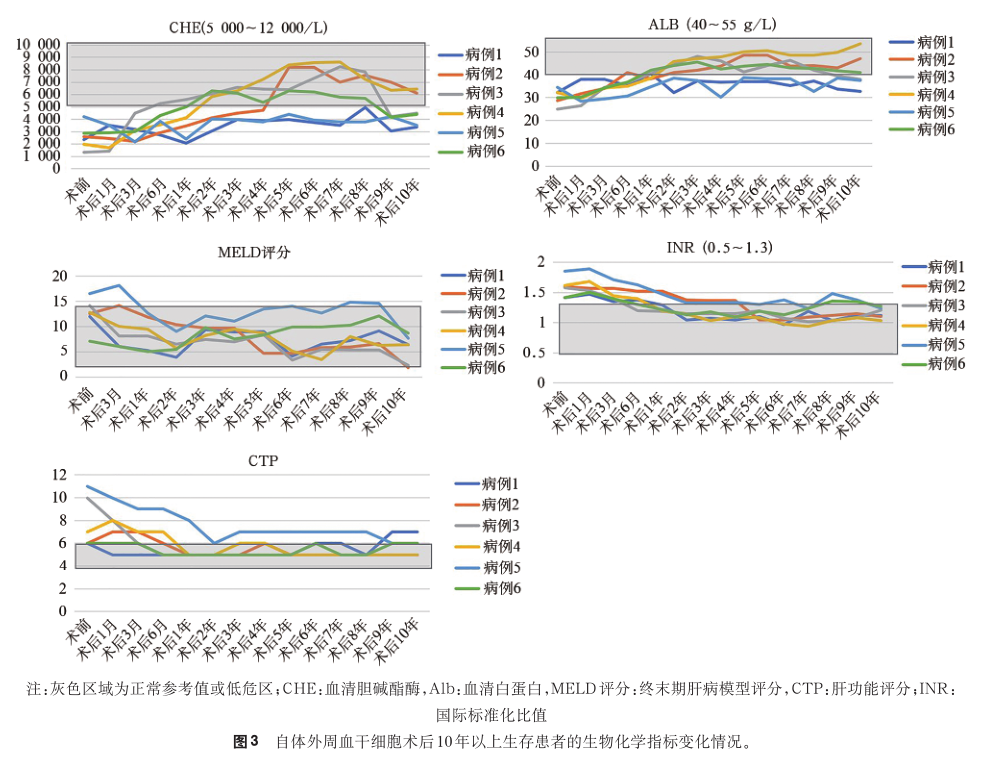
- 选取可以反映患者肝脏合成储备功能及可以预测患者预后的胆碱酯酶、白蛋白、国际标准化比值、CTP评分以及MELD评分等,对生存期>10年PBSC组患者的生物化学指标进行分析。
- 所有患者表现出基本相同的趋势,即PBSC治疗后的3个月 ~ 1年内以上指标逐渐恢复,并在后续长达10年的随访中长期稳定在较理想的水平(图3)。
安全性评估
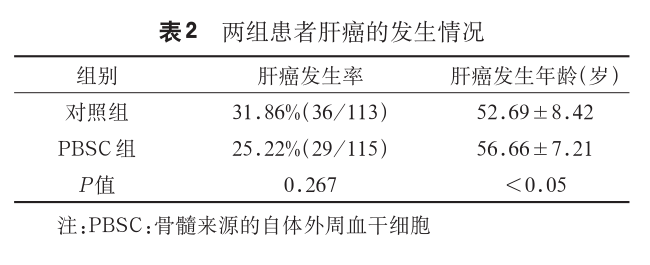
- PBSC组29例的中位肝癌发生年龄为60岁(39岁~68岁),平均肝癌发生年龄为(56.66±7.21)岁。
- 对照组的中位肝癌发生年龄为51.5岁(36岁~68岁),平均肝癌发生年龄为(52.69±8.42)岁。
- PBSC组的肝癌发生年龄晚于对照组。
综上所述,PBSC组的10年生存率高于对照组。胆碱酯酶、白蛋白、国际标准化比值、肝功能评分以及终末期肝病模型评分等多项指标在PBSC治疗后的3个月~1年内逐渐恢复,并在后续长达10年的随访中长期稳定在较理想的水平。
结论:通过10年以上的长期随访观察研究,进一步明确了PBSC治疗能使失代偿期肝硬化患者长期获益,并且远期安全性良好,为干细胞在临床应用的安全性和有效性提供更多的数据支撑。
⑤临床试验五:人脐带血间充质干细胞移植治疗失代偿性肝硬化患者
2023年5月,柳州市中医院和广州中医药大学第二附属医院联合在期刊《Journal of Gastrointestinal Surgery》上发表了一篇关于《人脐带血间充质干细胞移植治疗失代偿性肝硬化患者》的研究成果。【5】

纳入2010年11月至2013年2月柳州市中医院失代偿期肝硬化住院患者,共入组201例患者,其中接受人脐带血间充质干细胞移植(HUCB-MSCT)治疗(SCT组)36例,未接受HUCB-MSCT治疗(非SCT组)165例。
有效性评估
主要结果是总生存率。次要结果是3年和5年生存率以及发病率(HCC)发生率。总生存率定义为从研究开始到病例死亡的时间。
1.生存率评估
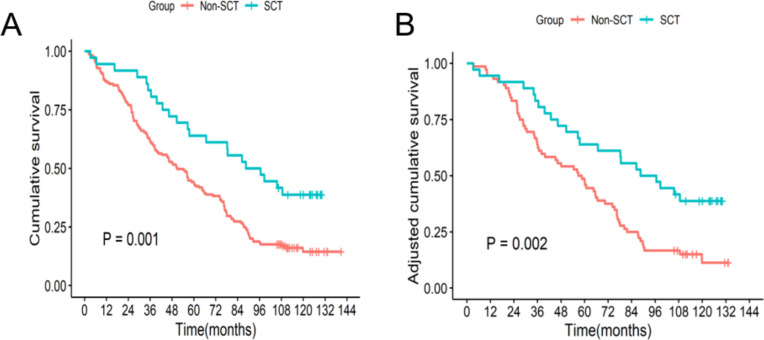
- PSM前研究对象总死亡率为80.1%(161/201),其中SCT组死亡率为61.1%(22/36),非SCT组死亡率为84.2%(139/165)(P=0.002)。
- PSM后研究对象总死亡率为74.1%(80/108),其中SCT组死亡率为61.1%(22/36),非SCT组死亡率为80.6%(58/72)(P=0.030)。
- PSM前后SCT组Kaplan-Meier生存曲线均高于非SCT组(均P<0.05)。多元回归分析发现,HUCB-MSCT治疗是患者OS的独立有益因素。
2.发病率评估
- 全部队列中,发病率(HCC)总发生率为33.3%(67/201),其中SCT组发生率为41.7%(15/36),非SCT组发生率为31.5%(52/165)(P=0.242)。
- 匹配队列中,HCC总发生率为32.4%(35/108),其中SCT组发生率为41.7%(15/36),非SCT组发生率为27.8%(20/72)(P=0.146)。PSM前后两组间HCC累积风险函数差异均无统计学意义(均P>0.05)。
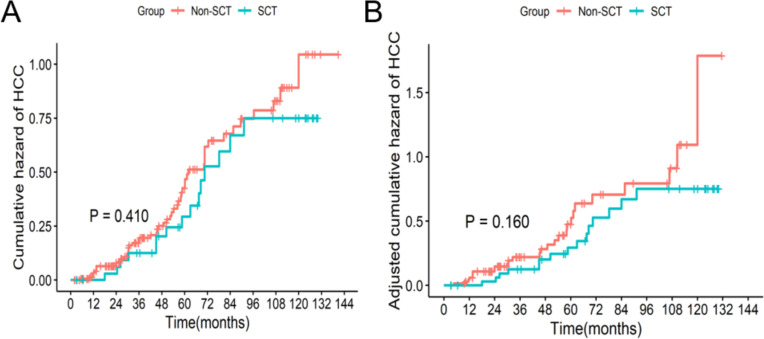
安全性评估:研究结果还发现,HUCB-MSCT不会增加这些患者罹患HCC的风险。因此,得出结论,HUCB-MSCT是一种安全有效的肝硬化治疗方法,无论是长期还是短期。
综上所述,两组的3年和5年生存率分别为83.3%vs61.8%和63.9%vs. 43.6%,中位OS时间分别为92.50和50.80个月。HUCB-MSCT治疗是患者OS的独立有益因素。HUCB-MSCT会改善DLC患者的长期OS,而不会增加HCC的发生率。
干细胞治疗肝硬化的临床研究进展
截止2024年8月27日,在美国国立卫生研究院的最大临床试验注册库clinicaltrials.gov网站上注册的有关干细胞治疗肝硬化临床研究项目有75项,已完成的有20项。
国内注册项目包括:
| 研究标题 | NCT 编号 | 地位 | 状况 | 干预措施 | 赞助 | 学习类型 | |
|---|---|---|---|---|---|---|---|
| 1 | 人脐带间充质干细胞治疗肝硬化 | NCT02652351 | 未知状态 | 肝硬化 | 生物:人脐带间充质干细胞 | 深圳市黄蜂玉米生物技术有限公司 | 介入 |
| 2 | 通过肝动脉为肝硬化患者输注脐带间充质干细胞 | NCT01224327 | 未知状态 | 肝硬化 放射科 间充质干细胞 更多 1 | 生物:脐带间充质干细胞 药品:保守治疗 | 青岛大学 | 介入 |
| 3 | 间充质干细胞治疗肝硬化 | NCT01233102 | 暂停 | 肝硬化 | 药品:保守治疗程序:肝动脉灌注或静脉灌注 | 石毓芳 | 介入 |
| 4 | 人脂肪干细胞治疗肝硬化的临床试验研究 | NCT02297867 | 完全的 | 肝硬化 | 药品:脂肪干细胞 | 国熙干细胞应用技术股份有限公司 | 介入 |
| 5 | 评估ADSCs对肝硬化患者疗效和安全性的开放标签单臂 II 期研究 | NCT04088058 | 招聘 | 肝硬化 | 药品: GXHPC1 | 国熙干细胞应用技术股份有限公司 | 介入 |
| 6 | 间充质干细胞治疗失代偿性肝硬化 | NCT03945487 | 未知状态 | 失代偿性肝硬化 | 生物:脐带间充质干细胞 其他:综合治疗 | 北京302医院 | 介入 |
| 7 | 间充质干细胞移植治疗失代偿性肝硬化试验 | NCT03209986 | 未知状态 | 肝硬化 | 程序:经外周静脉移植间充质干细胞 其他:间充质干细胞 | 西京消化病医院 | 介入 |
| 8 | 肝硬化患者的异基因骨髓干细胞移植手术 | NCT01223664 | 未知状态 | 肝硬化 | 程序:同种异体骨髓干细胞移植 药品:保守治疗 | 中山大学 | 介入 |
| 9 | 干细胞治疗失代偿期酒精性肝硬化的研究 | NCT05155657 | 招聘 | 酒精肝硬化 | 生物:常规疗法加低剂量UCMSCs治疗 生物:常规疗法加中剂量UCMSCs治疗 生物:常规疗法加高剂量UCMSCs治疗 | 烟台毓璜顶医院 | 介入 |
| 10 | 脐带间充质干细胞治疗肝硬化患者 | NCT01220492 | 完全的 | 肝硬化 | 药品:传统治疗加MSC治疗 药品:常规加安慰剂治疗 | 北京302医院 | 介入 |
| 11 | 骨间充质干细胞(BMSC)经门静脉移植治疗肝硬化 | NCT00993941 | 未知状态 | 肝硬化 | 程序:自体骨髓间充质干细胞移植 药品:保守治疗 | 中山大学 | 介入 |
| 12 | 肝硬化患者的自体骨髓间充质干细胞肝动脉移植术 | NCT00976287 | 未知状态 | 肝硬化 | 程序:肝动脉灌注 程序:保守治疗 | 中山大学 | 介入 |
| 13 | SHED治疗失代偿期肝硬化的安全性和有效性 | NCT03957655 | 未知状态 | 肝硬化 | 生物: SHED组 | 长海医院 | 介入 |
| 14 | 人脐带间充质干细胞移植治疗失代偿期肝硬化患者 | NCT01342250 | 完全的 | 肝硬化 | 生物:常规疗法加低剂量hUC-MSCs治疗 生物:常规疗法加中剂量hUC-MSCs治疗 生物:常规疗法加高剂量hUC-MSCs治疗 | 深圳市贝克生物科技有限公司 | 介入 |
| 15 | 用于治疗失代偿性肝硬化的人脐带间充质干细胞(MSC-DLC-1b) | NCT05984303 | 尚未招募 | 失代偿性肝硬化 | 生物:人脐带间充质干细胞 | 北京302医院 | 介入 |
| 16 | 用于治疗失代偿性肝硬化的人脐带间充质干细胞(MSC-DLC-1) | NCT05227846 | 招聘 | 失代偿性肝硬化 | 生物:人脐带间充质干细胞 | 北京302医院 | 介入 |
| 17 | 用于治疗失代偿性肝硬化的人脐带间充质干细胞(MSC-DLC-2) | NCT05224960 | 尚未招募 | 失代偿性肝硬化 | 生物:脐带间充质干细胞 生物:安慰剂(不含 UC-MSCs 的解决方案) | 北京302医院 | 介入 |
| 18 | 肝硬化患者干细胞移植与传统疗法的疗效差异 | NCT01718587 | 未知状态 | 肝硬化 | 程序:通过介入手术进行干细胞移植 药品:抗病毒治疗(拉米夫定,其他抗病毒药物) | 中国武警总医院 | 介入 |
| 19 | 用人脐带间充质干细胞治疗失代偿性肝硬化 | NCT05121870 | 未知状态 | 失代偿性肝硬化 | 生物:脐带间充质干细胞 生物:含1%人血清白蛋白的盐水(不含UC-MSCs的溶液) | 北京302医院 | 介入 |
| 20 | 间充质干细胞移植治疗难治性原发性胆汁性胆管炎 | NCT03668145 | 未知状态 | 原发性胆道肝硬化 | 程序:间充质干细胞移植或通过外周静脉输注安慰剂 | 西京消化病医院 | 介入 |
| 21 | 脐带间充质干细胞输注治疗失代偿期肝硬化的临床试验 | NCT03529136 | 未知状态 | 失代偿性肝硬化 | 生物:UC-MSC | 山东齐鲁干细胞工程有限公司 | 介入 |
| 22 | 脐带间充质干细胞治疗原发性胆汁性肝硬化患者 | NCT01662973 | 未知状态 | 原发性胆道肝硬化 | 其他:常规加UC-MSC治疗 其他:常规加安慰剂治疗 | 北京302医院 | 介入 |
| 23 | 间充质干细胞治疗肾脏纤维化的安全性和有效性研究 | NCT03460223 | 未知状态 | 肾脏肝硬化 | 生物:地中海航运 | 南京医科大学 | 介入 |
| 24 | 间充质干细胞和调节性 T 细胞联合移植治疗终末期肝病的安全性和有效性研究 | NCT03460795 | 尚未招募 | 肝硬化 | 生物: MSC 和 Tregs | 南京医科大学 | 介入 |
| 25 | 异基因间充质干细胞治疗难治性原发性胆汁性肝硬化患者的疗效和安全性研究 | NCT01440309 | 未知状态 | 原发性胆道肝硬化 | 生物:生物:间充质干细胞药品:熊去氧胆酸 | 赵春华医学博士 | 介入 |
| 26 | 注射胶原支架™联合 HUC-MSCs 移植治疗失代偿期肝硬化患者 | NCT02786017 | 未知状态 | 失代偿性肝硬化 | 生物:常规治疗 生物:可注射胶原蛋白支架 +HUC-MSCs | 中国科学院 | 介入 |
| 27 | 人骨髓干细胞治疗HBV相关性肝硬化的安全性和有效性 | NCT01724697 | 未知状态 | 肝硬化 终末期肝病 | 其他:骨髓间充质干细胞移植其他:常规治疗 & 抗病毒治疗 | 中国空军军医大学 | 介入 |
| 28 | 人自体外周血干细胞治疗 HBV 相关性肝硬化的安全性和有效性 | NCT01728688 | 未知状态 | 肝硬化 终末期肝病 | 其他: PBSC移植 其他:常规治疗 | 中国空军军医大学 | 介入 |
| 29 | 人脐带间充质干细胞治疗HBV相关性肝硬化的安全性和有效性 | NCT01728727 | 未知状态 | 肝硬化 终末期肝病 | 其他: UC-MSC 移植 其他:常规治疗 | 中国空军军医大学 | 介入 |
| 30 | 人脐带间充质干细胞在乙型肝炎肝硬化(补偿期)患者中的应用研究 | NCT05507762 | 未知状态 | 乙型肝炎导致的肝硬化 | 生物:脐带间充质干细胞 生物:盐溶液 | 武汉大学人民医院 | 介入 |
| 31 | 门静脉高压手术中通过肝动脉灌注 ABMSC以治疗肝硬化 | NCT01560845 | 未知状态 | 肝硬化 门脉高压症 肝功能衰竭 更多 | 程序:自体骨髓干细胞输注(ABMSCi)加腹部门脉高压症手术 程序:开放式腹部门脉高压症手术 | 温州医科大学 | 介入 |
| 32 | 自体骨髓单核细胞在肝硬化中的应用 | NCT05442437 | 完全的 | 乙型肝炎 | 生物:人类脐带间充质干细胞 | 中南医院 | 介入 |
| 33 | 干细胞移植治疗肝硬化的安全性和有效性 | NCT01491165 | 未知状态 | 其他外科手术 | 程序:通过介入手术进行干细胞移植 | 中国武警总医院 | 介入 |
| 34 | 自体间充质干细胞移植治疗难治性腹水肝硬化患者 | NCT01854125 | 未知状态 | 血液中的免疫功能血液中的肝功能腹水变异另外2个 | 生物:自体骨髓间充质干细胞移植 生物:自体骨髓间充质干细胞移植 | 南京解放军总医院 | 介入 |
| 35 | hUC 间充质干细胞(19#iSCLife®-LC)治疗失代偿期乙型肝炎肝硬化乙型肝炎肝硬化 | NCT03826433 | 招聘 | 乙型肝炎 | 生物:外围设备 iv | 深圳市世科生物技术有限公司 | 介入 |
| 36 | 通过外周静脉输入脐带间充质干细胞的不同频率对ESLD患者的影响 | NCT06242405 | 尚未招募 | 终末期肝病 | 生物:脐带间充质干细胞 | 沈阳军区总医院 | 介入 |
| 37 | 不同剂量通过外周静脉输入脐带间充质干细胞对ESLD患者的影响 | NCT06167473 | 招聘 | 终末期肝病 | 生物:脐带间充质干细胞 | 沈阳军区总医院 | 介入 |
结论
临床研究结果显示干细胞治疗肝硬化是具有临床价值的,可以让患者肝功能有所改善,白蛋白、胆红素、乳酸脱氢酶及碱性磷酸酶水平有所恢复并且可以提高肝硬化患者的生存率。
尽管干细胞治疗总体上安全,仍存在一些潜在风险,例如,低热和头晕和轻微不适反应。因此,患者在接受干细胞治疗前需要进行详细的检查和评估,并在专业医生的指导下进行治疗。
随着研究的深入和技术的成熟,我们期待干细胞治疗能够在肝硬化治疗中发挥更大的作用。
相关阅读:了解更多关于干细胞治疗肝硬化的新闻资讯!
【1】Zhang, Z., Lin, H., Shi, M., Xu, R., Fu, J., Lv, J., Chen, L., Lv, S., Li, Y., Yu, S., Geng, H., Jin, L., Lau, G.K.K. and Wang, F.-S. (2012), Human umbilical cord mesenchymal stem cells improve liver function and ascites in decompensated liver cirrhosis patients. Journal of Gastroenterology and Hepatology, 27: 112-120. https://doi.org/10.1111/j.1440-1746.2011.07024.x
【2】付庆春、金银鹏、王小金、李莉、王曦、李洪超、王兆京、周峰、臧祖胜、史立勤、李振宇、陈成伟.输注人脐带间充质干细胞改善乙型肝炎失代偿期肝硬化患者的肝功能[J].中国组织工程研究, 2018, 22(25): 3993-4000.
【3】Shi, M., Li, YY., Xu, RN. et al. Mesenchymal stem cell therapy in decompensated liver cirrhosis: a long-term follow-up analysis of the randomized controlled clinical trial. Hepatol Int 15, 1431–1441 (2021). https://doi.org/10.1007/s12072-021-10199-2
【4】崔玲娜, 王晓锋, 孙瑞琪, 等. 自体外周血干细胞回输对失代偿期肝硬化患者远期疗效影响的研究. 中华肝脏病杂志. 2022年3月;30(3):279-284. DOI: 10.3760/cma.j.cn501113-20220228-00091. PMID: 35462483.
【5】Zepeng Li, Xiaoling Zhou, Lu Han, Meijie Shi, Huanming Xiao, Ming Lin, Xiaoling Chi,Human Umbilical Cord Blood-Derived Mesenchymal Stem Cell Transplantation for Patients with Decompensated LiverCirrhosis,Journal of Gastrointestinal Surgery,Volume 27, Issue 5,2023,Pages 926-931,ISSN 1091-255X,https://doi.org/10.1007/s11605-022-05528-1.(https://www.sciencedirect.com/science/article/pii/S1091255X23000136)
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。
版权说明:本文来自杭吉干细胞科技内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台,转载授权请在网站后台下方留言获取。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号