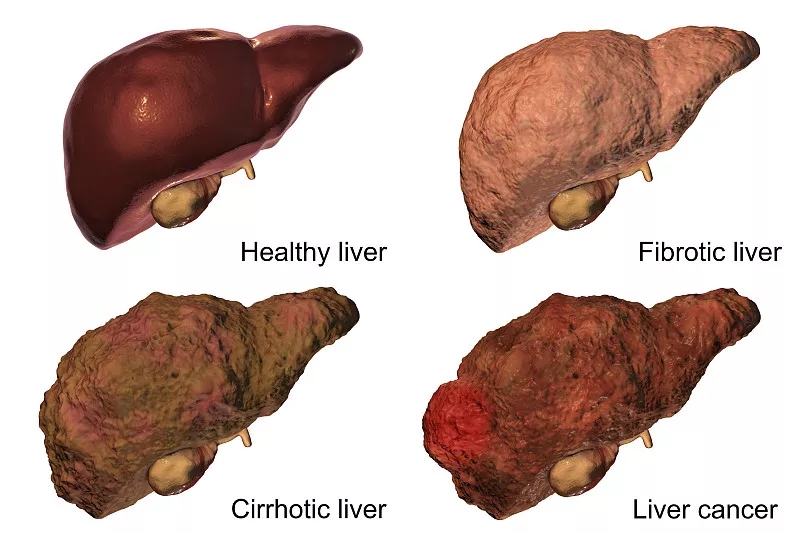
肝纤维化是由持续性损伤引起的,这可能由多种因素造成,例如病毒、药物、酒精、代谢疾病和自身免疫攻击。长期暴露于这些有害因素会导致肝细胞凋亡、炎症细胞募集、内皮细胞损伤,最后会导致肝星状细胞(参与肝纤维化的主要细胞)的活化。肝纤维化是一种对肝损伤作出反应的瘢痕组织形成。组织学上,它是由细胞外基质合成和降解之间的不平衡引起的。
肝硬化是一种疤痕组织取代肝脏的健康组织,并且由于损伤而形成周围纤维带的再生结节。肝硬化是各种原因的进行性肝病的共同终点,导致慢性肝功能衰竭,并伴有肝性脑病、自发性细菌性腹膜炎、腹水和食管静脉曲张等并发症。不幸的是,大多数病例在确诊时通常处于不可逆转的状态。尽管目前在其管理方面取得了进展 ,但2012年肝硬化是全球第14位主要死因。众所周知,原位肝移植是终末期肝硬化的唯一明确解决方案。
然而,一些问题排除了该程序的普遍应用,包括免疫排斥和供体来源的稀缺。
事实上,肝脏在很大程度上具有固有的再生能力,因此,这些有害因素的停止可能会阻止纤维化的进一步进展并在某些情况下扭转这种情况。在肝细胞增殖不足以从肝损伤中恢复的情况下,双能常驻肝祖细胞 (LPC) 被激活并通过分化为肝细胞和胆管上皮细胞参与肝再生。然而,当破坏超过再生时,纤维化是不可避免的。肝功能衰竭的临床症状通常在大约80%至90%的肝实质被破坏后出现。
肝细胞移植已被提议作为移植的替代方法,因为肝细胞已被证明与肝脏修复密切相关。虽然肝细胞移植在人体中是安全的,但由于器官可用性、供体移植失败、细胞培养中的活力弱以及易受冷冻保存损伤,其适用性仍然有限。根据最近的实验研究和人体研究,干细胞移植已显示出改善肝功能的治疗潜力,而不是肝细胞。尽管尚不清楚,但主要的潜在机制已被提出为双重的;一是通过旁分泌作用改善微环境,二是功能性肝细胞的替代。
目前关于干细胞治疗肝硬化的观点
迄今为止,已经研究了几种干细胞在肝硬化中的治疗可行性和临床潜力。本文根据干细胞的类型简要回顾了当前的文献,并讨论了干细胞在治疗肝硬化的未来前景。
干细胞来源
通过接受骨髓移植的患者尸检获得的肝细胞表明它们是骨髓中的多能细胞。目前,已知至少三种类型的骨髓衍生细胞分化为肝细胞样细胞 (HLC):造血干细胞 (HSC)、间充质干细胞 (MSC) 和内皮祖细胞 (EPC),尽管早期输注试验并未将这些细胞的来源与骨髓来源的基质细胞区分开来,但有一些改善。大量临床前研究已经证明 HSC、MSC和EPC在肝损伤模型中恢复肝功能的可行性。此外,包括胚胎干细胞 (ESCs) 和诱导多能干细胞 (iPSCs) 在内的其他干细胞也可以分化为HLC。HLC可促进肝硬化的重塑。
间充质干细胞治疗肝硬化的具体机制
目前对于移植的骨髓干细胞或间充质干细胞发挥治疗作用的具体机制有了初步的了解,机制可能包括:
(1) 直接分化:在肝脏损伤微环境的影响下定植、增殖,并分化成为肝细胞发挥作用;
(2) 旁分泌途径: 在肝损伤环境中间充质干细胞可以分泌不同水平的细胞因子相互影响,表现出抗炎症反应的作用,并可能激活肝内的肝干细胞,促进肝细胞再生;
(3)细胞融合: 间充质干细胞可能直接与肝细胞融合,进而启动细胞的增殖过程;
(4) 间充质干细胞通过高表达基质金属蛋白酶降解细胞外基质,直接降解肝内过量沉积的细胞外基质,减轻肝纤维化;
(5)间充质干细胞不仅能分化为肝细胞,而且在体内具有免疫调节的功能,减轻肝脏炎症反应和损伤。
使用干细胞治疗肝硬化的临床试验
早期自体骨髓干细胞移植可改善肝损伤和功能改善,它们可能包括HSC、MSC和EPC的混合细胞群。已经进行了一些小样本的单组 I 期临床研究,并在肝硬化患者中显示出一些前景。骨髓干细胞的输注有时被用作部分肝切除术患者的支持措施。尽管确切的机制仍未解决,但这些小样本研究的结果已经保证了手术后没有发生严重的并发症。此外,尽管存在持久的担忧,但肝细胞癌的移植后发病率并未增加。
一项使用人类胎儿肝源性干细胞招募25名肝硬化患者的试验表明,终末期肝病 (MELD) 评分的平均模型得到改善,尽管长期结果未得到适当报告。自Pai等人以来,已经有几项使用HSC的临床研究取得了有希望的结果。报道自体输注CD34+细胞可改善血清白蛋白水平和Child-Pugh评分。然而,大多数结果仅显示出暂时的影响,仍有许多问题有待回答。
最常研究的干细胞是间充质干细胞。因此,它们的作用机制也得到了更好的理解。特别是,BM-MSCs已被广泛使用。在两项早期试点研究中,据报道在少数患者中自体注射BM-MSCs可改善肝功能。BM-MSCs的安全性和短期疗效在两组各20名患者中得到证实,这表明Child-Pugh和MELD评分显著提高。随后的研究继续证实BM-MSC移植在不同大小的样本中的功效 。值得注意的是,与之前的报道相比,一项在肝硬化患者中使用自体MSCs的随机对照试验未能证明有益效果。
移植的细胞大部分是静脉输注,除了三项使用肝动脉的研究和一项直接注入脾脏的研究。注入细胞的数量和给药频率存在不小的变化。虽然整体研究质量没有超过中等或差的水平,但在MELD评分和肝功能改善方面,结果似乎很有希望。具体而言,大多数研究不包括组织学评估。
与其他种类的MSCs一样,脐带来源的MSCs (UC-MSCs) 在临床试验中进行了评估。脐带间充质干细胞输注耐受性良好,可显着改善功能并提高存活率。
总而言之,干细胞治疗肝硬化患者的干细胞试验已经证明了广泛的功能改善。此外,MELD和Child-Pugh评分也有所改善。不幸的是,这些有益效果随着时间的推移而减弱或未被测量。因此,根据两项系统评价(表1),可以暂时得出结论,使用干细胞的治疗可能略优于目前的常规治疗。
| 试用号 | 学习阶段(类型) | 细胞来源 | # | 资格标准 | 主要结果指标 | 次要结果测量 | 大体时间 | 开始日期 | 结束日期 | 地点 |
|---|---|---|---|---|---|---|---|---|---|---|
| NCT01875081 | 第二阶段(随机开放) | 骨髓间充质干细胞 | 72 | 组织学或临床诊断为酒精性肝硬化, 分类为Child-PughB级或C级 | 组织病理学评估 | 组织病理学评估评分、MELD评分、Child-Pugh分级等 | 6个月 | 2012.11 | 2016.03(已完成) | 韩国 |
| NCT02943889 | 第一阶段/第二阶段(非随机开放) | 骨髓间充质干细胞 | 40 | 失代偿性肝硬化儿童b级或c级 | 以儿童评分改善的形式改善肝功能 | 推迟或克服肝移植并发症 | 6、24个月 | 2016.10 | 2017.08(尚未招募) | 没有任何 |
| NCT02786017 | I/II 期(随机双盲对照) | 间充质干细胞 | 40 | 任何原因失代偿性肝硬化的受试者Child-pugh评分≥7 | 终末期肝病(MELD)评分模型的变化 | Child-Pugh 评分、肝功能临床实验室参数的变化 | 1 和 3 天 1 和 2 周 1、3、6、12 和 24 个月 | 2016.05 | 2018.12(招聘) | 中国 |
| NCT01591200 | 第二阶段(随机开放) | 同种异体间充质干细胞 | 40 | 儿童B级或C级,Child-Pugh 分数≥7且14 MELD分数至少 10 | 安全 | 肝功能改善、Child-Pugh评分、MELD评分、SF36-QOL等 | 24个月 | 2012.06 | 2016.04(已完成) | 印度 |
| NCT01120925 | I/II 期 (随机四盲控制) | 骨髓间充质干细胞 | 30 | MELD评分为12 或儿童评分B或 C 血清ALT比正常值高1/5倍 | 肝功能检查 | 肝硬化死亡率 | 6个月 | 2010.05 | 2013.07(已完成) | 伊朗 |
| NCT00420134 | I/II 期 (随机单 盲) | MSC | 30 | MELD评分至少为10 活体彩色多普勒检查门静脉开放 正常甲胎蛋白血清水平 | 肝功能检查 MELD评分 | 肝硬化死亡率 | 6个月 | 2006.02 | 2009.06(已完成) | 伊朗 |
| NCT01013194 | 第一阶段/第二阶段(非随机开放) | FLC | 25 | 基于Child-Pugh-Turcotte 分类的分数≥B8 和/或MELD分数≥14 | 生存 | 从基线到 1 年随访的 Child-Pugh 评分、融合评分分析 | 6个月和12个月 | 2007.02 | 2011.07(已完成) | 意大利 |
| NCT01342250 | I/II 期(随机开放) | 间充质干细胞 | 20 | 失代偿性肝硬化,Child-Pugh B/C(7-12分)或Meld评分≤21。 | 生存 | 肝功能改善、Child-Pugh评分、MELD评分、SF36-QOL等 | 24个月 | 2010.10 | 2011.10(已完成) | 中国 |
| NCT02652351 | 一期(开放) | 间充质干细胞 | 20 | 肝硬化的临床、放射学或生化证据 | 不良事件的严重程度 | 肝功能、肝纤维化指数 | 1、3、6 和 12 个月 | 2016.03 | 2016.10(招聘) | 中国 |
| NCT01147380 | 第一阶段(非随机开放) | NK细胞 | 18 | 需要满足肝移植资格标准的受试者 心肺功能 | 尸体供肝 NK 细胞输注的副作用 | NK细胞输注相关毒性、抗HCC、HCV作用 | 12 个月和 24 个月 | 2010.06 | 2014.12(已完成) | 美国 |
| NCT03254758 | 一期/二期(开放) | AD-MSC | 15 | 慢性丙型肝炎或非酒精性脂肪性肝炎 (NASH) Child-Pugh B 级肝硬化 | Child-Pugh 评分、安全概况 | Child-Pugh 评分、安全概况 | 6个月 | 2017.07 | 2018.12(招聘) | 日本 |
| NCT01333228 | 一期/二期(开放) | BM-EPC | 14 | 肝硬化(Child-Pugh8或以上) | 安全性和耐受性 | 对肝功能、门脉高压、肝硬化并发症的影响 | 12个月 | 2012.06 | 2015.03(已完成) | 西班牙 |
| NCT01503749 | 第一阶段(随机 开放) | PB-MNC (G-CSF) | 9 | Child-Pugh评分8或9的晚期肝硬化 | 严重不良事件 | Child-Pugh 评分和 MELD 评分的变化 | 1–4 周 2–6 个月 | 2012.01 | 2014.08(已完成) | – |
| NCT00713934 | I/II 期(随机单 盲) | BMMNC BMHSC | 7 | 肝活检显示组织学肝硬化,B级或C级(Child-Pugh评分) 超声检查研究中的肝硬化 超声 检查研究中的肝硬化 | 肝功能检查 MELD评分 | 肝硬化死亡率 | 6个月 | 2008.01 | 2009.02(已完成) | 伊朗 |
| NCT02297867 | 一期(开放) | 脂肪干细胞 | 6 | 调查人员无 HBV、HCV、HIV、梅毒等 | MELD | 没有任何 | 1-6个月 | 2015.07 | 2018.01(活跃中,未招募) | 台湾 |
| NCT02705742 | 一期/二期(开放) | AD-MSC | 5 | 临床、放射学和病理学证实的 HCV 肝炎引起的肝硬化 | 全因死亡率 | – | 12个月 | 2016.01 | 2017.12(招聘) | 土耳其 |
| NCT01454336 | 一期(开放) | 骨髓间充质干细胞 | 3 | 通过弹性成像、活检、超声检查证实肝硬化 | ALT、AST、血清白蛋白、肝纤维化 | 纤维化的进展 | 12个月 | 2010.06 | 2013.07(已完成) | 伊朗 |
结论
肝纤维化进展为肝硬化,这是实质细胞外基质沉积的结果。肝硬化的治愈性治疗目前仅限于原位肝移植,全球供体器官短缺导致等待器官的患者死亡。从实验和临床研究中积累的证据表明,干细胞治疗的方法已成为治疗肝硬化的一种有前途的疗法。已经研究了包括MSC、HSC、EPC、ESC和iPSC在内的多种干细胞的可行性和/或临床潜力。
其中,间充质干细胞研究最多,也比较了解。一种主要的作用机制被认为是旁分泌效应而不是转分化。从功能改善和临床参数的角度来看,临床试验的结果似乎非常有希望。然而,长期疗效尚未得到证实,需要标准化的试验方案。新技术有望克服目前与干细胞疗法临床应用相关的障碍。
参考资料:Kwak KA, Cho HJ, Yang JY, Park YS. Current Perspectives Regarding Stem Cell-Based Therapy for Liver Cirrhosis. Can J Gastroenterol Hepatol. 2018 Jan 29;2018:4197857. doi: 10.1155/2018/4197857. PMID: 29670867; PMCID: PMC5833156.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号