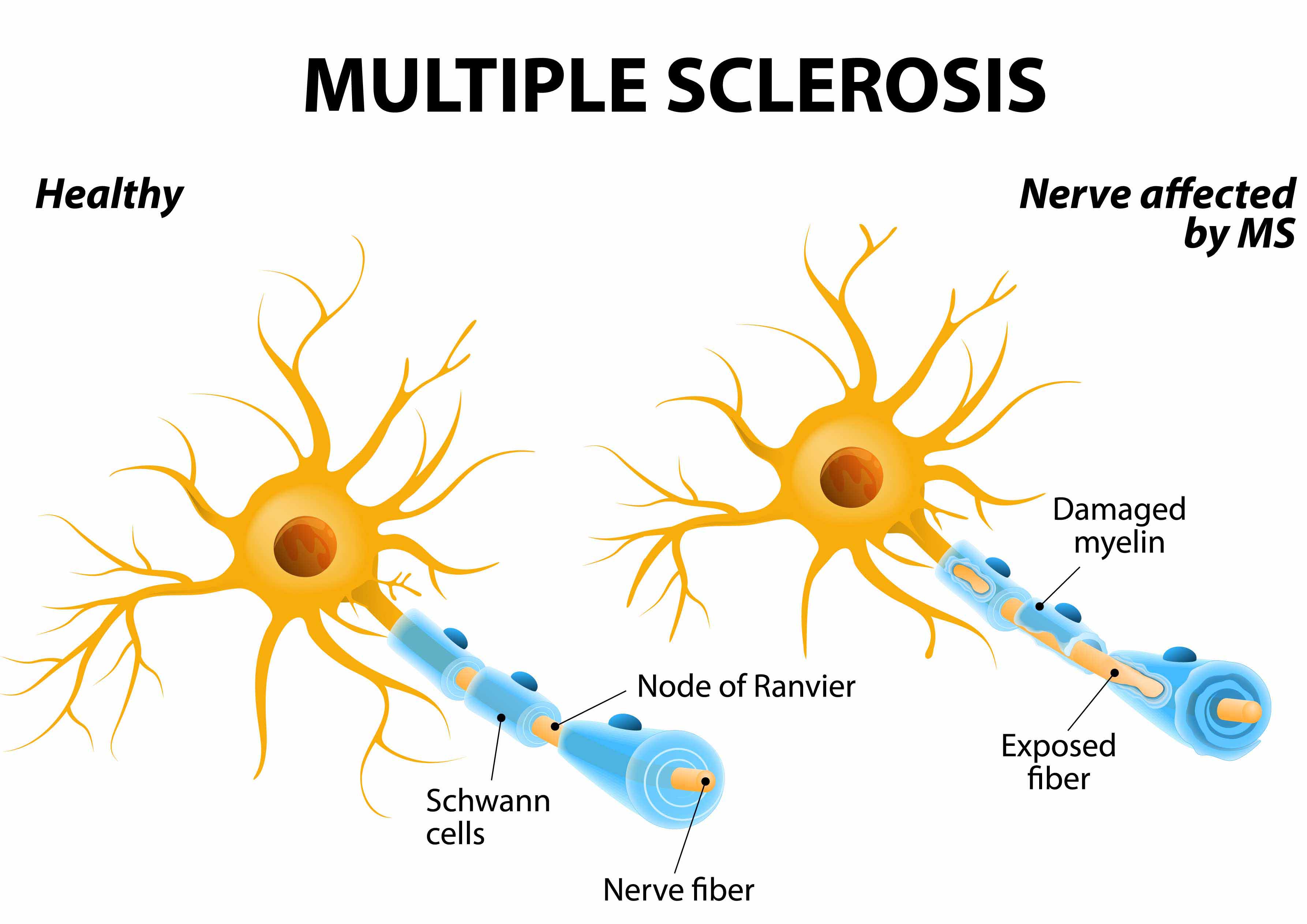
多发性硬化症是由针对神经细胞“髓鞘”的错误自身免疫反应(攻击)引起的。髓鞘很像电缆的绝缘层。它的作用是对神经进行电绝缘,起到保护作用,保证神经系统的正常功能(见图1)。该保护层的损坏或退化将导致受影响神经的正常功能受损。损伤的严重程度因人而异。
根据间充质干细胞对神经和免疫系统的再生作用,可以有效治疗所有类型的多发性硬化症,例如:复发缓解型多发性硬化症(RRMS)、原发性进展型多发性硬化症(PPMS)和继发性进展型多发性硬化症(SPMS)。
多发性硬化症:诊断 – 治疗 – 药物治疗 – 干细胞疗法
在此页面上,我们将向您介绍MS,其中概述了病因、治疗方案、精确诊断的重要方面以及干细胞疗法。
常规治疗多发性硬化症的方法
目前用于多发性硬化症 (MS) 的药物和药物用于减缓疾病的进展并减轻其症状。已知这些药物会抑制导致 MS 神经系统症状的一般免疫反应。很少能实现先前症状的逆转和疾病进展的预防。物理疗法和肌肉松弛剂(例如替代类大麻素疗法)等疗法可以极大地帮助患者,但也不会减缓进展或恢复功能。
此外,所使用的免疫抑制剂具有多种副作用,在许多情况下,干扰素治疗会将复发-缓解模式转变为对生活质量具有严重影响的继发性进展模式。由于这种影响,许多患者停止了干扰素治疗。
干细胞疗法与多发性硬化症
因此,基于干细胞的疗法最近已成为MS的一种有前途的新型治疗选择。干细胞已证明对免疫系统具有有益作用,而且还能刺激MS引起的神经损伤的再生。因此,基于干细胞的疗法是治疗该疾病的新兴选择。它们调节免疫系统的天然能力是基于可溶性因子的细胞间通讯,这种天然的调节方式在未来可能会更加有益,尽管干细胞也无法治愈MS。
干细胞似乎对治疗这种严重的自身免疫性神经退行性疾病有两个主要的有益作用,因为它们被证明可以:
- 改变免疫系统的作用,例如防止髓鞘受到进一步攻击(神经保护)
- 修复受损神经(髓鞘再生)
用基于干细胞的疗法治疗MS患者已经在外部临床试验中取得了很大成功。这些 I/II 期研究的有希望的结果表明:
- 减少炎症
- 提高视力并唤起改善的反应延迟
- 视神经面积增加
- 抑制新病灶的发展和减少病灶面积
- 与仅接受抗炎和免疫抑制治疗的患者相比,复发率降低
最重要的是,直到现在,在用干细胞治疗多发性硬化症患者时,还没有发现重大副作用。
干细胞疗法治疗多发性硬化症的可能机制
间充质干细胞是如何治疗多发性硬化症的呢?根据一些文献的研究,其作用机制主要是以下三个方面:
1、分化作用
间充质干细胞具有显著的归巢能力,目前已被用于治疗中枢神经系统性损伤。在正常动物体内,骨髓衍生的间充质干细胞大多数归巢于骨髓,而在一些炎性反应较活跃部位,间充质干细胞倾向于向病变区域聚集,迁移到白质病变区,分化成神经细胞和多种间质细胞,促进神经元的再生和髓鞘重建(少突胶质细胞的分化)。
2、免疫调节作用
免疫学、遗传学和组织病理学研究表明,免疫系统在多发性硬化症的进展中发挥着重要作用,而且最新研究显示先天性及获得性免疫反应对多发性硬化症的进展均具有主要影响。而间充质干细胞具有明显的免疫调控和免疫抑制的作用,且其对先天性和获得性免疫系统的调节能力已在各种自体免疫性疾病中获得临床验证,并可在临床上用于减轻神经功能障碍。
3、内分泌作用
间充质干细胞分泌神经营养因子和生长因子,其能够有效的诱导增殖、迁移和神经内源性祖细胞的分化,从而保护和诱导损伤组织的再生。Munoz等将骨髓间充质干细胞移植到免疫缺陷型小鼠的齿状回,结果显示,植入的间充质干细胞可明显增加内源性神经干细胞的增殖及分化,证明了内源性神经干细胞的增殖和分化与间充质干细胞分泌的生长因子如血管内皮生长因子(VEGF)、睫状神经营养因子(CNTF)、神经生长因子(NGF)密切相关。
更重要的是,有研究发现,单独注射由间充质干细胞分泌的蛋白质可调控小鼠海马神经元的分化,而间充质干细胞分泌的蛋白可调控少突胶质细胞的微环境。间充质干细胞表达的DKK-1蛋白因子作为Wnt信号通路中重要的拮抗分子,可存进神经突的形成,是神经突形成的必要因子;间充质干细胞分泌的神经营养性因子和细胞外基质分子均被证明可支持神经细胞的连接、神经细胞的生成以及轴突延伸等。此外,Neuhuber等还认为,间充质干细胞产生的神经营养因子对于轴索生长,以及脊髓损伤后的功能恢复至关重要。
早中期多发性硬化症的治疗流程
所有疗法都分为多个阶段,例如病史评估(我们分析您当前的疗法和病历)、初步咨询和潜力评估、干细胞疗法对患者个体的益处(适应症声明)、初步检查、诊断、就所有治疗方案进行咨询,制定个人治疗计划,包括成本估算、组织采集、干细胞产品生产、产品质量控制和应用。
不幸的是,我们只治疗早期至中期的MS患者。患者需要能够独立呼吸,需要适应镇静和收集脂肪所需的短暂干预。根据风险收益比,我们不能治疗儿童或孕妇。此外,其他因素也可以作为排除标准。
干细胞治疗的费用是多少?
我们的治疗始终根据您的具体情况、疾病、阶段和其他因素量身定制。这些疗法在使用的产品(BMC、分泌蛋白、PRP 或透明质酸)、治疗频率以及进一步检查以及您的镇静和麻醉意愿方面有所不同。MS 的治疗费用将远高于一万欧元。您将提前收到所有治疗的费用估算,以便您可以准确估算您的个案的治疗费用。
常见问题解答:干细胞治疗多发性硬化症的问题
什么是多发性硬化症?
多发性硬化症 (MS) 是一种中枢神经系统疾病,包括脊髓和大脑。在MS患者中,免疫系统会攻击包裹在神经纤维周围的保护鞘。这种鞘称为髓鞘。这种自身免疫攻击会导致神经系统受损,并可能导致大脑与身体其他部位之间的沟通问题。
MS可能会致残,因为它会对神经造成永久性损伤。
目前没有可以治愈MS的治疗方法。然而,有些疗法可能有助于缩短发作后的恢复时间、改变病程和控制症状。
多发性硬化症的症状是什么?
不幸的是,多发性硬化症是具有多种症状的疾病之一,使得潜在患者难以立即识别。它们也因患者而异,并且会随着时间而改变。所有这一切都是由于不同的神经纤维会受到影响,因此,症状可能会有所不同。
许多症状与运动障碍有关;例子是:
- 四肢麻木/无力。这也可能一次发生在身体的一侧
- 震颤和缺乏协调,包括不稳定的步态
- 某些颈部运动时会出现不舒服的电击感,尤其是向前弯曲颈部(Lhermitte 征)
- 身体不同部位刺痛/疼痛
一些症状与视力障碍有关;例子是:
- 视力丧失,通常一次是一只眼睛
- 眼球运动时疼痛
- 长时间复视
- 视力模糊
其他症状可能包括:
- 疲劳和头晕
- 言语障碍
- 性功能、节制和排便功能受损
多发性硬化症的病因是什么?危险因素有哪些?
MS 被认为是一种自身免疫性疾病,因为患者自身的免疫系统攻击身体的一部分,在这种情况下是神经纤维。不幸的是,MS的病因尚不清楚。
目前的科学假设是,潜在的机制要么与免疫系统的破坏有关,要么与髓鞘生成细胞的衰竭有关。
科学家们认为,这可能是环境因素(例如病毒感染)和导致该疾病的遗传因素的结合。
可能增加患MS风险的因素:
- 年龄:虽然这种疾病可以发生在任何年龄的患者身上,但通常发生在 20 至 40 岁之间。
- 性别:女性患复发缓解型 MS 的可能性是男性的 2 到 3 倍。
- 家族史:如果父母或兄弟姐妹患有 MS,则患 MS 的风险更高。
- 特定病毒感染:一些病毒与 MS 相关,例如 Epstein-Barr。
- 种族:白人患 MS 的风险最高,而亚洲、非洲或美洲原住民后裔的风险最低。
- 维生素 D 缺乏症:当维生素 D 水平低和/或阳光照射少时,患 MS 的风险更高。
多发性硬化症的类型、病程和并发症
已经描述了几种类型和进展模式。疾病的分类考虑了过去的病程以预测未来的病程。这对于能够确定预后和做出合理的治疗决定是必要的。
目前,可以描述四种类型的 MS:
- 临床孤立综合征 (CIS)
- 复发缓解型 MS (RRMS)
- 原发性进展型多发性硬化症 (PPMS)
- 二次进展型多发性硬化症 (SPMS)
大多数MS患者最初经历的是复发-缓解型,其特征是不可预测的复发,随后是症状部分或完全改善的较长时间的缓解期。在缓解期间,没有新的疾病活动迹象。复发缓解型MS通常以临床孤立综合征 (CIS) 开始,在这种情况下,患者会出现提示脱髓鞘的发作,但不符合MS的标准。
在10%到20%的患者中,发生原发性进行性MS。在这里,初始症状后没有缓解,其特征是残疾从发作开始进展,没有或只有轻微的缓解和改善。至少一半的初始复发-缓解型患者会发生继发性进展型MS。当发生这种情况时,患者将在急性发作之间出现进行性神经功能衰退,而没有任何明确的缓解期。在这些情况下,可能会偶尔出现复发和轻微缓解。当他们处理继发性进行性MS时,疾病进展因患者而异。
不幸的是,MS 也会引起许多其他并发症。多发性硬化症患者可能会出现:
- 麻痹
- 癫痫
- 肌肉僵硬/痉挛
- 健忘、情绪波动、抑郁和其他精神障碍
为什么现代医学应该使用干细胞治疗多发性硬化症——科学背景:

© Bruce Blaus;https://en.wikipedia.org/wiki/Multiple_sclerosis#/media/File:Multiple_Sclerosis.png
“多发性硬化症是由神经细胞髓鞘遭到破坏引起的,而髓鞘可以通过使用干细胞治疗进行重建”。
在过去十年中,干细胞研究揭示了利用间充质干细胞 (MSC) 减少炎症和有益地调节免疫系统的巨大潜力。除了免疫抑制能力外,MSCs还被证明可以刺激各种受损组织的再生。
干细胞所谓的旁分泌活动的特点是对受损组织和神经元产生再生作用。旁分泌作用描述为细胞分泌的重要因子的产生,用于周围细胞和组织之间的有效通讯。干细胞本身已被证明可以产生这些因子来启动与受损细胞和组织的通讯通路,从而触发和刺激它们的再生(见图2)。再生因子由生长因子、细胞因子和调节细胞周期的miRNA组成。它们被包裹在脂质壳(外泌体和微泡)中用于信息传输,即在整个身体中传输。
新的科学数据不断涌现,进一步证实和阐述了基于干细胞的治疗方法对神经退行性疾病和自身免疫性疾病的益处。有关当前干细胞研究的更多详细信息,请单击此处。
科学家和医生看到了干细胞在显着改善MS症状和减缓疾病进展方面的巨大潜力。在未来,可能有可能完全阻止 MS 的发展,甚至可能治愈该疾病,使用干细胞或干细胞与其他措施相结合。但要达到治愈 MS 的最终目标,还需要更多的临床工作。
参考资料:
Fox, R. J. & Ransohoff, R. M. New directions in MS therapeutics: vehicles of hope. Trends Immunol. 2004; 25(12):632-6.
Caplan, A. I. Adult mesenchymal stem cells for tissue engineering versus regenerative medicine. J Cell Physiol. 2007; 213(2):341-7.
Gianvito Martino, Robin J. M. Franklin, Anne Baron Van Evercooren, Douglas A. Kerr. Stem cell transplantation in multiple sclerosis: current status and future prospects. Nat. Rev. Neurol. 2010; 6, 247–255.
Trapp, B.D. et al. Axonal transection in the lesions of multiple sclerosis. N. Engl. J. Med. 1998; 338, 278–285
Freedman MS, Bar-Or A, Atkins HL, Karussis D, Frassoni F, Lazarus H, Scolding N, Slavin S, Le Blanc K, Uccelli A; MSCT Study Group. Study Group The therapeutic potential of mesenchymal stem cell transplantation as a treatment for multiple sclerosis: consensus report of the International MSCT Study Group. Multiple Sclerosis. 2010; 16(4) 503–510.
Karussis D, Karageorgiou C, Vaknin-Dembinsky A, Gowda-Kurkalli B, Gomori JM, Kassis I, Bulte JW, Petrou P, Ben-Hur T, Abramsky O, Slavin S. Safety and Immunological Effects of Mesenchymal Stem Cell Transplantation in Patients With Multiple Sclerosis and Amyotrophic Lateral Sclerosis. Arch Neurol. 2010; 67(10):1187-1194.
Connick P1, Kolappan M, Crawley C, Webber DJ, Patani R, Michell AW, Du MQ, Luan SL, Altmann DR, Thompson AJ, Compston A, Scott MA, Miller DH, Chandran S. Autologous mesenchymal stem cells for the treatment of secondary progressive multiple sclerosis: an open-label phase 2a proof-of-concept study. Lancet Neurol 2012; 11: 150–56.
Llufriu S, Sepúlveda M, Blanco Y, Marín P, Moreno B, Berenguer J, Gabilondo I, Martínez-Heras E, Sola-Valls N, Arnaiz JA, Andreu EJ, Fernández B, Bullich S, Sánchez-Dalmau B, Graus F, Villoslada P, Saiz A. Randomized Placebo-Controlled Phase II Trial of Autologous Mesenchymal Stem Cells in Multiple Sclerosis. PLoS One. 2014; 1;9(12).
Li JF, Zhang DJ, Geng T, Chen L, Huang H, Yin HL, Zhang YZ, Lou JY, Cao B, Wang YL. The Potential of Human Umbilical Cord-Derived Mesenchymal Stem Cells as a Novel Cellular Therapy for Multiple Sclerosis. Cell Transplant. 2014; 23 Suppl 1:S113-22.
Tyndall A, Walker UA, Cope A, Dazzi F, De Bari C, Fibbe W, Guiducci S, Jones S, Jorgensen C, Le Blanc K, Luyten F, McGonagle D, Martin I, Bocelli-Tyndall C, Pennesi G, Pistoia V, Pitzalis C, Uccelli A, Wulffraat N, Feldmann M. Immunomodulatory properties of mesenchymal stem cells: a review based on an interdisciplinary meeting held at the Kennedy Institute of Rheumatology Division, London, UK, 31 October 2005. Arthritis Research & Therapy 2007; 9:301
Baraniak PR1, McDevitt TC. Stem cell paracrine actions and tissue regeneration. Regen Med. 2010; 5(1):121-43
Chandran S, Hunt D, Joannides A, Zhao C, Compston A, Franklin RJ. Myelin repair: the role of stem and precursor cells in multiple sclerosis. Philos Trans R Soc Lond B Biol Sci. 2008; 12;363(1489):171-83.
Bollini S, Gentili C, Tasso R, Cancedda R. The Regenerative Role of the Fetal and Adult Stem Cell Secretome. J Clin Med. 2013; 17;2(4):302-27
Yeo RWY, Lai RC, Tan KH Lim SK. Exosome: A Novel and Safer Therapeutic Refinement of Mesenchymal Stem Cell. Exosomes microvesicles. 2013, Vol. 1, 7.
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞不保证信息的准确性和完整性。所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号