干细胞治疗正在成为中风患者的一种有吸引力的替代疗法,但仍需要就现有的方案达成一致,包括给药途径。
近日,Universitas Airlangga医学院神经外科在《Clinincal Medicine》临床医学杂志上面发表了一篇文章,文章内容阐述了干细胞通过不同给药途径治疗缺血性脑中风得到的临床结果和安全性也不同的系统评价。结果显示脑内给药显示出比其他途径更好的结果,但由于其侵入性,随之而来的不良事件数量更多。不良事件显示与中风的自然史有关,与治疗无关。

简介:中风是世界范围内最主要的死亡原因之一,它仍然是全球卫生资源的巨大消耗。大多数中风本质上是缺血性的,约占美国所有病例的87%,这使其成为中风研究的主要焦点。尽管80%的中风患者在事故发生后可以存活一年,但仍有超过10%的患者存在长期残疾。
缺血性卒中后存活率的增加和后遗症的减少可能部分是由于溶栓疗法的急性期给药。唯一被批准用于急性中风的疗法是静脉内重组组织纤溶酶原激活剂 (tPA),其时间窗只有4.5小时。此外,接受紧急血管内治疗有严格的患者标准,而且获益尚不确定。由于未能达到预期的结果,因此迫切需要具有更长时间框架和更小侵入性方法的新治疗策略是很自然的。
大量研究已经证明了干细胞治疗在恢复中风患者功能能力方面的功效。除了它在不替换受损脑组织的情况下刺激内源性修复机制的潜力外,它还被证明可以促进免疫调节以及神经元、血管和胶质细胞重塑。干细胞治疗脑卒中患者的临床试验表明,该疗法是可行的、安全的,并能促进缺血性脑卒中的恢复。
方法:本综述包括对通过脑内、脑室内、蛛网膜下腔、动脉内、静脉内、腹膜内或鼻内给药接受干细胞治疗的成人缺血性中风患者(急性、亚急性或慢性)进行的全文队列研究和临床试验。
搜索信息:这些文章发表于2010年至2022年之间,是在2022年3月31日通过搜索PubMed、Scopus、Cochrane和其他电子数据库来源(谷歌学术搜索)获得的。(图1)

结果测量的类型:使用改良的Rankin量表 (mRS)、美国国立卫生研究院卒中量表 (NIHSS) 和Barthel 指数 (BI) 测量临床结果。分析了干细胞给药途径的不良事件 (AE) 和严重不良事件 (SAE),以确定每种治疗的安全性。
结果:总共确定并筛选了175项研究。其中,对33项进行了资格评估,将21项(11项PubMed研究、7项Scopus研究和3项Google Scholar研究)纳入荟萃分析。
人口统计学、干预时间、中风部位和干细胞类型
纳入的研究在亚洲、美国和欧洲进行。大多数研究来自亚洲(21项中有12项;57.1%),主要来自中国(21项中有5项;23.8%)。五项 (23.8%) 研究在美国进行,而欧洲的研究(21项中有5项;23.8%)主要在英国进行(21项中有3项;14.2%)。
在21项研究中,共纳入836名患者,中位年龄为60.6岁(范围30-85 岁)。干细胞治疗组由406名患者组成;247名 (60.83%) 参与者为男性,159名 (39.16%) 参与者为女性。
406名参与者中有333名 (82.02%) 报告了中风发作和干细胞给药的持续时间。大多数参与者 (35.22%) 在亚急性期接受了干细胞治疗,其次是慢性中风,有108名 (26.6%) 参与者,而其余的则患有急性中风 (20.2%)。
406名参与者中有339名 (83.49%) 报告了卒中血管化区域。大多数中风涉及大脑中动脉 (MCA) (87.6%),其次是大脑前动脉 (ACA) 和 MCA 受累 (2.4%),而后循环和 ACA 中风的发生率分别为2.09%和 1.8%。
施用了六种不同的干细胞类型和来源,即骨髓、外周血、脐带血、成体祖细胞和人类神经干细胞。大多数参与者接受了骨髓来源的干细胞治疗(265名参与者,65.27%),其次是多能干细胞(71名,17.49%),神经来源的外周血和脐血来源的干细胞分别给予20( 4.92%) 参与者。在最近的研究中,九名 (2.21%) 参与者使用了脂肪来源的干细胞(表3)。


给药途径:临床结果和不良事件
静脉注射组采用最常用的给药途径,由304名 (78.87%) 参与者组成。脑内组由64名 (15.76%) 参与者组成,而动脉内组由38名 (9.35%) 参与者组成。
临床结果
我们提取的临床结果数据为6个月(21项研究中的6项)、12个月(21项研究中的4项)和24个月的NIHSS(21项研究中的3项);6个月、12个月和24个月的mRS(各21项研究中的2项);6个月、12个月和24个月BI(分别为21项研究中的4项、21项研究中的2项和21项研究中的3项)。
6个月后的NIHSS临床结果显示,脑内注射组下降了6.96±2.36,动脉内注射组下降了2.2±1.92,静脉注射组下降了7.25±5.31。6个月后,脑内注射组的mRS评分也下降了3.34±0.63,动脉注射组下降了2.33 ±0.86,静脉注射组下降了2.63±0.90。BI评分的改善以6个月后增加为标志,脑内组为26±16.80,静脉内组为76.85±21.41,而动脉内组无可用数据。
干细胞治疗组12个月和24个月后,NIHSS和mRS评分有下降趋势,BI分数上升,表明临床结果更好(表4)。




不良事件(基于给药途径)
据报道,AE在21项研究中发生了431次,而SAE发生了101次 (26.09%)。这些数字因不同的给药途径而异。
静脉组282例 (65.42%) 患者发生AE,其中68例 (24.11%) 被归类为严重,占报告的静脉组AE患者的23.05%。
脑内组AE发生在123名 (28.53%) 患者中,其中28名 (22.76%) 被认为是严重的,占报告的脑内组AE患者的44.44%。
在动脉内组中,26例 (6.03%) 患者发生了AE,其中5例 (19.23%) 被归类为严重,占报告的动脉内组AE患者的17.24%。表5提供干细胞给药途径的不良事件的总结。

使用风险比分析,我们比较了干细胞组和对照组的AE和SAE风险。该分析涉及八项具有可用数据的研究。因此,亚组分析人群是异质的 (I2=72%)。结果显示,干细胞组发生AE的风险较低,尽管在统计学上不显着(图2)。
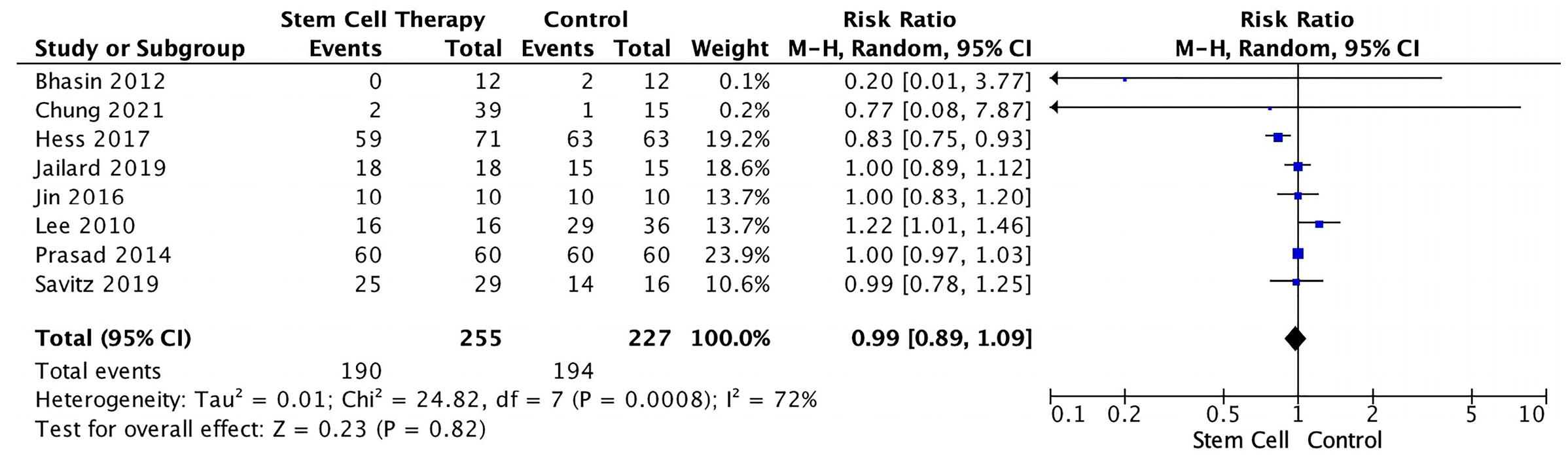
我们还比较了干细胞组和对照组的SAE风险。该分析涉及八项具有可用数据的研究。结果显示,干细胞组发生SAE的风险较低,但无统计学意义。亚组分析人群是同质的 (I2=0%)(图3)。
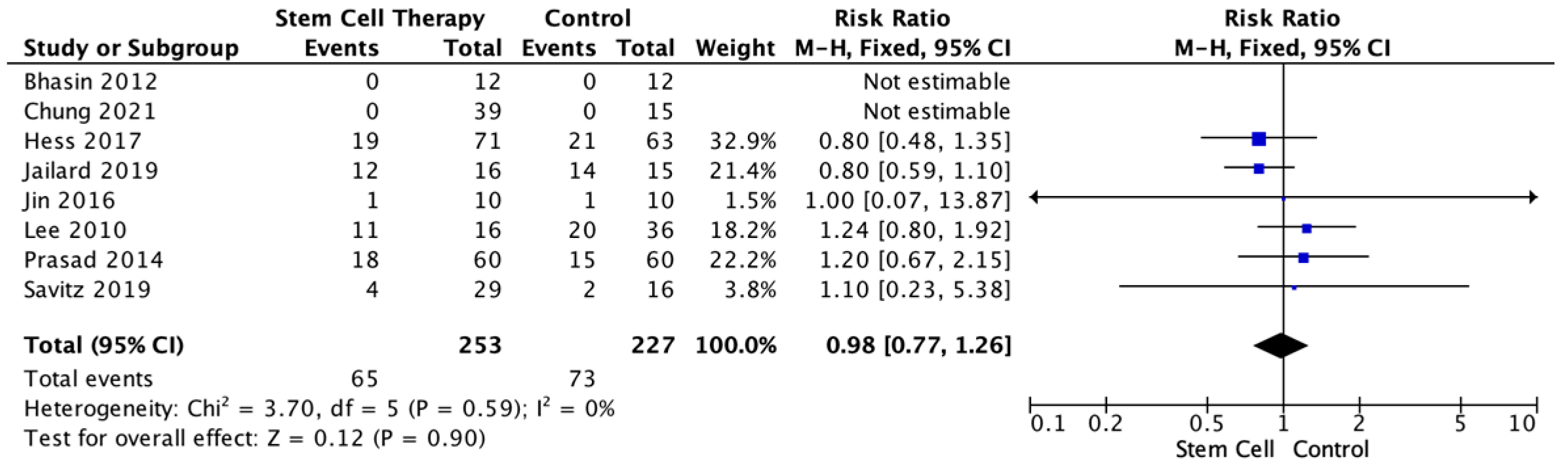
结论
总之,干细胞治疗缺血性脑卒中患者中显示出优于单独标准保守治疗的结果,但我们的数据表明,有几个因素(例如,患者的合并症、治疗时间、给药途径)可能会模糊治疗的益处和安全性。
据我们所知,本综述是第一项根据分娩途径确定功能结果和治疗不良事件的研究。使用各种递送方法的试验结果证明了积极的有效性和安全性。
虽然脑内注射比其他途径产生更好的神经学结果,但由于其侵入性,它与更高的AE发生率相关。另一方面,动脉内和静脉内途径的结果不尽如人意,但安全性最高,尽管大多数AE的发生与治疗方案无关。由于我们发现在本综述中的大多数纳入研究中,研究的结果和随访既多样又有限,因此需要进行更广泛和更有针对性的调查来评估这种未来治疗策略的有效性和安全性。
主要参考资料:Fauzi, A.A.; Thamrin, A.M.H.; Permana, A.T.; Ranuh, I.G.M.A.R.; Hidayati, H.B.; Hamdan, M.; Wahyuhadi, J.; Suroto, N.S.; Lestari, P.; Chandra, P.S. Comparison of the Administration Route of Stem Cell Therapy for Ischemic Stroke: A Systematic Review and Meta-Analysis of the Clinical Outcomes and Safety. J. Clin. Med. 2023, 12, 2735. https://doi.org/10.3390/jcm12072735
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号