概述:糖尿病肾病(DN)是糖尿病最严重的并发症之一。然而,由于其病理机制复杂,临床上多年来一直未应用有效的治疗方法(除ACEIs和ARBs外)。最近的研究表明,包括新型靶向药物疗法、细胞疗法和饮食调节在内的新兴疗法为 DN 的治疗带来了新的希望。
本综述旨在通过描述糖尿病肾病的重要病理机制,分析药物治疗、细胞治疗和饮食调节等临床治疗的最新进展,为糖尿病肾病的治疗提供新的思路。在病理机制方面,RAAS激活、AGE积累和EMT参与了炎症、细胞应激、细胞凋亡、热噬和自噬。在药物治疗方面,包括SGLT2抑制剂、GLP-1激动剂和MRAs在内的几种新疗法正受到公众的关注。此外,干细胞疗法和饮食调节也受到重视。在此,我们强调结合疗法和饮食调节治疗糖尿病肾病的重要性,并期待更多的基础研究或临床试验来验证新策略。
介绍
糖尿病及其并发症给公众健康带来了相当大的负担。不幸的是,遏制糖尿病及其并发症的各种尝试都失败了。糖尿病肾病(DN)是糖尿病最常见的并发症,也是终末期肾病的最常见原因。据统计,30%的糖尿病患者患有DN,从而给公众健康造成了相当大的负担。1997年至2017年间,DN占全球所有慢性肾病患者伤残调整生命年的三分之一,且其发病率逐年增加。肾脏和心血管风险事件是DN患者的最大威胁。有证据表明,严格的血糖和血压控制是治疗DN患者的重要工具。
此外,糖尿病患者的微量白蛋白尿已被认为是DN进展和预后的预测因子。因此,预防尿白蛋白排泄升高,以及减少和预防肾脏和心血管事件的发生是DN的重要治疗目标。
目前DN的药物治疗范围狭窄,主要基于应用ACEI和ARB来阻断RASS和控制血糖。其他药物用于补充和增强这种RASS阻断或血糖控制,例如SGLT2抑制剂、GLP-1激动剂、盐皮质激素受体拮抗剂和内皮素拮抗剂(下文将更详细地描述)。
除了药物治疗外,饮食调节也被推荐作为治疗糖尿病肾病的有效策略,从而控制血糖和减少蛋白尿。许多临床试验试图探索DN患者的合理饮食,如低蛋白饮食(NCT01521910、NCT00448526、NCT00363987和NCT03415074)、低血糖饮食(NCT02384902)、低热量饮食(NCT01671969)和低盐饮食(NCT01671969)。 NCT01918488)。这些限制性饮食调整已被证明有利于延缓DN的进展。此外,一些研究试图通过饮食干预来减轻肾脏AGE负担。值得注意的是,针对糖尿病肾病的干细胞疗法也逐渐兴起,如脐带间充质干细胞疗法(NCT04125329和NCT04216849)、间充质基质细胞疗法(NCT02585622)、肾自体细胞疗法(NCT03270956和NCT02836574)。
尽管许多努力为DN患者的管理提供了多种选择,但仍有许多患者的疾病难以控制,这促使研究人员寻求新的治疗靶点和方法,以开发和实施新的治疗机会。本文综述了糖尿病肾病的重要病理机制、临床试验中的药物研发、干细胞治疗和饮食调节等,为进一步研究提供新的参考。
糖尿病肾病的病理特点
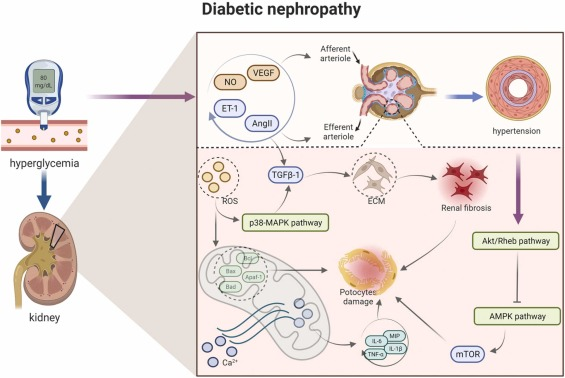
在DN状态下,肾细胞(包括足细胞、系膜细胞、内皮细胞和上皮细胞)中,肾素血管紧张素醛固酮系统(RAAS)激活,晚期糖基化终末产物(AGEs)积累,上皮间质转化(EMT)涉及炎症、细胞应激、细胞凋亡、细胞焦亡和自噬(图1)。
目前治疗糖尿病肾病的方法有哪些?
血糖和血压控制是DN治疗的一个重要方面。DN患者的高血糖管理,尤其是GFR降低的患者,是一个严峻的挑战。事实上,近20年来,血管紧张素转换酶抑制剂 (ACEIs) 和血管紧张素受体阻滞剂(ARB) 一直是DN 的唯一治疗选择。抗糖尿病药物经过几十年的发展,治疗选择更加多样化,主要包括第二代磺酰脲类药物(格列吡嗪和格列齐特)、胰岛素治疗、二肽基肽酶-4(DPP-4)抑制剂、胰高血糖素样肽-1(GLP- 1) 激动剂和钠-葡萄糖转运蛋白2 (SGLT2) 抑制剂。
本节讨论当前DN治疗方案的前景,包括ACEI/ARB,以及SGLT2抑制剂、内皮素拮抗剂、GLP-1激动剂和盐皮质激素受体拮抗剂(MRA) 等新型治疗方法,以及支持DN治疗的代表性临床试验。这些药物的使用(可在 https://clinicaltrials.gov/ 获取)(图2)。还讨论了其他新兴药物治疗方案,例如DPP-4抑制剂、磷酸二酯酶抑制剂和黄嘌呤氧化酶抑制剂(图3)。
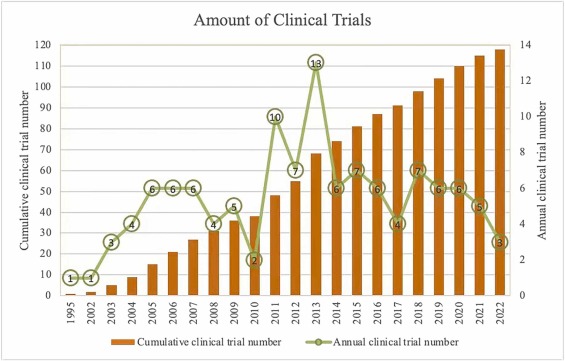
绿色圆圈数字代表年度临床试验编号。橙色条代表累积临床试验数。
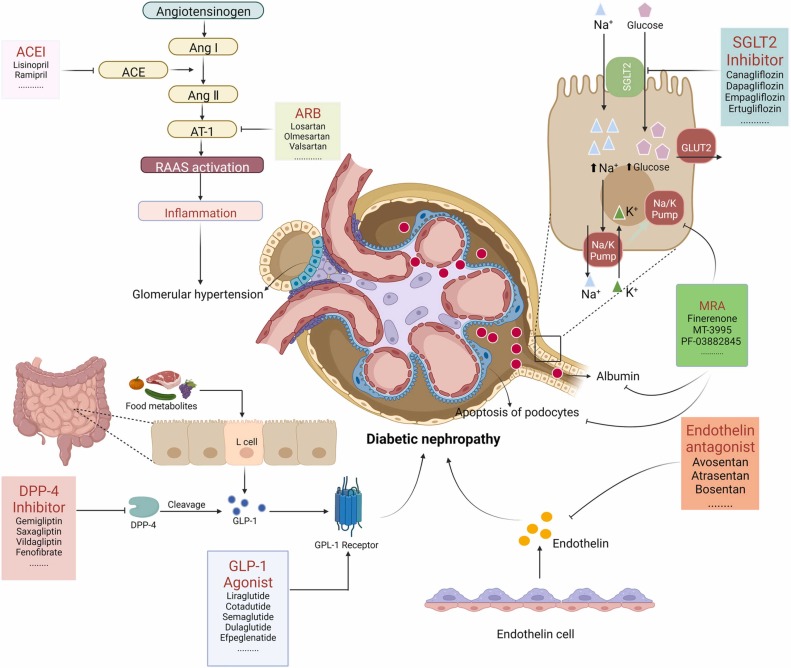
阻断RAAS
如上所述,RAAS通过ACE将血管紧张素I转化为血管紧张素II,从而激活肾脏炎症。因此,通过ACEIs和 ARBs阻断RAAS对DN患者具有肾保护作用。卡托普利是第一个用于治疗DN的ACEI药物。利辛普利(NCT00118976)是一种ACE抑制剂,可有效降低1型糖尿病DN患者的白蛋白排泄率。另外两项评估雷米普利效果的试验(NCT00893425和NCT01703234)已经完成,在替米沙坦疗法联合雷米普利试验中显示出了有益的效果。有几项试验(NCT00774904、NCT00361023和NCT00561704)验证了常用血管紧张素受体阻滞剂洛沙坦的效果,从而证明洛沙坦可通过抑制氧化应激和降低胰岛素抵抗来治疗2型糖尿病患者的DN。然而,有证据表明,洛沙坦治疗对减缓早期DN患者GFR的下降无益(NCT00340678)。
SGLT2抑制剂
在肾近曲小管中,SGLT2对肾功能和血糖稳态以及肥胖和能量代谢具有广泛的影响。初步研究表明,SGLT2 抑制剂主要通过增加尿糖排泄来控制2型糖尿病的血糖。随后的研究主要集中在通过SGLT2抑制剂改善肾功能,因为SGLT2在Na+重吸收中发挥虽小但重要的作用。多项临床试验的现有数据已经证明了SGLT2抑制剂对血糖控制和肾脏的益处,这有助于巩固其在DN患者治疗中的作用。
GLP-1激动剂
GLP-1是肠道L细胞分泌的肠促胰岛素激素,促进胰岛细胞分泌胰岛素,抑制胰高血糖素分泌,从而相应降低血糖。GLP-1受体广泛分布于多种器官,包括肾、肺、胃等。此外,GLP-1的激活可抑制血管紧张素II介导的炎症并抑制氧化应激和蛋白尿。由于这些作用,GLP-1激动剂代表了DN患者的一种新的潜在选择。
MRAs
盐皮质激素受体分布于肠道、心脏和血管组织中,其表达可分为“经典”和“非经典”组织。经典盐皮质激素受体主要分布在醛固酮敏感的远端肾小管中。盐皮质激素受体的非典型表达主要位于各种细胞上(就肾脏而言,主要位于足细胞上)。螺内酯是最具代表性的MRA;但由于选择性较差,很快就被淘汰了。因此,依普利酮是在螺内酯的基础上开发的,螺内酯对MR的体外亲和力相对较低。不幸的是,依普利酮在DN患者中的使用因其自身的高钾血症风险而受到限制。幸运的是,以finerenone为代表的非甾体MRA为DN治疗带来了新的潜力。近年来,大量研究集中在非甾体MRA的活跃领域。
内皮素拮抗剂
1988年,内源性血管收缩剂内皮素被发现,它由三种结构相似的肽(内皮素1、2和3)组成,参与多种血管收缩途径 。有证据表明它在糖尿病患者中过度表达。内皮素受体拮抗剂已被证明可以改善肾脏微循环并减少尿蛋白。基于上述迹象,已经进行了许多临床试验来验证内皮素受体拮抗剂对DN患者的疗效。
干细胞治疗糖尿病肾病的临床试验
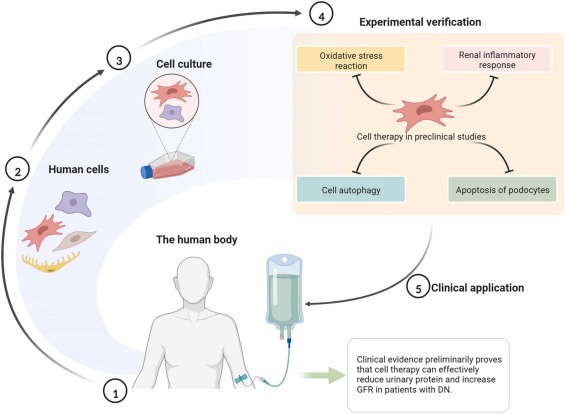
使用能够修复的细胞(包括间充质干细胞、肾自体细胞和间充质基质细胞)针对DN的细胞疗法可能会带来新的治疗机会。最近的研究表明,间充质干细胞在临床前研究中显示出对DN的初步疗效,并且可以通过抑制足细胞的炎症和凋亡来修复肾损伤。这些实验结果可以为DN细胞疗法的临床应用铺平道路。
在澳大利亚,一项临床试验(表2,NCT01843387)是第一项研究成人同种异体骨髓源性间充质前体细胞(MPC)对DN患者的疗效和安全性的研究。结果表明,与安慰剂相比,MPC治疗的患者在第12周表现出稳定或改善eGFR和mGFR的趋势。
| 细胞疗法 | 注册号 | 阶段 | 注册 | 地位 |
|---|---|---|---|---|
| 间充质前体细胞 (MPC) | NCT01843387 | 一/二 | 30 | 完全的 |
| 人胎盘来源细胞 (PDA-002) | NCT02552277 | 二 | 26 | 完全的 |
| 脐带间充质干细胞 | NCT04125329 | Ⅰ | 15 | 招聘 |
| 间充质基质细胞 | NCT02585622 | 一/二 | 48 | 招聘 |
| 自体脂肪间充质干细胞/基质细胞(MSC) | NCT03840343 | Ⅰ | 30 | 招聘 |
| 同种异体脂肪来源的间充质干细胞(MSC) | NCT04869761 | Ⅰ | 40 | 招聘 |
| 自体肾自体细胞疗法 (REACT™) | NCT03270956 | 二 | 10 | 主动,不招聘 |
| 自体肾自体细胞疗法 (REACT™) | NCT02836574 | 二 | 83 | 主动,不招聘 |
| 沃顿果冻间充质干细胞 | NCT03288571 | 一/二 | 20 | 未知 |
| 人脐带间充质干细胞(UC-MSC) | NCT04562025 | 不适用 | 38 | 未知 |
| 人脐带间充质干细胞(UC-MSC) | NCT04216849 | 一/二 | 54 | 未知 |
此外,另一项研究发现,T1D患者联合移植脐带间充质干细胞(MSC)和骨髓间充质细胞可降低慢性糖尿病并发症的发生率。更多关注MSC在DN管理中的功效和安全性的研究正在进行中(表2)。
此外,一项针对2型DN患者的自体肾细胞治疗的新临床试验即将在中国开展,这将为DN的细胞治疗带来新的推动力。总体而言,细胞疗法治疗DN仍处于起步阶段,相关临床试验大多处于小样本的1期或2期;然而,其良好的初步疗效预计需要通过更大规模的试验进一步验证(图4)。
糖尿病肾病患者的饮食干预
毫无疑问,DN患者的营养状况和膳食摄入是影响其病程和转归的关键和干预因素。尽管人们已经认识到糖尿病患者需要健康均衡的饮食,但对于DN患者的饮食要求更高,因为DN患者的饮食需要延缓肾脏损害的进展。更重要的是,根据患者的治疗方案调整饮食至关重要。
除了药物治疗和新兴的细胞疗法之外,持续的临床实践已经证明了饮食干预在DN患者管理中的重要性。众所周知,人体营养过剩会导致肾功能受损。例如,高蛋白饮食会加重CKD的进展并增加尿毒症毒素的水平,例如微生物硫酸吲哚、吲哚和硫化氢(H2S)。同样,过量的盐摄入被怀疑会通过多种机制加剧肾脏疾病的症状,例如增加蛋白尿。此外,糖的摄入量对于DN的饮食限制也至关重要。因此,低盐、低蛋白饮食,包括限糖,已成为控制DN进展的共识。此外,一些新颖的饮食探索已被证明可以为DN患者提供最佳解决方案。
近年来,以高脂肪、中等蛋白质和低碳水化合物饮食为特征的生酮饮食被认为是抑制DN的有效饮食干预措施。最初,一项临床前研究表明,为期2个月的生酮饮食干预通过降低小鼠白蛋白/肌酐比率有效缓解 DN。最近,一项随机临床试验评估了DN患者接受6个月生酮饮食干预后肾功能的变化 (NCT05071287)。最近发现补充短链脂肪酸(SCFA)或高纤维饮食可以通过诱导G蛋白偶联受体GPR43和GPR109A的激活来减少肾脏炎症和氧化应激。
临床上,目前正在进行一项试验,研究补充高膳食纤维对DN患者的影响(NCT01838330)。地中海饮食是一种饮食干预方式,主要涉及植物性摄入,包括水果、蔬菜、豆类、豆类、橄榄油和坚果,可能有利于 DN管理。一项临床研究表明,地中海饮食可以有效预防DN患者心血管疾病的发生并改善肾功能(NCT00924937)。如上所述,AGEs是DN发生过程中的重要影响因素。
因此,AGEs饮食限制已成为DN患者饮食干预的新目标。一项临床试验表明,限制AGE的饮食有利于平衡晚期肾病患者的肠道微生物(NCT02467530)。此外,最近的研究表明,添加一些营养素,如鱼油、维生素和咖啡因,有利于DN管理。
结束语
目前,DN占糖尿病患者的30%以上,是终末期肾病的最常见原因,对世界健康产业产生重大影响。目前,如何阻止DN的进展是一个紧迫的问题。
事实上,通过ACEI和ARB抑制RAAS是20年来治疗DN患者的唯一治疗选择,这仍然是治疗DN患者的基石。令人鼓舞的是,一些新发现的治疗靶点已经开发出来,为该领域的DN治疗带来新的希望,例如SGLT2抑制剂(卡格列净)、GLP-1激动剂和MRA(finerenone)等其他药物。令人鼓舞的是,其他调节新靶点的药物正在受到公众的关注。
除药物治疗外,细胞疗法也越来越受到公众的关注,其新颖的治疗方法主要包括间充质干细胞、肾自体细胞和间充质基质细胞。然而,这种新兴疗法仍处于起步阶段。
此外,我们强调日常饮食调节在DN管理中的重要作用,并支持根据KDIGO 2020年慢性肾脏病糖尿病管理临床实践指南将药物与饮食调整相结合的策略。日常饮食的调节(尤其是已被证明具有保护作用的低盐低蛋白饮食)可以通过降低高血压和白蛋白肌酐比来减轻肾脏损伤并抵抗炎症和氧化应激反应。不同的治疗方法搭配不同的饮食调整。因此,这些饮食调整(结合RAAS阻断等药物治疗)将形成DN治疗的生力军。
总之,本文总结了糖尿病肾病的重要病理机制、临床试验中的药物开发、干细胞疗法和饮食调节。我们强调治疗和饮食调节相结合在糖尿病肾病治疗中的重要性。我们期待更多的基础研究或临床试验来验证治疗DN的新策略。
参考资料:https://doi.org/10.1016/j.biopha.2023.114252
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号