介绍:慢性阻塞性肺病 (COPD) 是一种主要的慢性呼吸系统疾病,影响全世界超过3.8亿人。据估计,到2023年,COPD将成为全球第三大死因。肺实质损伤(肺气肿)和严重的气流阻塞是COPD的典型病理生理特征。
慢性阻塞性肺病全球倡议 (GOLD) 根据肺活量测定气流阻塞的严重程度定义了COPD的阶段。第一秒用力呼气容积 (FEV1)/用力肺活量 (FVC) <0.70的患者,对于FEV1≥80%的预测值,这些患者的阶段被定义为轻度。如果FEV1≥50%且<预测值的80%,则该阶段定义为中度。如果FEV1≥30%且<50%的预测值,阶段被定义为严重。如果FEV1<预测值的30%,则该阶段定义为非常严重。
目前可用的药物主要集中在缓解COPD患者的症状上。已经研究了新的再生治疗方法,目的是修复或替换呼吸系统受损的功能结构。再生方法
再生方法包括外源性细胞疗法,例如输注外源性干细胞以修复呼吸系统的受损结构,以及内源性细胞疗法,例如给予小分子刺激内源性肺干/祖细胞再生和替代损坏的结构)。这是第一个全面的综述,旨在根据从当前已完成的临床前研究和临床试验中获得的经验,讨论更有效的COPD干细胞治疗方案。

外源性细胞疗法
已经研究了多种外源性干细胞用于在COPD动物模型中治疗COPD。这些干细胞包括胚胎干细胞 (ESC)、诱导多能干细胞 (iPS)、间充质干细胞 (MSC) 和肺干细胞 (LSC)。
研究报告称,小鼠和人源性ESC均可在体外分化为AECII样细胞。AECII样细胞表达表面活性蛋白,例如表面活性蛋白C (SPC),这是AECII细胞的标志物。AECII样细胞(5×105) 将来自人类ESC系的小鼠气管内注入免疫缺陷的 SCID/C57BL/6小鼠,这些小鼠在BLM攻击后1或2天服用博来霉素 (BLM) 以诱导急性肺损伤。对照小鼠用生理盐水处理。给药后10天,与对照小鼠相比,AECII样细胞治疗显着减少了肺泡结构损伤,细胞浸润减少,间质增厚减少,肺部胶原蛋白沉积减少。
通过将源自小鼠iPS细胞系的AECII样细胞(5×105)移植到施用BLM后的C57BL/6小鼠,也证实了对受损肺的改善作用。移植后12天,与接受AECII样细胞治疗的小鼠相比,接受AECII样细胞治疗的小鼠纤维化程度降低,表现为胶原蛋白沉积减少,肺组织结构得到恢复。
然而,尽管上面提到的两项成功的临床前研究显示了肺结构再生的潜力,但仍然没有临床试验报告或注册使用来源于ESCs或iPS细胞,或ESCs,或iPS细胞治疗COPD患者。不应用这些细胞类型的原因包括:ESCs有形成畸胎瘤和免疫排斥的可能性,而且ESCs的应用存在伦理问题;iPS细胞也可以形成畸胎瘤,目前的技术无法产生可靠数量的临床级iPS细胞。
使用MSCs治疗COPD的治疗方法已被广泛研究。除了MSCs,c-kit阳性的LSCs可能是治疗COPD的新候选产品。现在更详细地讨论MSC和LSC。
间充质干细胞
注入MSCs的临床前结果
MSC是一群多能细胞,可以分化成多种细胞类型,包括成骨细胞、软骨细胞和脂肪细胞。鉴于免疫原性低的特点,来自骨髓或脂肪的自体和同种异体间充质干细胞(BM-MSCs和AD-MSCs)已被广泛应用于临床前研究。据报道,同种异体MSCs的动物受体对这些注射给药的细胞耐受良好。
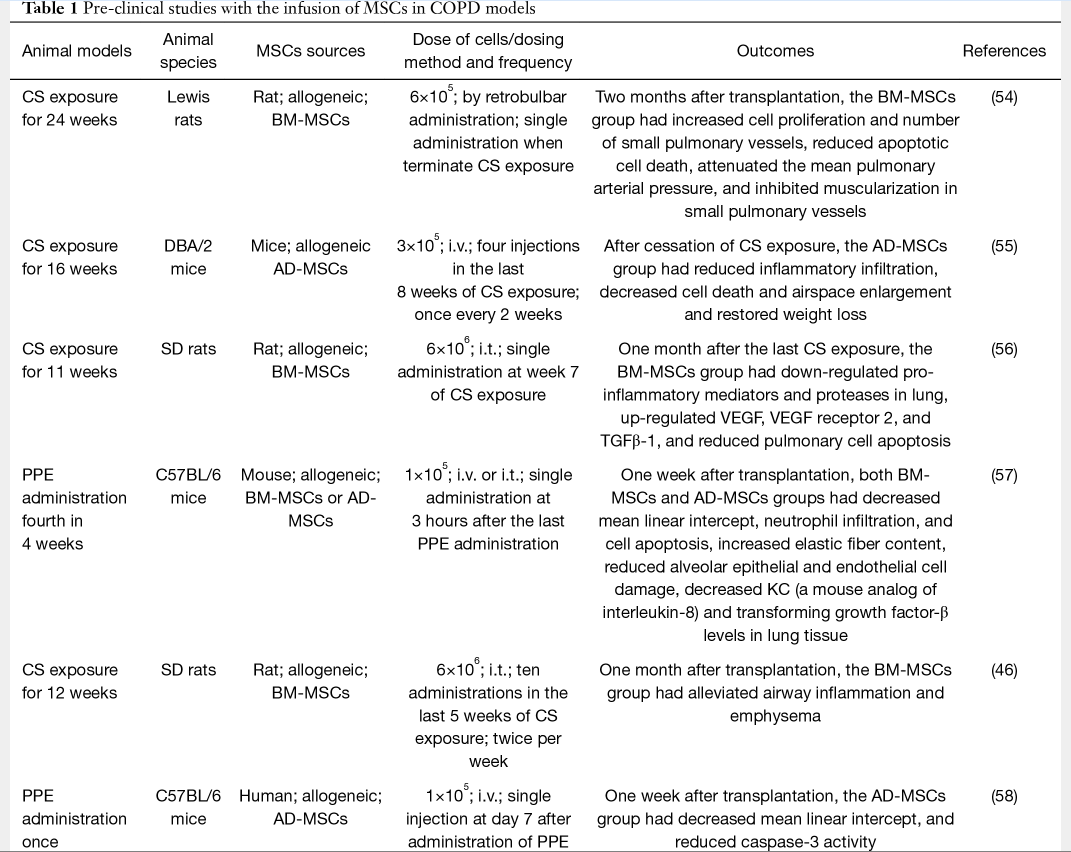
临床前研究报道了在COPD模型中外源性MSCs对受损肺的结构修复和功能恢复。表1列出了在COPD模型中应用MSC的代表性临床前研究。这些临床前研究将同种异体BM-MSC或AD-MSC应用于不同COPD模型,这些模型由 CS或PPE在不同品系的小鼠或大鼠中诱导。不同研究的细胞剂量、给药频率和给药方法各不相同。尽管存在这些差异,但所有研究都在干细胞移植后的数周或数月内呈现出积极的结果。积极的结果主要表现为减少炎症和减少空域扩大。
输注间充质干细胞的临床结果
2008年至2010年间,一项开创性的多中心、双盲和安慰剂对照II期临床试验 (NCT00683722) 将MSCs应用于中度至重度COPD患者。在该试验中,62名登记患者中的30名接受了同种异体BM-MSC移植。其他32名患者接受安慰剂治疗。在随后的2年中,未检测到外源性BM-MSC的毒性反应,并且在输注BM-MSC后未发现功能变化。仅在第一次输注后1个月,C反应蛋白 (CRP) 水平与输注前相比略有下降。
第二项已完成的临床试验 (NCT01110252) 在COPD患者中应用自体骨髓单核细胞 (BMMC),并于2009年至2011年间进行。招募了四名患有严重COPD的患者。静脉注射GTT,单次输注。没有报告与BMMC移植相关的副作用。在接下来的2年内进行了肺功能测试。与预测值相比,四名患者中有两名表现令人满意,FEV1增加,表明空气滞留减少和弹性增加。
作者指出,根据报告的临床前研究和首次报告的临床试验 (NCT00683722),肺功能相对改善可能是由于抗炎作用。
第三项完成的临床试验(NCT01306513)是一项开放标签、非随机、非盲、前瞻性I期临床试验。该试验于2010年至2012年间进行。在进行第一次肺减容手术 (LVRS) 时,从7名严重至非常严重的COPD患者中收集骨髓,并离体培养以获得BM-MSC。两次输注自体BM-MSCs,第一次是在LVRS后6-10周,第二次是在第一次输注后1周。所有患者在第二次输注BM-MSC后3周进行第二次LVRS。没有观察到与BM-MSCs输注相关的毒性。第二次LVRS一年后,FEV1和体重显着增加,与第一次LVRS之前相比,所有患者的肺密度测定也发生显着变化。但这些变化与之前报告的只有LVRS的患者相当,表明肺结构、功能和体重的改善是由LVRS而不是BM-MSCs引起的。
总之,这项研究表明了自体BM-MSCs在重度和极重度COPD患者中的安全性和可行性。
表2给出了在COPD患者中应用MSC的三个已完成临床试验的信息。

已报道的COPD间充质干细胞临床试验的适应症
成功的临床前研究为在COPD患者中使用各种来源的MSCs进行进一步的临床研究提供了重要基础。然而,鉴于报告的少数初步临床试验均未成功,这削弱了将MSCs应用于COPD患者的潜力。最近注册了旨在使用BM-MSC或AD-MSC治疗COPD的进一步临床试验,但这些试验尚未开始。
所研究患者的晚期阶段可能是失败的主要原因。目前报道的三项临床试验招募了中度、重度或极重度COPD患者。
第一项临床试验 (NCT00683722) 的作者表示,患者的COPD阶段可能是失败的主要原因。他们还指出,对肺部结构的损害可能太严重而无法被少数移植的MSCs逆转。临床前研究中广泛使用的COPD模型只能模拟轻度或至多模拟COPD患者的中度阶段,这或许可以解释为什么临床前研究均有MSCs移植后的结构修复和功能改善。有趣的是,据报道,与肺气肿较弱的动物(由一种刺激诱导)相比,具有更强肺气肿(由两种刺激诱导)的动物在肺中募集和移植了更多的外源性MSCs。
因此,我们可以预测,晚期COPD患者也可能会在肺部募集和移植更多的外源性MSC,因此应该会导致结构修复和功能恢复,如动物模型所示。然而,已完成的临床试验并未达到我们的预期。尽管如此,这提醒我们可以做进一步的研究来研究如何增强外源性间充质干细胞在受损肺中的植入。此外,由于具有抗炎和免疫调节的特性,外源性间充质干细胞在急性肺病中可能比在具有严重结构损伤的慢性、进行性疾病中更有效。
外源性MSCs的状态也是试验成败的关键。
第一次临床试验(NCT00683722)中使用的同种异体间充质干细胞从冷冻袋中解冻后立即在床边直接输注。这种工业过程使移植变得简单方便。然而,数据表明新解冻的MSCs已经失去了部分免疫调节能力。
第一次临床试验(NCT00683722)和第三次临床试验(NCT01306513)的失败可能都与新解冻细胞的应用有关。因此,未来的试验设计应使用新鲜的MSC或解冻后约24小时培养的MSC。
第二个临床试验(NCT01110252)使用新鲜的自体BMMCs,并没有表现出明显的改善。
除了COPD分期、MSC状态(新鲜或冷冻,来自较年轻或年老的供体),其他重要参数包括细胞剂量、给药方法、给药频率以及研究终点的设计、患者病例的年龄和规模, 包括适当的对照组。这些不同的参数可能共同导致了临床前研究和临床研究之间出现的相互矛盾的结果。
内源性细胞疗法
理论上,激活内源性干细胞或祖细胞以诱导功能性肺泡上皮细胞再生可能是逆转COPD的替代方法。基于内源性干细胞或祖细胞的动员,这种再生方法被命名为“内源性细胞疗法”,这是一种不同于外源性细胞疗法的方法。
以前,在人类呼吸系统中鉴定的干/祖细胞包括基底细胞、Clara细胞、肺间充质干细胞和气道中的c-kit阳性LSC以及肺泡中的AECII细胞。据报道,基底细胞和AECII细胞可以从静止状态重新进入细胞周期;它们可以在肺损伤后繁殖并促进组织修复。激活这些干细胞/祖细胞的研究仍处于较早的研究阶段,尚未在临床前和临床研究中得到充分批准和广泛应用。
结论
考虑到目前可用的药物主要侧重于缓解症状,预计新方法将逆转结构退化并改善COPD患者呼吸系统的功能。干细胞疗法可以通过修复或更换受损结构来改善肺功能。
基于大量MSCs临床前研究和初步临床试验的数据,以上讨论了临床试验失败的可能原因。失败的主要原因可能是外源性MSCs对中重度COPD患者广泛受损的肺结构的抗炎和免疫调节作用不足。为了增强效果,必须考虑几个参数,包括细胞状态(新鲜或冷冻,来自年轻或衰老的供体)、细胞剂量、给药方法、给药频率。
至于细胞的状态,建议将来自年轻捐赠者的新鲜而非冷冻的BM-MSC或AD-MSC用于未来的研究。此外,还应该更加努力地精心设计新的试验,包括研究终点、患者年龄、状态和规模的设计,对于使用外源性 hLSC 的外源性细胞疗法和使用可激活内源性干细胞/祖细胞的分子的内源性细胞疗法,在开始新的临床试验之前应收集更多的临床前证据。
总之,所讨论的再生疗法方法已在COPD动物模型中显示出积极作用,并且在临床试验中是安全的。然而,必须付出更大的努力来开发能够为COPD患者提供治愈方案的方法。
参考资料:Sun Z, Li F, Zhou X, Chung KF, Wang W, Wang J. Stem cell therapies for chronic obstructive pulmonary disease: current status of pre-clinical studies and clinical trials. J Thorac Dis 2018;10(2):1084-1098. doi: 10.21037/jtd.2018.01.46
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号