简介:脊髓损伤 (SCI) 仍然是一种无法治愈、改变生活的神经系统疾病,导致全世界数百万人永久丧失运动和感觉功能,并影响他们个人和社会生活的各个方面。在过去的二十年中,干细胞疗法在各个医学领域取得成功后,作为SCI的潜在治疗方法在研究领域进行了研究。
近期,雅典KAT医院医学院在《Cureus》医学杂志期刊上发表一篇关于干细胞疗法在脊髓损伤方面进行的临床试验的文章,文章侧重于介绍SCI的病理生理学、用于治疗的不同干细胞疗法的特点,以及这些疗法在最近发表的临床试验中的结果。
如何让干细胞疗法安全以及有效地帮助脊髓损伤病人,这是科学家们正在做的事情。每一项临床试验进展,都是在为脊髓损伤的治疗和康复做加法!

脊髓损伤的介绍与背景
每年,全世界大约有500,000起新的脊髓损伤 (SCI) 事件。在大多数情况下,原因是车祸、跌倒、枪击或医疗/手术并发症造成的外伤。由于其原因的性质,脊髓损伤仍然是一种主要影响年轻人的疾病。然而,随着我们生活在一个不断老龄化的社会中,低能量创伤后老年人群中新发脊髓损伤病例也在增加。损伤后病理生理事件的后遗症通常会导致永久性神经功能缺损,例如损伤水平以下的运动和感觉功能丧失以及自主神经功能障碍。
目前的临床实践侧重于SCI部位的早期手术减压和机械稳定,然后进行药物干预,例如甲泼尼龙、尼莫地平、纳洛酮等。在第一个关键阶段之后,患者参与康复计划以重新获得功能和自主权。不幸的是,所有这些干预措施在神经保护、神经再生和功能恢复方面都表现不佳。这一失败背后的原因在于脊髓损伤病理生理机制的复杂性,导致损伤部位的神经元环境受到不可逆的损伤。
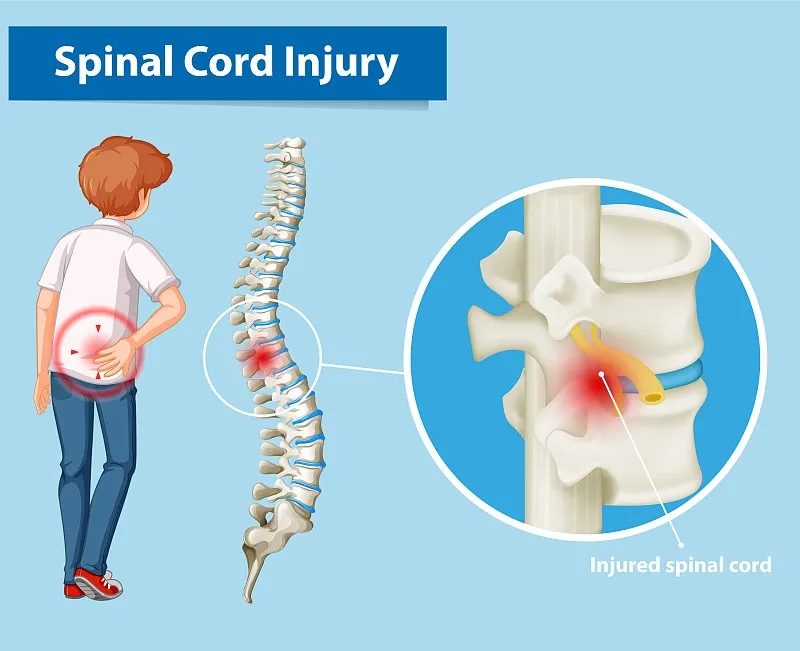
在过去的几十年中,干细胞疗法已成为SCI领域非常有前途的解决方案。在不同物种的动物身上使用不同类型的干细胞进行了大量令人鼓舞的治疗试验后,涉及人类脊髓损伤的临床试验在本世纪第一个十年中期成为现实。本综述阐述了SCI 的病理生理学、不同干细胞在脊髓修复中的可能作用机制,并介绍了PubMed在线图书馆最近五年发表的相关临床试验的基本特征和结果。
脊髓损伤的病理生理学
原发性和继发性伤害
SCI病理生理学可分为两个阶段。第一种称为原发性损伤,发生在机械力作用于脊髓时,导致神经元组织受压、撕裂、牵拉或剪切,同时损伤血管和周围组织。研究表明,原发性损伤几乎从不完全破坏脊髓的解剖学连续性。
继发性损伤又可进一步分为四个阶段:即刻(伤后0-2小时)、急性(急性早期:2-48小时、亚急性:2天-2周)、中期(2周-6个月)、和慢性期(>6个月)。
第一个可检测到的变化是脊髓普遍肿胀并伴有中央灰质出血。细胞膜的直接破坏和血管损伤引起的缺血导致细胞坏死性死亡,从而导致白质出血并产生可能延伸到许多脊柱节段的脊髓缺血。在此阶段,肿瘤坏死因子-α (TNF-α) 和白细胞介素-1β (IL-1β) 等促炎细胞因子被上调,炎症开始。离子失调、谷氨酸兴奋性毒性和免疫神经毒性等次级过程加剧了轴突死亡。自由基介导的脂质过氧化作用导致轴突破坏。血脊髓屏障的破坏会诱发神经炎症,进一步导致神经细胞死亡。
在亚急性期,病灶周围的星形胶质细胞肥大、增殖,长出多个大的胞质突起。这些细胞质突起结合形成神经胶质瘢痕。
在随后的中间阶段,神经胶质瘢痕成熟。最后,在慢性损伤阶段。
研究的目的是回顾2017年1月1日至2022年期间发表的使用干细胞治疗脊髓损伤的临床试验。共有18项临床试验被纳入本综述。
临床试验中使用的干细胞治疗脊髓损伤的概述
表1按细胞类型和发表年份总结了经过审查的临床试验。
| 作者 | 临床试验阶段 | 细胞起源 | 细胞类型 | 剂量 | 给药途径 | 患者人数 | AIS 分类或受伤程度 | 受伤时间(急性/亚急性/慢性期) | 跟进 | 主要结果(功能改善/不良反应) |
| Honmou 等人2021 | 二期 | 自体的 | BMSC(自动血清扩展) | 84 − 150 × 10 6 | 静脉 | 13 | AIS A:6,B:2,C:5 | 亚急性 | 6个月 | AIS A→B(3/6 患者)、A→C(2/6)、B→C(1/2)、B→D(1/2)、C→D(5/5)。根据 ISCSCI-92 和 SCIM-III 量表的功能改进。 |
| Phedy 等人。[24] 2019 | 案例报告 | 自体的 | 骨髓间充质干细胞 | 10 − 17 × 10 6 (× 7 次) | 鞘内 x1 静脉 x6 | 1个 | AIS A T12 | 慢性的 | 5年 | AIS A→C。AIS 分数增加:10→30。L1 和 L2 神经支配肌肉的 MRC 评分增加:0/5→3/5。 |
| Vaquero 等人。[25] 2018 | 二期 | 自体的 | 骨髓间充质干细胞 | 100 × 10 6 × 3 剂量 | 鞘内 | 11 | A: 3, B: 4, C: 3, D: 1 | 慢性的 | 10个月 | 27% 的患者 AIS 得到改善。 |
| Vaquero 等人。[26] 2018 | 二期 | 自体的 | 骨髓间充质干细胞 | 100 × 10 6 | 髓内 | 6个 | A: 3, B: 2, D: 1 | 慢性的 | 6个月 | 2 例 AIS 改善。大便和膀胱功能得到改善。4 名患者的 NCS 结果有所改善。 |
| 瓜达拉哈拉[27] 2018 | 案例报告 | 自体的 | 骨髓间充质干细胞 | 300 × 10 6 × 3 剂(1 次/月) | 鞘内 | 1个 | AIS A T12 | 慢性的 | 6个月 | 改善功能,尤其是 Krogh 的神经源性肠功能障碍量表。 |
| Vaquero 等[28] 2017 | 二期 | 自体的 | 骨髓间充质干细胞 | 30 × 10 6 × 4 剂量 | 鞘内 | 10 | 颈椎、胸椎、腰椎 | 慢性的 | 12个月 | AIS 改进。运动和感觉得分得到改善。 |
| 邓等。[29] 2020 | 第一阶段 | 同种异体 | UCMSC+ 脚手架 | 40 × 10 6 (胶原支架) | 髓内 | 20 | AIS A 颈椎病 | 急性 | 12个月 | AIS A→B(9 名患者),AIS A→C(2 名患者)。提高 ADL 分数。改善肠道和膀胱功能。 |
| 杨等。[30] 2020 | 第一/二期 | 同种异体 | 加州大学医学中心 | 1×10 6 /kg(×4次) | 鞘内 | 41 | C1-C7:24,T1-T9:7,T10-L1:10 | 亚急性或慢性 | 12个月 | AIS 和 IANR-SCIRFS 分数的统计增加。减少肌肉痉挛。无严重不良反应。 |
| 肖等。[31] 2018 | 第一阶段 | 同种异体 | UCMSC+ 脚手架 | 40 × 10 6 | 髓内 | 2个 | AIS A C4, T11 | 急性 | 12个月 | 两名患者的 AIS A→C。 |
| 阿尔布等。[32] 2020 | I/IIa期 | 同种异体 | WJ-MSC | 10 × 10 6 | 鞘内 | 10 | T3-T11 | 慢性的 | 6个月 | 与安慰剂组相比,针刺感显着改善。运动功能、独立性、QoL、SEP、MEP、痉挛或肠功能没有变化。 |
| 柯特等人。[33] 2020 | I/IIa期 | 同种异体(干细胞公司) | huCNS-SC® | 20 × 10 6 | 髓内 | 12 | A: 7, B: 5 (T2-T11) | 亚急性或慢性 | 6年 | 12 名患者中有 5 名感觉得到改善。没有观察到运动改善。 |
| 列维等。[34] 2019 | 第一/二期 | 同种异体(干细胞公司) | huCNS-SC® | 15 + 30 + 40 × 10 6 (Coh.I) 40 × 10 6 (Coh.II) | 髓内 | 17 队列 I:6,队列 II:11 6/11 监测 | AIS A、B 颈椎 | 亚急性或慢性 | 12个月 | 申办者提前终止试验。UEMS 分数的提高。无不良影响。 |
| 列维等。[35] 2018 | 第一/二期 | 同种异体(干细胞公司) | huCNS-SC® | 15 – 40 × 10 6 | 髓内 | 29 | 颈椎:17(队列 I:6,队列 II:11)胸椎:12 | 亚急性 | 长达 56 个月 | AIS 运动评分的改善。颈椎组 15 例严重不良反应,胸椎组 4 例。 |
| 柯蒂斯等人[36] 2018 | 第一阶段 | 同种异体(Seneca Biopharma) | NSI-566® | 6 次注射(平均数) | 髓内 | 4个 | AIS 胸部 | 慢性的 | 60个月 | 改进的 AIS 分数、神经学水平和 EMG 结果。QoL 没有改善。无严重不良反应。 |
| 扎马尼等人[37] 2022 | 第一阶段 | 自体的 | OEC+ 骨髓基质干细胞 | 15 × 10 6 , OEC/BMSC = 1/1 | 鞘内 | 3个 | 自动识别系统 | 慢性的 | 24个月 | AIS A→B:SCIM 提高 1 点和 6 点。轻微的不良反应。 |
| 甘特等人。[38]2021 | 第一阶段 | 自体(腓肠神经) | SC | 50 − 200 × 10 6(取决于患者的囊肿体积) | 髓内 | 8个 | 颈椎:4 胸椎:4 | 慢性的 | 5年 | 1例患者神经功能水平提高1级。所有胸部病变患者和 2 名颈部病变患者的感觉评分均有改善。 |
| 安德森等人[39] 2017 | 第一阶段 | 自体(腓肠神经) | SC | 5、10 或 15 × 10 6 | 髓内 | 6个 | 胸椎 | 亚急性 | 12个月 | AIS A→B:1。FIM 和 SCIM III 分数的提高。无不良影响。 |
| 斯米尔诺夫等[40] 2022 | I/IIa期 | 同种异体 | 华侨银行 | 14.8 × 10 6 /kg(4次输注的总细胞数) | 静脉 | 10 | A: 6, B: 4 | 急性(受伤后 3 天内) | 12个月 | 没有与治疗相关的严重不良反应。AIS A→C:3,AIS B→D:2,AIS B→E:2,AIS A→D:1 |
都有哪些干细胞用来治疗脊髓损伤?
间充质干细胞治疗脊髓损伤的临床试验
间充质细胞是多能祖细胞,可以很容易地从各种组织中分离出来,例如骨髓、脂肪组织、脐带和羊水。它们的使用不会引起伦理问题。此外,它们具有低致瘤性和免疫反应性。它们被认为通过分泌多种因子在损伤部位起作用,例如生长和粘附因子、抗炎因子和细胞因子。因此,它们的作用被认为具有抗细胞凋亡、神经营养、神经保护和免疫调节作用。
骨髓间充质干细胞:骨髓间充质干细胞 (BMSCs) 是从骨髓中提取的,它们是多能的,可以分化成各种细胞类型,包括成骨细胞、成纤维细胞、成软骨细胞、软骨细胞、脂肪细胞、神经元和神经胶质细胞。它们的有益特性似乎是通过它们的免疫抑制和神经保护作用而出现的,并且是由于在损伤部位释放的大量生长因子,例如 NGF(神经生长因子)、VEGF(血管内皮生长因子)、GDNF(神经胶质衍生的神经营养因子)因子)、BDNF(脑源性神经营养因子)、NT-3(神经营养因子3)、FGF(成纤维细胞生长因子)和EGF(表皮生长因子)。
在文献检索中确定了六项使用BMSC的临床试验。其中四个处于第二阶段,其中两个已作为案例研究发表。共有42名患者接受了此类干细胞治疗。在四项研究中,给药是鞘内给药,在一项研究中是静脉内给药,而在另一项研究中,细胞是通过静脉内和鞘内方法相结合的方式输送的。在42名患者中,13名在移植时处于亚急性损伤阶段,其余处于慢性阶段。
日本札幌医科大学医学院前沿医学研究所神经再生医学系,Honmou等人在2021年用自体骨髓间充质干细胞治疗了13名脊髓损伤亚急性期患者。其中6例为AISA型损伤,2例为AISB型,5例为AISC型。细胞在自体血清中扩增,剂量在84到1.5亿个细胞之间。有一次静脉注射细胞,对患者进行了六个月的随访。

结果很有希望,显示7名患者的AIS分类以及根据ISCSCI-92和SCIMIII量表的功能活动有所改善。
脐带间充质干细胞:脐带间充质干细胞 (UCMSC) 从人脐带中提取。它们可以很容易地在体外扩增并且具有低免疫反应特性。它们产生多种因子,例如细胞因子、生长因子、白细胞介素、BDNF、bFGF(碱性成纤维细胞生长因子)和中性粒细胞激活剂。人们认为,这些细胞在移植时表现出抗炎、抗凋亡、神经营养和促血管生成作用。
在这篇综述中,确定了三项使用UCMSCs的临床试验。在其中两个中,UCMSCs与支架相结合。支架是高度多孔的生物材料,具有生物相容性,可作为组织再生的模板,并可能引导新组织的生长。在这些临床试验中,63名患者参与了脊髓损伤的急性、亚急性或慢性阶段。
2020年,甘肃中医药大学中西医结合学院邓等研究人员移植髓内4000万细胞联合胶原支架治疗20例颈椎损伤(AIS A)。该支架由牛腱膜制成,并接种了4000万个UCMSC。患者接受了移植并接受了12个月的随访。对照组接受常规治疗(感染预防和支持治疗)。
12个月后,九名移植患者从AIS A转变为B,两名从AIS A转变为C。与对照组相比,ADL评分和肠/膀胱管理也有所改善。
2020年,中山大学第三附属医院脊柱外科杨等人发表了I/II期临床试验的结果。总共包括41名患有亚急性或慢性损伤的患者。他们接受了四次鞘内注射,每次注射一百万个UCMSC,并接受了12个月的监测。没有记录到不良反应。

结果显示AIS和IANR-SCIRFS评分增加,肌肉痉挛减少。
2018年,中国武警后勤大学附属医院神经外科与神经内科医院和戴建武等人在两名急性SCI患者 (AIS A) 中移植了4000万个UCMSCs联合NeuroRegen胶原支架。支架由牛腱膜制成。对患者进行了六个月的随访。
随访结束时,两名患者均已从AIS A转为C,且未记录到不良反应。
脐带沃顿-果冻间充质干细胞:沃顿胶是脐带内的一种凝胶状物质,可隔离血管。可以提取和培养Wharton-Jelly间充质干细胞 (WJ-MSC)。它们产生多种神经营养因子,并且由于释放显着水平的NGF、bFGF和GDNF,可以促进神经发生和血管发生。已经在动物身上证明,反复输注WJ-MSC可以减少胶质瘢痕,并且可以引起脊髓再生。
2021年,西班牙巴塞罗那自治大学阿尔布等在I/II期、RCT、安慰剂对照临床试验中使用WJ-MSCs治疗10名慢性SCI (T3-T11) 患者。患者通过鞘内递送接受细胞,并随访六个月。

在随访结束时,与安慰剂组相比,针刺感明显改善,而运动功能、独立性测量、QoL、SEP、MEP、痉挛或肠功能没有变化。神经干细胞治疗脊髓损伤的临床试验
神经干细胞 (NSC) 具有分化成胶质细胞、神经元和星形胶质细胞的能力。它们位于海马齿状回、侧脑室和脊髓中央管。研究表明,神经干细胞分泌生长因子,帮助受损细胞存活。它们增强少突胶质细胞分化,从而在髓鞘再生中提供支持作用。它们还可以增强神经分化、替换坏死的神经元、在灰质中形成突触并恢复功能。最后,它们充当屏障,防止初始病变区域扩大。
人类中枢神经系统干细胞和NSI-566®
HuCNS-SCs®是源自胎儿脑的人中枢神经系统干细胞祖细胞群。它们通过表面标记表达纯化、扩增,然后储存。HuCNS-SCs®已显示出神经保护能力,与胚胎干细胞相比,它们具有非致瘤性优势。几项使用HuCNS-SC治疗Pelizaeus-Merzbacher病、年龄相关性黄斑变性 (AMD) 和神经元蜡样脂褐质沉着症的临床试验已经完成,没有安全问题,移植细胞的存活率很高。
NSI-566®是一种人脊髓来源的神经干细胞系,源自八周大的流产胎儿的脊髓。它们已用于治疗ALS的临床试验。当注入脊髓时,它们会分化成神经元,支持受损的ALS运动神经元,并形成连接。它们的有益作用在于分泌多种神经营养因子。
自2017年初以来,已经确定了四项使用源自人类胎儿CNS的神经祖细胞的临床试验。其中三名患者接受了HuCNS-SC®治疗,一项临床试验使用了NSI-566®。共有62名患者接受了髓间细胞。
2018年,美国加州大学圣地亚哥分校神经外科系柯蒂斯等人发表了一项I期临床试验的结果,该试验的四名慢性胸椎AISA SCI患者平均接受了六次NSI-566®髓间注射。
对患者进行了60个月的监测,结果令人鼓舞,显示两名患者的神经水平(T8→T10和T5→T7)和AIS运动和感觉评分有所改善,其中三名患者的EMG结果有所改善,但无显着差异在生活质量。磁共振成像 (MRI) 和扩散张量成像 (DTI) 显示没有可见的形态学变化,也没有注意到不良反应。
2020年,瑞士苏黎世巴尔格里斯特大学医院柯特等人2020年在I/IIa期临床试验中使用HuCNS-SC®治疗12名亚急性或慢性胸部损伤患者。所有患者均接受了2000万个髓间细胞的单次剂量,并接受了六年的监测。
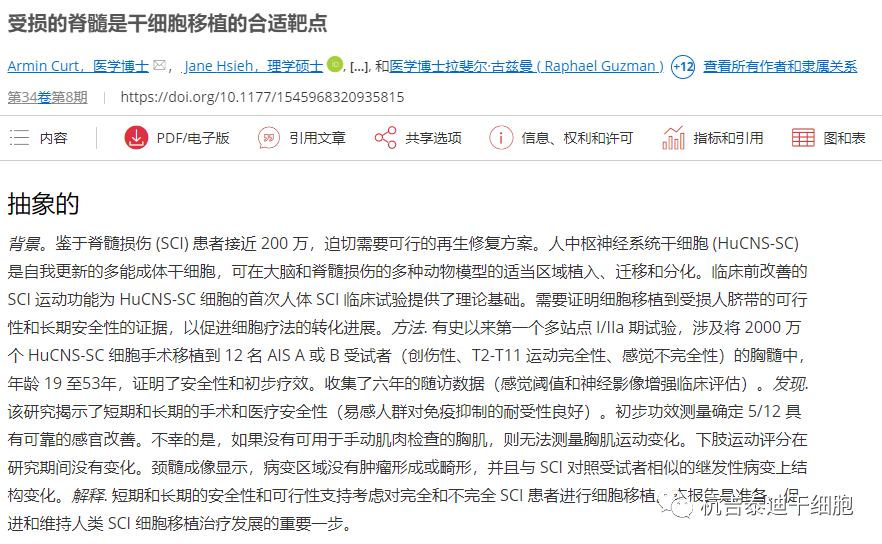
最终结果显示有部分患者的感觉有所改善 (5/12)。人脐带血细胞治疗脊髓损伤的临床试验
使用人脐带血细胞 (HUCBC) 是有利的,因为它易于获取且采集过程无创。人脐带血含有大量造血干细胞 (HSC),能够产生红系和髓系祖细胞集落。具体而言,人脐带血单核祖细胞(HUCBC)的增殖能力远高于骨髓中的同类细胞。它们表现出免疫耐受性,对人类白细胞抗原错配的反应性较低,因此可轻松用于同种异体移植。在病变部位,HUCBC似乎具有多因素作用。它们可以分化成神经谱系,表现出抗细胞凋亡作用,诱导血管生成和轴突髓鞘再生,并表达多种生长因子。
2022年,俄罗斯联邦NV Sklifosovsky急救护理研究所Smirnov等人发表了一项I/IIa期临床试验的结果,该试验使用HUCBCs通过静脉注射治疗10名急性SCI(AIS A或B)患者。在受伤后三天内,对每位患者进行了四次注射。参与者被跟踪了12个月。

没有报告与细胞疗法相关的不良反应。五名患者的AIS水平提高了两分(A→C,B→D),一名患者提高了三分(B→E)。
讨论
脊髓损伤的干细胞疗法仍处于起步阶段。每项临床试验都提供了研究领域的丰富知识。目前主要问题是除了使用的干细胞类型外,在首选给药途径、每剂细胞数、剂量数和移植时间方面存在很大的异质性。这样,各种试验结果就很难进行比较。
结论
基于干细胞的疗法为脊髓损伤提供了有趣的治疗潜力。使用生物材料的组合方法也可能在改善脊髓损伤治疗方面发挥重要作用。更深入地了解脊髓损伤的病理生理机制似乎对于开发比已经研究的治疗方法更有效的治疗方法至关重要。还需要解决几个问题,如各种干细胞的伦理问题、致瘤性、免疫原性和免疫毒性。
最后,似乎有必要增加资金以开展更强大、设计更完善的I期和II期临床试验,这些试验将引领未来几年的第一个III期研究。
参考资料:Damianakis E I, Benetos I S, Evangelopoulos D, et al. (April 28, 2022) Stem Cell Therapy for Spinal Cord Injury: A Review of Recent Clinical Trials. Cureus 14(4): e24575. doi:10.7759/cureus.24575
说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议,如有版权等疑问,请随时联系我。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号