随着全球细胞与基因治疗产业迈入了高速发展期,当前全球已登记的细胞与基因治疗相关临床试验已超过7000余项,其中近3000项已完成临床试验研究,并进行了数万例干细胞移植。
国内干细胞药物注册也正处在蓬勃发展的趋势中,自从2018年国家药品监督管理局药品审评中心(CED)重新受理干细胞新药临床试验申报以来,干细胞药物临床试验的申请稳步增长。就承办受理号总量,从2018年申报5个(以受理号计)增长至2022年的26个,较2021年度增长了一倍,我国干细胞新药研发速度明显加快。

表1 2018-2022年干细胞药品申报一览
01
申报情况
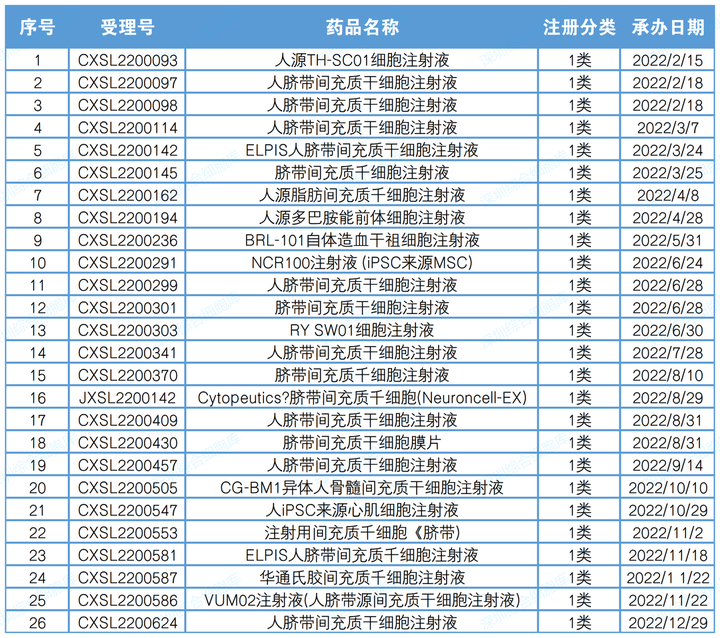
2022年CDE受理干细胞药物临床申请26项(以受理号计),其中国产1类创新药注册申请25项,进口1类创新药注册申请1项。进口干细胞药物为Cytopeutics脐带间充质干细胞(Neuroncell-EX)。
表2 2022年度干细胞药物注册申请受理清单
02
临床试验默示许可情况
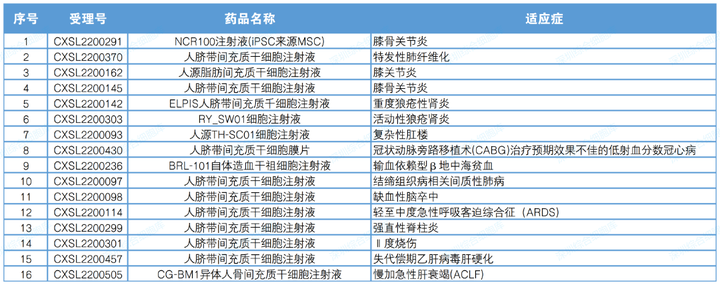
2022年CDE合计默许许可11款干细胞药物的16项临床试验。其中使用间充质干细胞的有11项,间充质干细胞使用类型占比达到68%。
表3 2022年度干细胞药物临床默示许可一览表
03
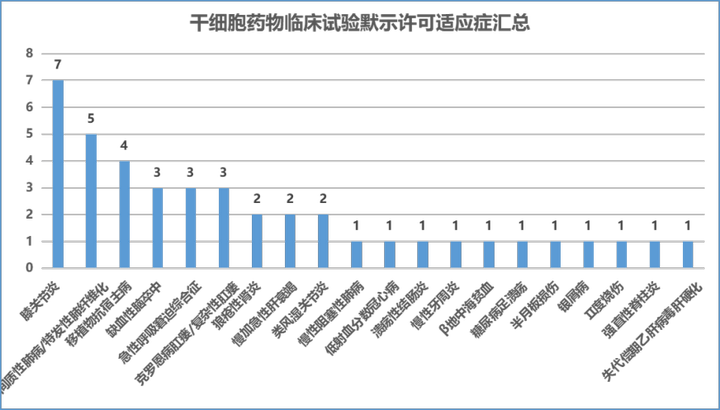
临床试验适应证分析申报的干细胞类型分析
截至2022年12月31日,CDE合计默许的42项临床试验涉及20项适应证。其中位于前三的分别是:膝关节炎(7项)、间质性肺病(主要是特发性肺纤维化)(5项)、移植物抗宿主病(GVHD)(4项)。其中膝骨关节炎的7款干细胞药物,干细胞类型包括:自体脂肪间充质干细胞(1种)、异体脂肪间充质干细胞(2种)、脐带间充质干细胞(3种)、人诱导多能干细胞来源的间充质样细胞(1种)。从适应证来看,绝大多数药物利用间充质干细胞的免疫调控能力以针对炎症相关或自身免疫系统相关等疾病展开治疗。干细胞药物针对的适应证情况。
04
2023年度干细胞药物申报或迎来更大爆发
全球细胞治疗领域在基础研究领域已取得诸多重大原创性成果,我国名列前茅。随着《干细胞临床研究管理办法 ( 试行) 》《干细胞制剂质量控制及临床前研究指导原则( 试行) 》《细胞治疗产品研究与评价技术指导原则(试行)》等政策出台,《深圳经济特区细胞和基因产业促进条例》的正式通过表决,我国干细胞临床转化逐步走向正轨,并逐渐明确了以干细胞药物作为转化出口的道路。
根据全球最大临床试验登记网站http://clinicaltrials.gov上的信息,诸如新冠感染后遗症、糖尿病、骨髓增生异常综合征、新生儿严重缺氧缺血性脑病、阴茎硬结症、勃起功能障碍等疾病的临床治疗研究也在应用干细胞开展治疗。
相信2023年度会是干细胞药物研发的爆发期,会有更多针对新适应证的干细胞药物进入临床试验阶段。同时,正在开展干细胞药物Ⅰ期/Ⅱ期临床试验也将逐步产生结果,相信随着干细胞技术研发的不断深入,干细胞作为治疗药物离上市将在不远的未来。
免责声明:
本文仅供参考并不构成任何应用建议,如文章内容涉及版权或其他问题,请及时跟本网站联系,我们将在第一时间处理。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号