
近期,国家药品监督管理局药品审评中心公开受理了四款干细胞新药,它们分别是来自浙江生创精准医疗科技有限公司的“宫血间充质干细胞注射液”(受理号:CXSL2400156)、江苏得康生物科技有限公司的“异体人源脂肪间充质干细胞注射液”(受理号:CXSL2400111)、深圳市北科生物科技有限公司的“人脐带间充质干细胞注射液”(受理号:CXSL2400092)以及吉林省拓华生物科技有限公司的“人脐带间充质干细胞注射液”(受理号:CXSL2400023)。这四款新药的受理日期分别为2024年2月26日、2024年2月8日、2024年2月3日和2024年1月10日。
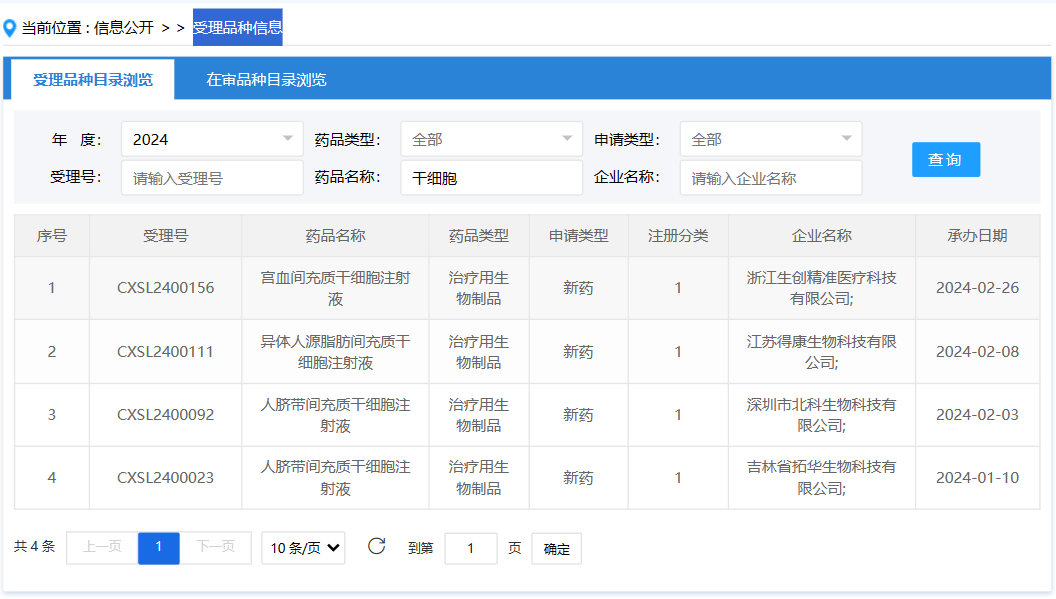
这四款新药均属于治疗用生物制品,且均为新药注册(1类),显示出我国在干细胞药物研发领域的持续创新和突破。值得一提的是,除了两款人脐带间充质干细胞注射液外,还有一款宫血间充质干细胞注射液和一款异体人源脂肪间充质干细胞注射液,进一步丰富了干细胞来源与治疗的种类和适应症范围。
总之,这四款新药的受理,不仅代表了我国在干细胞药物研发领域的最新成果,也为广大患者带来了新的治疗选择和希望。我们期待这些新药能够顺利通过审批,早日应用于临床,为更多患者带来福音。
信息来源:CDE
免责说明:本文仅用于传播科普知识,分享行业观点,不构成任何临床诊断建议!杭吉干细胞所发布的信息不能替代医生或药剂师的专业建议。如有版权等疑问,请及时跟本公众号联系,我们将在第一时间处理。




 浙公网安备 33010202002429号
浙公网安备 33010202002429号 官方微信公众号
官方微信公众号